Все послеоперационные травмы мочевого пузыря
Содержание статьи
Травма мочевого пузыря
Травма мочевого пузыря — это нарушение целостности стенки органа, вызванное механической травмой, воздействием химических веществ, редко – давлением мочи при некоторых заболеваниях. Проявляется болью в животе, припухлостью и синюшностью кожи над лоном, учащенными ложными позывами к мочеиспусканию, снижением или отсутствием диуреза, макрогематурией, подтеканием мочи из раневого отверстия, нарастанием симптоматики травматического шока. Диагностируется с помощью ретроградной цистографии, катетеризации, УЗИ, КТ, МРТ мочевого пузыря, общего анализа мочи, лапароскопии. В легких случаях возможно консервативное ведение с установкой катетера, при внутрибрюшинных и крупных внебрюшинных разрывах выполняется реконструктивная пластика органа.
Общие сведения
В структуре общего травматизма механические повреждения мочевого пузыря составляют от 0,4 до 15% (в России — от 1 до 7%). В последние годы отмечается более частое травмирование органа, что связано с усилением интенсивности транспортного сообщения, износом автопарка, увеличением количества тяжелых техногенных катастроф и локальных военных конфликтов.
Пик травматизации наблюдается в 21-50-летнем возрасте, около 75% пострадавших — мужчины. Особенностью травм является преимущественно сочетанный характер поражения (в 100% открытых ранений и в 85% тупых травм кроме мочевого пузыря повреждаются кости таза, позвоночник, другие органы). Актуальность своевременной диагностики и экстренных лечебных мероприятий обусловлена неблагоприятным прогнозом – в соответствии с оценочными шкалами 31,4% пострадавших относятся к категории тяжелых, 49,2% — крайне тяжелых больных, уровень смертности превышает 25%.
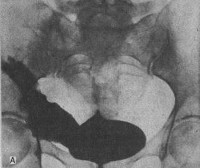
Травма мочевого пузыря
Причины
У большинства пациентов травматическое повреждение мочевого пузыря связано с воздействием на его стенку внешних механических факторов различного происхождения. В редких случаях травма обусловлена влиянием агрессивных химических веществ, инсталлированных в мочевой пузырь, или наличием заболеваний, препятствующих мочеиспусканию. Причинами травм являются:
- Дорожно-транспортные происшествия. Более чем в четверти случаев мочевой пузырь травмируется во время ДТП. Повреждение возникает при прямом ударе в проекцию органа, сильном сдавлении в транспортном средстве, ранении осколками тазовых костей, конструктивными элементами автомобиля, предметами окружающей среды.
- Ятрогенные факторы. 22-23% пациентов получают травму во время медицинских манипуляций. Стенка органа может повреждаться при его катетеризации, бужировании уретры, выполнении операций — трансуретральных вмешательств, кесарева сечения, экстирпации матки, миомэктомии, аденомэктомии, резекции толстой кишки и др.
- Бытовой и производственный травматизм. В 10% случаев повреждение происходит из-за падения с высоты на твердый предмет. При наличии предпосылок (переполнении мочой, рубцовых изменениях и др.) возможен разрыв органа из-за резкого сотрясения тела при прыжке. У 4,2% пострадавших травма возникает под действием производственных факторов.
- Насильственные действия. Целостность мочевого пузыря может нарушаться при тупых ударах в живот, ранении ножом или другими острыми предметами в драках, при криминальных абортах. В военное время в 3-4 раза увеличивается количество огнестрельных травм и открытых ранений органа осколками взрывных боеприпасов.
- Урологические заболевания. Крайне редко самопроизвольный разрыв мочевого пузыря отмечается у пациентов, которые страдают заболеваниями, нарушающими мочеиспускание, — аденомой и раком простаты, стенозом уровезикальной шейки, стриктурами уретры. Чаще урологическая патология играет роль предрасполагающего фактора, усиливая растяжение органа.
Риск возникновения наиболее тяжелых повреждений — частичных или полных разрывов — зависит не только от силы травматического воздействия, но и от места его приложения, направления, внезапности. Вероятность получения травмы существенно возрастает при алкогольном опьянении, которое способствует переполнению мочевого пузыря из-за притупления позывов к мочеиспусканию и провоцирует травмоопасное поведение. Предполагающими факторами также являются опухолевые поражения, фиброзные изменения стенки органа после перенесенных операций, лучевой терапии, воспалительных заболеваний.
Патогенез
Механизм травмы мочевого пузыря зависит от типа факторов, вызвавших повреждение. При тупом ударе в надлобковую область, противоударе о крестец, сдавлении резко повышается внутрипузырное давление, усиливается нагрузка на мочепузырную стенку. Возникновение гидродинамического эффекта способствует внутрибрюшинному разрыву органа на участке наименее развитой мускулатуры (обычно по задней стенке пузыря возле его верхушки).
Рана обычно рваная, с неровными краями. При меньшей силе механического воздействия удар вызывает закрытые повреждения (ушибы, кровоизлияния в стенку). Аналогичный патогенез характерен при наличии урологических заболеваний с нарушением пассажа мочи. Значительное смещение пузыря при механических травмах приводит к резкому натяжению поддерживающих боковых и пузырно-простатических связок с внебрюшинным разрывом мягко-эластичной стенки органа. Сильный удар способен вызвать разрыв связок, мочепузырных кровеносных сосудов, отрыв шейки.
При закрытых и открытых повреждениях везикальных оболочек острыми предметами, инструментами, осколками костей происходит поверхностное, глубокое надсечение или сквозное рассечение стенки. Рана при этом обычно линейная. Сочетание с гидродинамическим ударом при огнестрельных и оскольчатых ранениях приводит к дополнительным радиальным надрывам круглого раневого отверстия.
Классификация
Критериями систематизации травматических повреждений являются степень тяжести, возможное сообщение с окружающей средой, расположение разрыва по отношению к брюшине, сочетание с травмами других органов. Такой подход позволяет спрогнозировать течение патологического процесса и вероятные осложнения, выбрать оптимальную тактику ведения пациента. В зависимости от тяжести повреждения мочепузырной стенки травмы могут быть глухими (ушиб, поверхностное ранение наружной оболочки, надрыв слизистой) или сквозными (полный разрыв, отрыв шейки). В свою очередь, сквозные повреждения разделяют на три группы:
- Интраперитонеальные разрывы. Наблюдаются более чем у 60% пострадавших. Обычно обусловлены прямыми ударами в переполненный мочевой пузырь. Из-за истечения мочи в брюшную полость быстро осложняются перитонитом.
- Экстраперитонеальные разрывы. Возникают в 28% случаев. Чаще провоцируются избыточным натяжением поддерживающего связочного аппарата. Травмированный мочевой пузырь не сообщается с брюшной полостью, моча истекает в малый таз.
- Комбинированные разрывы. Наблюдаются у 10% пострадавших. Множественное повреждение стенки органа обычно сочетается с переломами тазовых костей. Сообщение между мочевым пузырем, брюшной и тазовой полостями обуславливает особую тяжесть патологии.
До 90% травм мирного времени являются закрытыми, благодаря сохранению целостности кожи поврежденный мочевой пузырь не сообщается с внешней средой. В военный период, при насильственных действиях с использованием холодного и огнестрельного оружия возрастает частота открытых травм, при которых нарушается целостность кожи, возникает сообщение между оболочками или полостью органа и окружающей средой. По наблюдениям специалистов в сферах травматологии и клинической урологии, сочетанные повреждения превалируют над изолированными. У 40-42% пациентов выявляются переломы костей таза, у 4-10% — разрывы кишечника, у 8-10% — травмы других внутренних органов.
Симптомы
Важная клиническая особенность данного повреждения — частое преобладание общей симптоматики над локальной. Из-за выраженного болевого синдрома и кровотечения у пострадавших нарастают признаки гемодинамических нарушений, у 20,3% наблюдается травматический шок: снижается уровень АД, ускоряется частота сердечных сокращений, кожные покровы бледнеют, покрываются липким холодным потом, возникает слабость, головокружение, оглушенность, спутанность, а затем и потеря сознания.
Из-за раздражения брюшины мочой пациенты с интраперитонеальными разрывами ощущают интенсивную боль в надлонной области, в нижней части брюшной полости, которая впоследствии распространяется на весь живот, сопровождается тошнотой, рвотой, задержкой газов и стула, напряжением брюшной мускулатуры. Специфические симптомы травмы мочепузырной стенки — боль и локальные изменения области повреждения, дизурия. При открытых ранениях на передней стенке живота, реже — в зоне промежности выявляется зияющая рана, из которой может истекать моча.
Для закрытых внебрюшинных травм характерно образование болезненной припухлости над лобком, в паху, синюшный цвет кожных покровов из-за их пропитывания кровью. Пострадавшие испытывают частые ложные позывы к мочеиспусканию со значительным уменьшением либо полным отсутствием диуреза, выделением капель крови из мочеиспускательного отверстия. При сохранении мочевыделения у пациентов с надрывами слизистой моча окрашена кровью.
Осложнения
Летальность при травматических повреждениях мочевого пузыря, особенно открытых и сочетанных, достигает 25% и более. Причинами смерти обычно являются запущенные формы перитонита, болевой, инфекционно-токсический, геморрагический шок, сепсис. Сквозные травмы стенки мочевого пузыря быстро осложняются вовлечением в процесс других органов. Анатомические особенности паравезикальной, забрюшинной клетчатки, фасциальных пространств способствуют мочевой инфильтрации, распространению затеков, образованию урогематом.
При внутрибрюшинном разрыве возникает уроасцит. Вторичное инфицирование приводит к формированию абсцессов, флегмон. У 28,3% пациентов развивается мочевой перитонит, у 8,1% — уросепсис. Восходящее распространение инфекции провоцирует начало острого пиелонефрита. В 30% случаев при сочетании травмы пузыря с повреждениями других органов наблюдается ДВС-синдром. В отдаленном периоде у больных иногда формируются мочевые свищи, наблюдается недержание мочи.
Диагностика
С учетом серьезности прогноза всем пациентам с подозрением на травму мочевого пузыря назначают комплексное обследование, позволяющее выявить разрывы мочепузырной стенки, определить их особенности и количество, обнаружить возможное повреждение смежных органов. Рекомендованными методами лабораторной и инструментальной диагностики являются:
- Общий анализ мочи. Исследование удается провести только при сохраненном мочеиспускании. Объем разовой порции зачастую уменьшен. В анализе в большом количестве присутствуют эритроциты, подтверждающие наличие кровотечения.
- УЗИ. По данным эхографии мочевого пузыря, орган обычно уменьшен в объеме, рядом с ним определяются скопления крови. Исследование дополняют УЗИ почек, при проведении которого обнаруживаются признаки постренального нарушения оттока мочи, и УЗИ брюшной полости для выявления свободной жидкости.
- Рентген. Ретроградная цистография считается «золотым стандартом» диагностики этого вида травм. Разрывы органа проявляются затеками рентгеноконтрастного вещества в пузырно-прямокишечную ямку, околопузырную клетчатку, область крыльев подвздошной кости, полость брюшины.
- Томография мочевого пузыря. С помощью КТ удаётся получить трехмерное изображение поврежденного органа, в ходе МРТ он изучается послойно. Результаты томографии позволяют точно оценить повреждения, объем урогематом, выявить сочетанные травмы.
- Диагностическая лапароскопия. Осмотр мочевого пузыря через лапароскоп дает возможность определить особенности травмированной стенки, обнаружить затеки мочи, крови. При выполнении лапароскопии визуализируются повреждения соседних органов.
Большое диагностическое значение играет катетеризация мочевого пузыря, дополненная вливанием в него жидкости (проба Зельдовича). О наличии разрывов свидетельствует отсутствие мочевыделения через катетер или поступление небольшого количества мочи с кровью. Жидкость, введенная в травмированный орган, обратно выделяется слабой струей и не в полном объеме. При интраперитонеальных разрывах возможно отхождение в 2-3 раза большего объема жидкости, что обусловлено проникновением катетера в брюшную полость и выделением ранее попавшей в нее мочи.
Экскреторную урографию назначают с осторожностью, чтобы не спровоцировать развитие контраст-индуцированной нефропатии на фоне шоковых изменений гемодинамики. Цистоскопия обычно не проводится из-за риска занесения инфекции. В общем анализе крови определяются признаки анемии — эритропения, снижение уровня гемоглобина, возможен умеренный лейкоцитоз и повышение СОЭ.
Дифференциальная диагностика проводится с повреждением заднего отдела уретры, травмами печени, селезенки, различных отделов кишечника, разрывами сосудов брыжейки. Кроме врача-уролога пациента осматривает травматолог, хирург, анестезиолог-реаниматолог, терапевт, по показаниям — проктолог, гинеколог, кардиолог, гастроэнтеролог, невропатолог, нейрохирург.
Лечение травмы мочевого пузыря
Пострадавшего срочно госпитализируют в травматологическое или урологическое отделение, переводят на строгий постельный режим. Консервативное ведение в виде катетеризации (обычно на 3-5 суток до прекращения макрогематурии) возможно только при контузии мочевого пузыря, надрывах слизистой при грубых медицинских манипуляциях, небольших экстраперитонеальных разрывах с сохраненной уровезикальной шейкой. Остальным пострадавшим показано экстренное проведение реконструктивного хирургического вмешательства с дренированием брюшной или тазовой полостей.
На этапе предоперационной подготовки назначаются гемостатические, антибактериальные, противовоспалительные, анальгезирующие препараты, средства для стабилизации гемодинамики. Объем операции зависит от особенностей повреждения. При внутрибрюшинных разрывах мочевой пузырь перед ушиванием раны экстраперитонизируют для прекращения подтекания мочи и проведения полноценной ревизии, после реконструкции поврежденного органа брюшную полость в обязательном порядке санируют.
Внебрюшинные повреждения ушивают без экстраперитонизации. Вне зависимости от типа травмы после восстановления целостности стенки мужчинам накладывают эпицистостому , женщинам устанавливают уретральный катетер. Брюшную или тазовую полость дренируют. После операции продолжают введение антибиотиков, анальгетиков, противошоковую инфузионную терапию.
Прогноз и профилактика
Нарушения целостности стенок мочевого пузыря обоснованно считаются тяжелыми, прогностически неблагоприятными травмами. Соблюдение алгоритма хирургического лечения больных обеспечивает достоверное снижение частоты осложнений даже при тяжелых повреждениях. Профилактика направлена на создание безопасных производственных условий, соблюдение правил дорожного движения, выполнение требований безопасности при занятиях травмоопасными хобби и видами спорта, отказ от злоупотребления алкоголем. Для уменьшения предпосылок к травматизму пациентам с диагностированными заболеваниями простаты, уретры, мочевого пузыря рекомендуется регулярное наблюдение и лечение у уролога.
Источник
Профилактика острой задержки мочеиспускания в раннем послеоперационном периоде у хирургических больных.
Современные научные достижения хирургии, травматологии и анестезиологии позволяют значительно расширить объем оперативных вмешательств у лиц пожилого и старческого возраста. Однако сама операционная травма, кровопотеря, анестезиологическое пособие и особенности послеоперационного периода, в первую очередь связанные с длительной иммобилизацией после таких операций, чреваты возникновением ряда осложнений, одним из которых является острая задержка мочеиспускания (ОЗМ). Послеоперационную острую задержку мочеиспускания (ПЗМ) можно охарактеризовать как внезапно возникшую невозможность самостоятельного мочеиспускания при наличии позывов к нему и наполненном мочевом пузыре в течение 6–10 ч после операции [16].
Данное осложнение встречается, по данным ряда авторов, от 2 до 60% после хирургических вмешательств [13–15, 17, 18, 20]. На развитие ОЗМ оказывают влияние многие факторы, препятствующие нормальному оттоку мочи, такие как: механическая обструкция (стриктура уретры, доброкачественная гиперплазия предстательной железы — ДГПЖ); динамическая обструкция (вследствие повышенного мышечного тонуса), нарушение иннервации стенки мочевого пузыря (возможно и как результат лекарственной терапии) и др. [12]. Нередко ОЗМ возникает после оперативных вмешательств, причем не только у больных, страдающих ДГПЖ. Механизм ПЗМ связывают со снижением внутрипузырного давления на 20–40% в горизонтальном положении; с выключением из акта мочеиспускания мышц передней брюшной стенки; с рефлекторным воздействием перенесенной операции на сократительную способность мочевого пузыря; с отрицательным влиянием общей, эпидуральной, спинно-мозговой анестезии и лекарственных препаратов (миорелаксантов, наркотических анальгетиков). Особенно часто ОЗМ наблюдается после проктологических операций. Причинами этого являются денервация мочевого пузыря во время мобилизации прямой кишки, нарушение нормального анатомического расположения мочевого пузыря с его смещением кзади, кровоизлияния в стенку мочевого пузыря. В. И. Кныш и соавторы провели исследование частоты и причин развития атонии мочевого пузыря после радикальных операций по поводу рака прямой кишки. По мнению авторов, причиной атонии мочевого пузыря после подобных операций служит его прогрессирующая дисфункция в результате нарушения парасимпатической иннервации и развития посттравматического перицистита. Частота возникновения послеоперационной ОЗМ у подобных пациентов зависит от объема оперативного вмешательства и является достоверно более высокой после наиболее травматичной операции — брюшно-промежностной экстирпации прямой кишки [7].
По данным W. E. Varger [19], после операций по поводу рака прямой кишки ишурия возникает в 13–32% наблюдений. З. С. Вайнберг [3, 11] наблюдал ОЗМ у 44,5% больных после операций по поводу геморроя, полипов и трещин прямой кишки.
Больные с повреждениями опорно-двигательного аппарата занимают одно из ведущих мест по численности среди поступивших в стационар в экстренном порядке. Длительная иммобилизация у таких больных ведет к венозному застою в органах малого таза и отеку предстательной железы. С учетом того, что оперативные вмешательства на нижних конечностях производятся преимущественно под эпидуральной или спинальной анестезией, риск развития ОЗМ в раннем послеоперационном периоде крайне высок, что обусловлено блокадой афферентных и эфферентных парасимпатических сигналов, проходящих по корешкам спинного мозга и приводящих к динамической обструкции нижних мочевых путей. Также возникают нарушения в сердечно-сосудистой и дыхательной системах, выражающиеся в повышении артериального давления, нарушениях ритма сердца, ограничении экскурсий диафрагмы и снижении глубины дыхания. Переполнение мочевого пузыря способствует нарушению функции поджелудочной железы и печени, развитию пареза кишечника [4].
Основным лечебным мероприятием, применяющимся для разрешения ПЗМ, считается катетеризация мочевого пузыря — быстрый и эффективный способ эвакуации мочи из мочевого пузыря. Интермиттирующая катетеризация позволяет ликвидировать ПЗМ без выполнения оперативного вмешательства у 23% больных с ДГПЖ. Эффективность катетеризации ниже у больных старше 75 лет, при емкости мочевого пузыря свыше 1000 мл и при внутрипузырном давлении менее 35 см вод. ст. [12].
Однако даже однократная катетеризация мочевого пузыря, а тем более длительное дренирование катетером приводит к инфицированию мочевыводящих путей, проявляющемуся от ассимптоматической бактериурии до уросепсиса с высокой степенью летальности [5]. При ишурии нарушается опорожнение не только нижних, но и верхних мочевыводящих путей, что грозит развитием острого гнойно-воспалительного процесса. Часто ишурии сопутствует пузырно-мочеточниковый рефлюкс (17%), и это повышает опасность возникновения острого пиелонефрита. Снижаются почечный кровоток, клубочковая фильтрация и диурез [10]. В результате у пациентов с острой задержкой мочеиспускания может возникнуть почечная недостаточность [1, 2, 6, 8].
Одним из основных подходов в профилактике послеоперационной задержки мочеиспускания у данной категории пациентов является назначение α-адреноблокаторов, которые блокируют действие катехоламинов на α1-адренорецепторы нижних отделов мочевыводящих путей, приводят к расслаблению гладких мышц шейки мочевого пузыря, простатического отдела уретры, стромальной части простаты, тем самым улучшая максимальную скорость потока мочи и уменьшая остаточный объем мочи. Кроме того, α1-адреноблокаторы воздействуют и на детрузор, улучшая кровоток в его стенке и снижая явления гипоксии [9].
Профилактический прием α1-адреноблокаторов в пред- и послеоперационный период приводит к снижению частоты развития ПЗМ, ускорению восстановления адекватного мочеиспускания и предупреждению инфекционно-воспалительных осложнений со стороны мочеполовой системы. Кроме того, под воздействием боли и стресса, которые пациент испытывает при операции, повышается стимуляция симпатического отдела вегетативной нервной системы, что приводит к инфравезикальной обструкции. Последней способствует подавление рефлекса мочеиспускания после спинномозговой анестезии. Антагонисты α1-адренорецепторов могут предотвратить развитие инфравезикальной обструкции, связанной с повышением активности симпатической нервной системы, и, таким образом, уменьшить риск развития острой задержки мочеиспускания. Препарат теразозин (Сетегис) является производным хиназолина, селективным и конкурентным антагонистом α1-адренорецепторов, отвечающих за сокращение гладкой мускулатуры предстательной железы, ее капсулы, проксимального отдела уретры и основания мочевого пузыря. Данный эффект приводит к уменьшению симптомов инфравезикальной обструкции. Кроме того, отличительной особенностью теразозина является его гипотензивный эффект в дозе 5 мг, вследствие снижения периферического сопротивления за счет блокады α1-адренорецепторов.
В урологической клинике РУДН на базе ГКБ № 29 г. Москвы в течение 2004–2006 гг. проведено исследование по оценке эффективности применения α1-адреноблокатора теразозина (Сетегиса) в дозировке 5 мг в качестве средства профилактики нарушений мочеиспускания в раннем послеоперационном периоде у больных с повреждениями опорно-двигательного аппарата и у больных с патологией прямой и толстой кишки и сопутствующей ДГПЖ.
Открытое сравнительное исследование проведено на 86 пациентах, поступивших в травматологическое отделение больницы по поводу травм опорно-двигательного аппарата и 66 пациентах колопроктологического отделения с соответствующей патологией и сопутствующей ДГПЖ, которым планировалось оперативное лечение. Из группы исследования исключены пациенты, которым производились операции на мочевом пузыре, простате, уретре, принимавшие α1-адреноблокаторы в анамнезе, а также пациенты с инфекцией мочевыводящих путей.
По возрасту распределение пациентов было следующим: в основной группе количество пациентов от 50 до 59 лет составило 22 человека (27%), от 60 до 69 лет — 36 (44%), от 70 до 79 лет — 24 человека (29%). В контрольной группе распределение по возрасту было следующим — от 50 до 59 лет — 24 больных (34%), от 60 до 69 лет — 27 человек (39%) и от 70 до 79 лет 19 (27%) человек.
Диагноз ДГПЖ устанавливался на основании жалоб, пальцевого ректального исследования, шкалы IPSS, УЗИ почек и мочевого пузыря с определением количества остаточной мочи, ТРУЗИ с определением объема предстательной железы и данных урофлоуметрии. По результатам ТРУЗИ распределение пациентов по объему предстательной железы в основной и контрольной группах было следующим (табл. 1).
У 61 пациента основной (74 %) и 51 пациента (73%) контрольной группы имела место гипертоническая болезнь с уровнем артериального давления от 140/90 до 180/100 мм рт. ст., получавших до поступления в стационар гипотензивную терапию.
Оперативному лечению, проводившемуся под спинальной или эпидуральной анестезией, были подвергнуты все 152 пациента.
Пациенты с травматологической патологией были распределены следующим образом. Основную группу составили 47 пациентов, из которых 22 (47 %) имели перелом шейки бедра (из них у 15 (32%) произведен остеосинтез шейки бедренной кости, у 7 (15%) — эндопротезирование шейки бедренной кости), у 14 (30%) — перелом костей голени с последующим проведением остеосинтеза костей голени, у 11 (23%) — перелом бедра (с проведением остеосинтеза бедренной кости). Всем пациентам проводилось скелетное вытяжение или иммобилизация в предоперационном периоде. Все пациенты этой группы в течение 5 сут перед и 10 сут после операции принимали препарат теразозин (Сетегис) в дозе 5 мг однократно на ночь.
Контрольную группу составили 39 пациентов: у 13 (33%) произведен остеосинтез шейки бедренной кости, у 6 (15%) — эндопротезирование шейки бедренной кости, у 11 (28%) — остеосинтез лодыжки, у 9 (24%) — остеосинтез бедренной кости.
Результаты обследования пациентов показали, что в группе больных, получавших в течение 5 сут перед операцией и 10 сут после операции препарат Сетегис в дозе 5 мг не отмечалось нарушений акта мочеиспускания в раннем послеоперационном периоде. У одного пациента, страдающего ДГПЖ, развилась задержка мочеиспускания, которая разрешилась однократной катетеризацией мочевого пузыря. В то же время из 39 пациентов контрольной группы, не получавших препарат Сетегис в пред- и послеоперационном периодах, у 6 (15%) пациентов ранний послеоперационный период осложнился ОЗМ, что потребовало дренирования мочевого пузыря уретральным катетером в течение 5 сут на фоне приема Сетегиса и антибактериальной терапии, после чего у них восстановилось самостоятельное мочеиспускание. Двум пациентам (5%) произведена троакарная цистостомия в связи с отсутствием самостоятельного мочеиспускания после удаления катетера. Результаты исследования показали, что при контрольном измерении объема остаточной мочи у больных основной группы отмечалось его достоверное снижение после окончания приема Сетегиса, по сравнению с контрольной (табл. 2).
Результаты оценки состояния больного с ДГПЖ по международной шкале симптомов (IPSS) до начала исследования показали, что средний балл у обследуемых пациентов составил 22,1. Через 2 нед приема препарата теразозин (Сетегис) у пациентов основной группы он снизился до 16,3, тогда как в контрольной группе составлял 21,6.
Пациенты с колопроктологической патологией были распределены следующим образом. Основную группу составили 35 пациентов, контрольную группу — 31 пациент (табл. 3). Возраст пациентов в среднем составил 65 лет.
Результаты обследования 79 пациентов с колопроктологическими заболеваниями и сопутствующей ДГПЖ представлены в табл. 4.
Оперативному лечению были подвергнуты все 66 пациентов. 21 пациенту (32%) была произведена геморроидэктомия, 16 (24%) — иссечение трещины и дозированная задняя сфинктеротомия, 4 (6%) — брюшно-промежностная экстирпация прямой кишки с сигмостомией, 6 (9%) — брюшно-анальная резекция прямой кишки, 5 (8%) — электрорезекция опухоли прямой кишки, 8 (12%) — передняя резекция сигмовидной кишки, 6 (9%) — резекция сигмы и анастомоз. Операции по поводу геморроя и анальных трещин осуществлялись под внутривенной анестезией, операции на прямой и сигмовидной кишке — под комбинированным обезболиванием — эпидуральной и внутривенной анестезией.
Результаты обследования пациентов показали, что в группе, получавших в течение 5 сут перед операцией и 10 сут после операции Сетегис в дозе 5 мг, не отмечалось нарушений акта мочеиспускания в раннем послеоперационном периоде. В то же время из 31 пациента контрольной группы, не получавших препарат в пред- и послеоперационном периодах и перенесших операции на прямой и сигмовидной кишке, у 4 (13%) в раннем послеоперационном периоде отмечалась острая задержка мочеиспускания, которая потребовала катетеризации мочевого пузыря в течение 4 сут. При этом 1 пациенту, в связи с невосстановившимся самостоятельным мочеиспусканием, была произведена троакарная цистостомия.
Назначение препарата Сетегис привело к снижению суммарной оценки IPSS на 29% к уменьшению количества остаточной мочи на 41% и к увеличению максимальной скорости потока мочи на 57%.
При анализе динамики артериального давления у всех исследуемых пациентов нами отмечено, что у пациентов основной группы страдающих гипертонией, на фоне приема препарата Сетегис в дозе 5 мг отмечалось минимальное, статистически значимое снижение систалического/диастолического давления, в среднем на 5,4/3,3 мм рт. рт., тогда как у пациентов контрольной группы, страдающих гипертонией, достоверного снижения артериального давления отмечено не было. Частота сердечных сокращений не менялась в обеих группах.
Заключение
Назначение препарата Сетегис 5 мг пациентам с повреждениями опорно-двигательного аппарата и патологией прямой и толстой кишки в течение 5 сут перед и 10 сут после операции в дозировке 5 мг однократно является не только эффективным и обоснованным, так как на фоне приема препарата достоверно уменьшаются динамические и ирритативные симпотомы заболевания предстательной железы, но и экономически целесообразным.
Профилактический прием α1-адреноблокаторов в пред- и послеоперационном периоде больными с повреждениями опорно-двигательного аппарата и патологией прямой и толстой кишки предотвращает развитие нарушений мочеиспускания вплоть до развития острой задержки мочеиспускания в раннем послеоперационном периоде, в связи с чем не требуется катетеризация мочевого пузыря и, как следствие, предотвращается инфицирование мочевых путей, а следовательно, сокращаются сроки пребывания в стационаре.
Кроме того, препарат теразозин (Сетегис) является препаратом выбора среди α1-адреноблокаторов при лечении больных ДГПЖ с сопутствующей гипертонической болезнью, так как обладает небольшим гипотензивным эффектом у этой категории пациентов.
Учитывая полученные нами результаты при обследовании пациентов с повреждениями опорно-двигательного аппарата и паталогиями прямой и толстой кишки в пред- и послеоперационном периоде, можно предположить, что аналогичный эффект будет получен у больных, страдающих ДГПЖ, в пред- и послеоперационном периоде с другой хирургической паталогией.
По вопросам литературы обращайтесь в редакцию.
В. П. Авдошин, доктор медицинских наук, профессор
М. И. Андрюхин, кандидат медицинских наук, доцент
С. А. Пульбере
РУДН, Москва
Источник