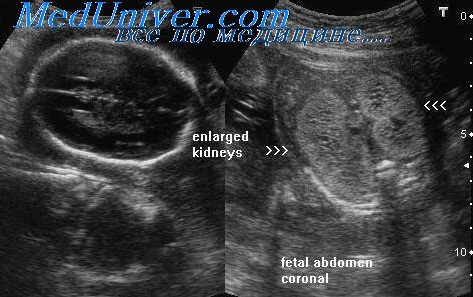
Впр плода мочевой пузырь
Содержание статьи
Врожденные пороки развития мочевого пузыря
Агенезия мочевого пузыря встречается исключительно редко и, как правило, сочетается с другими множественными пороками. Возникает вследствие недостаточного развития клоаки или аллантопса. Летальный порок. Из 37 описанных в литературе случаев только 8 отмечено у живых лиц (7 женщин и 1 мужчина), при этом имелись уретровагинальные и уретропрямокишечные свищи Нередко сочетается с атрезией прямой кишки и влагалища, и отсутствием уретры. ТТП — до 57-го дня. Удвоение мочевого пузыря — редкая аномалия. Может быть полным, частичным или с сагиттальными и поперечными перегородками в пузыре. Описаны трех- и даже пятилопастные пузыри. Патогенез этой группы пороков объясняется неправильным развитием аллантоиса и формированием патологической складки клоаки. При полном удвоений имеются две уретры. Каждый пузырь имеет по одному мочеточнику, мышечный слой, общую серозную оболочку и располагается (в тазе. Тазовая аномалия совместима с нормальной функцией, но почти всегда сочетается с другими тяжелыми пороками. В половине описан и ректовагинальными свищами. Часты сочетающиеся обструктивные аномалии мочевой системы. Неполное удвоение — два пузыря имеют одно основание и общую уретру. Изредка сочетается с пороками кишечника. Полная сагиттальная или поперечная перегородка — дупликатура стенки мочевого пузыря без серозной оболочки, разделяющая пузырь на верхнюю н нижнюю половины (форма песочных часов). При этом наблюдается одна обструктнвная половина. Если в последнюю впадает мочеточник, то развивается уретерогидроиефроз или соответствующая почка диспластична и не функционирует. Расширенная вторая половина может привести к застою мочи в мочеточниках, развитию пиелонефрита, гидронефроза и почечной недостаточности. При неполной сагиттальной перегородке нет обструкции, но часты тяжелые сочетающиеся пороки.
Лечение хирургическое.
Дивертикулы мочевого пузыря — слепо заканчивающиеся выпячивания стенки. Бывают одиночными и множественными. Локализуются в области мочепузырного треугольника, вблизи устьев мочеточников, которые могут открываться в просвет дивертикула. Стенка дивертикула состоит из тех же слоев, что и пузырь, мышечный слой гипоплазирован. Патогенез объясняют врожденной неполноценностью мышечного слоя. Клинически проявляются лишь в случаях присоединения инфекции, образования камней или опухоли, в том числе и злокачественной. Чаще встречаются у лиц мужского пола. Маленькие, бессимптомные дивертикулы обычно ие требуют лечения, более крупные подлежат иссечению. Экстрофия (эктроння) мочевого пузыря — врожденная расщелина пузыря и брюшной стенки. Задняя стенка пузыря, покрытая красной бархатистой слизистой, выпячивается через дефект брюшных мышц наружу. Устья мочеточников зияют. В основе порока лежит эмбриональное нарушение роста мезодермы. Частота 1 случай на 40 000 — 50 000 новорожденных, в 3 раза чаще у мужчин.
Экстрофия мочевого пузыря — часть группы пороков, вовлекающих мочеполовой тракт, мышечно-скелетную систему, а иногда и тонкую кишку. Классическая экстрофия составляет 60% пороков этой группы, в 10% — встречаются экстрофия клоаки, верхняя расщелина пузыря, псевдоэкстрофия, экстрофия с удвоением. В 30% — наблюдается эписпадия . Обычно сочетается со значительным расхождением лонных костей, у женщин с расщеплением клитора, эписпадией, стенозом выходного отверстия влагалища, которое смещено кпереди, может встречаться удвоение маткн. У мальчиков часты двусторонние паховые грыжи, крипторхизм, эписпадия. В 20% случаев сопровождается выпадением прямой кишки. Верхние мочевые пути и почки обычно имеют нормальное строение, но с течением времени нередко развивается уретерогидронефроз. Известны семейные формы.
Лечение хирургическое,
Мегацистис (мегатреугольннк, гипертрофия мочепузырного треугольника) -большой мочевой пузырь (объем от 500 мл и более) без обструкции. Патогенез неизвестен. Устья мочеточников в 2 раза шире по сравнению с диаметром нормальных отверстий. Стенка пузыря и треугольник гипертрофированы. Клинически выявляется у детей старше 3 лет, всегда сопровождается нарушением оттока из пузыря и наличием остаточной мочи, что способствует восходящей инфекции. Если консервативное лечение не дает эффекта, то показано оперативное, особенно, при развитии пузырно-мочеточниковых патологических рефлюксов. Необходимо дифференцировать с врожденной атонией мочевого пузыря, которая также характеризуется большой емкостью пузыря, но мочепузырный треугольник и отверстия мочеточников обычных размеров, стенка пузыря истончена. Атония — следствие обструкции в области шейки мочевого пузыря: или уретры. Мегацистимегалоуретер синдром — сочетание мегацистиса с мегалоуретером. Может быть изолированным пороком или сочетается с пороками других систем, является компонентом аномалада. Постоянно-сопровождается возникновением патологических рефлюксов, восходящей инфекцией, развитием уретерогидронефроза и почечной недостаточностью. Около 50% детей умирают в течение первых 2 лет жизни. Этиология и патогенез не выяснены. Высказываются предположения о врожденной дисплазии мышечной стенки пузыря и мочеточника, а в случаях сочетания с синдромом «сливового живота» и мышц передней брюшиой стенки.
Лечение хирургическое.
Контрактура шейки мочевого пузыря. Патогенез неизвестен. Гистологически обнаруживается избыточное развитие соединительной ткани в подслизистом слое без воспалительных изменений. Чаще встречается у мальчиков. В 70% диагностируется в школьном возрасте. Основной клинический симптом — задержка мочи, способствующая инфицированию верхних мочевых путей.
Лечение хирургическое.
Персистироваиие (незаращение) — открытый проток аллантоиса. Патогенез объясняется недостаточной облитерацией урахуса. Наблюдается в следующих вариантах:
- незаращение урахуса на всем протяжении от пупка до пузыря с мочевым свищом, открывающимся в пупке,
- урахус облитерируется только в пупочном сегменте и может существовать долго без клинических проявлений,
- частичное незаращение урахуса с облитерацией концов и открытой средней частью (кнста урахуса).
Содержимое кист — серозная или серозно-кровянистая жидкость, стенки представлены соединительной тканью с примесью гладкомышечных клеток, выстланы переходным эпителием. Большие кисты выстланы уплощенным эпителием, мышечных клеток не содержат. Полное персистирование урахуса описано у 18-летней женщины. В 1883 г. Tail описал впервые кисты урахуса. Частота перснстирования урахуса среди детских аутопсий 1 случай на 7610, кист урахуса — 1 случай на 5000, ТТП — до 6-го месяца. Урахус обычно закрывается на 4-5-м месяце эмбриональной жизни.
Лечение полного иезаращения урахуса хирургическое в первые дин или месяцы жизни, неполного — начиная с 1-го года жизни.
Источник
номалии мочеполовой системы плода. УЗИ почек плода
Аномалии мочеполовой системы плода. УЗИ почек плодаПочки плода начинают развиваться в области таза из мезенхимы метанефроса и мочеточниковых зачатков приблизительно в 7 нед беременности. Из метанефрогенной ткани формируются нефроны почек, а из мочеточниковых зачатков — собирательные трубочки, почечные чашечки и лоханки, а также мочеточники. В сроки 7-11 нед, по мере увеличения размеров плода, почки поднимаются на свое постоянное место в поясничной области за счет быстрого роста каудальной части эмбриона. В начале почки состоят из нескольких, свободно распологающихся друг относительно друга долей, которые имеют тонкий корковый слой. В течение второго триместра доли сливаются, переставая быть разобщенными, корковый слой утолщается, но дольчатый контур почек продолжает сохраняться в течение нескольких лет после рождения.
Ко второму триместру беременности функция почек становятся основным фактором, влияющим на объем околоплодных вод. Их достаточный объем необходим для нормального развития легких и скелета плода, поскольку обеспечивает пространство для его роста и двигательной активности. Таким образом, функционирование мочевой системы является необходимым условием для нормального развития легких и костной системы плода. Трансвагинальное ультразвуковое исследование позволяет визуализировать почки плода в некоторых случаях уже в 9 нед беременности, и они всегда должны обнаруживаться при этом доступе в 13 нед. Трансабдоминальное сканирование обеспечивает визуализацию почек в некоторых случаях в 13-14 нед, и в большинстве случаев — 16-18 нед. Ряд факторов, таких как избыточная масса тела у беременной или миома матки больших размеров, могут затруднять оценку почек при эхографии. Аномалии мочеполовой системы составляют около четверти всех врожденных пороков развития, при этом частота их распространенности при рождении составляет 0,2-0,6%. Аномалии мочеполового тракта возникают вследствие остановки развития на раннем этапе, аномалий развития почечных канальцев, нарушения процессов смещения почек в поясничную область, а также вследствие обструкции мочевыводящих путей или устья мочевого пузыря. Чаще всего такие пороки имеют изолированный характер, но могут сочетаться с другими аномалиями развития плода или вызывать их. Сочетания мальформаций мочеполовой системы и других систем плода обнаруживается при широком спектре различных наследственных, в том числе связанных с хромосомными нарушениями, и спорадических синдромов. Кроме того, обструкции мочевыводящих путей, при которых уменьшается количество выделяемой мочи, приводят к маловодию и вследствие этого обусловливают деформации других частей тела плода. В частности, выраженное маловодие, которе возникает до 20 нед беременности, может вызвать гипоплазию легких, лицевые аномалии, в том числе приплюснутый нос, низкое расположение ушных раковин, косолапость и другие деформации конечностей. Ультразвуковое исследование во втором и третьем триместрах беременности позволяет выявлять не менее 80-85% аномалий мочеполовой системы, что делает возможным проведение дородового консультирования будущих родителей и обеспечивает своевременное обследование и лечение сразу после родов. До появления эхографии именно запаздывание с лечением приводило к значительному нарушению функции почек или даже к ее полной потере. — Также рекомендуем «Агенезия почек плода. Эктопия почек плода» Оглавление темы «Патология почек плода»: |
Источник
Экстрофия мочевого пузыря
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Введение
Экстрофия мочевого пузыря (ЭМП) — редкий тяжелый врожденный порок развития нижних мочевых путей, характеризующийся отсутствием передней брюшной стенки и передней стенки мочевого пузыря, а также расхождением лонного сочленения (диастаз). Через дефект передней брюшной стенки пролабирует слизистая оболочка. В нижней части обнаженной слизистой оболочки расположены устья мочеточников, из которых постоянно выделяется моча. Пуповина впадает низко в верхний край дефекта передней брюшной стенки.
Экстрофийные пороки нижних мочевых путей делят на классическую экстрофию мочевого пузыря и экстрофию клоаки. У мальчиков экстрофия мочевого пузыря сочетается с расщеплением мочеиспускательного канала (эписпадия). Экстрофия мочевого пузыря у девочек сопровождается расщеплением клитора, расщеплением или отсутствием мочеиспускательного канала, а также спайками больших и малых половых губ [1, 2].
В литературе экстрофия мочевого пузыря чаще всего описывается в комплексе с эписпадией, хотя имеются сообщения об изолированном поражении стенки мочевого пузыря, когда его шейка и мочеиспускательный канал сформированы. Такая патология называется неполной экстрофией, или переднепузырным свищом. При неполной экстрофии патология половых органов отсутствует [3, 4]. Наиболее тяжелой и редкой формой порока является экстрофия клоаки, при которой расщепление распространяется не только на урогенитальную область, но и на терминальный отдел кишечника [5, 6].
Впервые экстрофию мочевого пузыря, как врожденный порок развития, описал Schenk von Grafenberg в 1597 г. В 1780 г. Chaussier впервые использовал термин «экстрофия». Упоминания об экстрофии мочевого пузыря обнаружены на ассирийских табличках, сделанных 2000 лет до н. э. [7]. Частота экстрофии мочевого пузыря составляет 0,25-0,5 на 10 тыс. новорожденных. Соотношение классической экстрофии мочевого пузыря у мальчиков и девочек 3:1 [1, 8]. При экстрофии мочевого пузыря встречаются сопутствующие врожденные аномалии — паховые грыжи (у 56 % мальчиков, у 15 % девочек), крипторхизм (20 %), колоректальные аномалии (1,8 %) и др. [1, 2]. Экстрофия мочевого пузыря может входить в состав комплекса OEIS (omphalocele, extrophy, imperforate anus, spinal defects), OMIM 258040.
Пренатальная диагностика экстрофии мочевого пузыря возможна уже при первом скрининговом обследовании в 11-14 нед беременности, когда в норме полость мочевого пузыря начинает наполняться мочой. Визуализация мочевого пузыря обязательно входит в стандартные протоколы исследования пренатального скрининга.
Эмбриопатогенез
Экстрофия мочевого пузыря формируется на 4-5-й неделе эмбриогенеза, когда на 28-32-й день происходит каудальная миграция мембраны клоаки. В то же время формируется передняя брюшная стенка, однако если мезенхима не переходит из одного клеточного слоя нижней брюшной стенки в другой, то это приводит к нестабильности клоакальной мембраны. Преждевременный разрыв мембраны клоаки приводит к комплексу «подпупочных» аномалий. Разрыв клоакальной мембраны после полного разделения «урогенитальной» части от пищеварительного тракта приводит к формированию классической экстрофии мочевого пузыря.
Если повреждение мембраны происходит до того, как спускается уроректальная перегородка, тогда это приводит к вывороту нижнего уретрального тракта и части пищеварительного тракта с формированием клоакальной экстрофии. Генетические факторы, связанные с экстрофией мочевого пузыря, на сегодняшний день не выявлены, однако существует гипотеза, что потеря экспрессии р63 из-за полиморфизмов очередности у промотера является фактором риска развития экстрофии мочевого пузыря [1, 9].
Ниже представлен случай диагностики экстрофии мочевого пузыря в III триместре беременности.
Материал и методы
Пациентка С.,18 лет, настоящая беременность первая, от первого брака, супруги соматически здоровы, профессиональных вредностей не имеют, наследственность не отягощена. На учете в женской консультации пациентка состояла с 9 нед беременности. Беременность протекала без осложнений. При скрининговом УЗ-исследовании в I и II триместрах по месту жительства ВПР и УЗ-маркеров хромосомных перестроек у плода не обнаружено.
При УЗ-обследовании в 34 нед беременности в женской консультации по месту жительства было обнаружено образование средней эхогенности размером 28x23x25 мм в области нижних отделов передней брюшной стенки. Женщина была направлена в медикогенетическое отделение МОНИИАГ с диагнозом: «ВПР плода, экстрофия мочевого пузыря?».
УЗ-исследование проводилось на сканере WS80A (компании Samsung Medison) с использованием объемного датчика CV1-8A.
Результаты
При УЗ-исследовании обнаружен один живой плод женского пола в головном предлежании. Гестационный срок составил 34,4 нед. Фетометрические показатели плода соответствовали данному сроку. Патологических изменений плаценты и околоплодных вод не выявлено. При исследовании мочевой пузырь в типичном месте не визуализировался.
В нижних отделах передней брюшной стенки в надлобковой области визуализировалось эхогенное образование размером 30x28x25 мм (рис. 1, 2). Определялось низкое впадение пуповины. Почки плода визуализировались в типичном месте, без структурных изменений. Патологических изменений других органов не было выявлено.
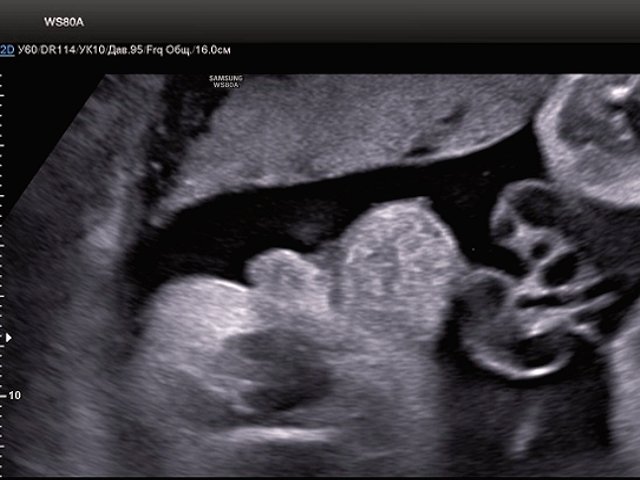
Рис. 1. Эхогенное образование в нижнем отделе передней брюшной стенки (экстрофированный мочевой пузырь).
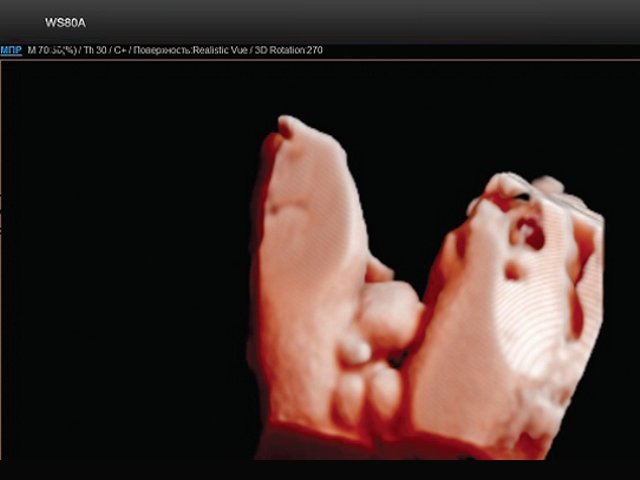
Рис. 2. Экстрофия мочевого пузыря в сочетании с отсутствием видимой патологии наружных половых органов (режим трехмерной реконструкции).
Поставлен диагноз: «Беременность 34,4 нед. ВПР плода — экстрофия мочевого пузыря».
Обсуждение
Пренатальными УЗ-признаками экстрофии мочевого пузыря являются: отсутствие визуализации мочевого пузыря при нормальном количестве околоплодных вод, структурно неизмененные почки, визуализация эхогенного образования в надлобковой области, аномалии строения половых органов. Использование ЦДК является дополнительным инструментом для диагностики экстрофии мочевого пузыря. В норме пупочные артерии проходят вдоль стенки мочевого пузыря при поперечном сканировании нижней части живота. Для экстрофии мочевого пузыря характерно низкое впадение пуповины, при котором артерии охватывают образование в надлобковой области. При отсутствии визуализации мочевого пузыря в типичном месте необходимо провести повторное сканирование через 30-40 мин для адекватной оценки его расположения и степени наполнения.
Изолированная экстрофия мочевого пузыря, как правило, не сочетается с хромосомными перестройками у плода и не требует пренатального кариотипирования.
В данном клиническом наблюдении экстрофия мочевого пузыря была диагностирована у плода женского пола, что встречается значительно реже, чем у плодов мужского пола. Кроме того, отсутствие выраженной деформации наружных половых органов позволяет предположить неполную форму экстрофии. Оценка анатомии мочевого пузыря включена в протокол обязательного скринингового обследования во всех триместрах беременности. Отсутствие визуализации мочевого пузыря в типичном месте должно насторожить врачей УЗ-диагностики. Однако часто экстрофия мочевого пузыря диагностируют лишь в III триместре беременности.
После рождения детям с экстрофией мочевого пузыря требуется многоэтапная сложная хирургическая коррекция. Процент неудовлетворительных отдаленных результатов, к сожалению, остается на сегодняшний день очень высоким, как правило, вследствие присоединения таких осложнений, как нарушение функции тазовых органов: недержание мочи, рубцовая деформация половых органов, половая дисфункция, выраженная деформация передней брюшной стенки, уретерогидронефроз III-IV степени, непрерывно рецидивирующий пиелонефрит со снижением функции почек, хроническая почечная недостаточность и др. [4, 7]. Огромной и сложной проблемой остается медико-социальная реабилитация больных с экстрофией мочевого пузыря.
Заключение
Сложности ранней диагностики связаны с невыраженными УЗ-проявлениями достаточно тяжелой патологии. Четкое соблюдение алгоритма скрининговых УЗ-исследований анатомии плода в 11-14 и 20-22 нед беременности позволяет диагностировать экстрофию мочевого пузыря. При выявлении экстрофии мочевого пузыря у плода необходимо проведение медико-генетического консультирования с оформлением пренатального консилиума. Требуется тщательное разъяснение родителям сути выявленной патологии, а также информация о частых послеоперационных отдаленных последствиях и осложнениях как физического, так и психогенного генеза.
Литература
- Лопаткин Н.А., Пугачев А.Г. Пороки развития мочевого пузыря и уретры. В кн. Детская урология. Руководство. М.: Медицина, 1986. С. 207-242.
- Gearhart J.P. Criteria for the prenatal diagnosis of classic bladder exstrophy / J.P. Gearhart, J. Ben-Chaim, R.D. Jeffs // Obstet. Gynecol. 1995. Jun. 1. V. 85. № 6. P. 961-964.
- Михельсон А.И. Оперативное лечение недержания мочи на почве врожденных аномалий мочевой системы. Минск, Госсиздат БССР. 1957.
- Осипов И.Б. Реконструктивно-пластические операции при экстрофии мочевого пузыря у детей: автореф. дисс. докт. мед. наук. СПб, 1996.
- Ахунзянов А.А. Диагностика и лечение врожденной клоаки у детей // Хирургия. 1976. № 9. С. 98-101.
- Захаров Н.Л. Дефекты передней брюшной стенки у новорожденных // Хирургия. 1986. № 6.
- Hollowell J.G., Ransley P.G. Surgical management of Incontinence in bladder exstrophy // Brit. J. Urol. 1991. V. 68. № 5. P. 543-548.
- Kockum C.C., Hansson E.E., Stenberg A.et. al. Bladder exstrophy in Sweden-a long-term follow-up study // Eur. J. Pediatr. Surg. 1996. V. 6. P. 208-211.
- Баиров Г.А., Ахметджанов И.А., Осипов И.Б. Реконструктивно-пластические операции при экстрофии мочевого пузыря у детей // Вестник хирургии. 1986. Т. 136. № 6. С. 105-108.

УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Источник