Рак мочевого пузыря радикальная цистэктомия
Содержание статьи
Радикальная цистэктомия
Основное лечение мышечно-инвазивного рака мочевого пузыря является хирургическое удаление мочевого пузыря.
Причины при которых может рекомендоваться удаление всего пузыря:
- Наличие мышечно-инвазивной опухоли
- Наличие опухоли, которая агрессивно растет, которая имеет множественные злокачественные очаги (мультифокальная) или поверхностная, но имеет рецидивы после химиотерапии или иммунотерапии
- Наличие постоянных болей и кровотечения у пациентов с неизлечимым заболеванием.
Оценить риск удаления мочевого пузыря, можно путем прохождения медицинской комиссии в составе (например, уролог, онколог, хирург, анестезиолог, терапевт).
Важны также такие факторы, как ваш биологический возраст (общесоматическое состояние, ваше самочувствие, измеряемое как состояние работоспособности или ожидаемая продолжительность жизни) и другие заболевания, которые у вас имеются (диабет, сердечные заболевания, гипертоническая болезнь и т.д.). Пациенты старше 80 лет труднее переносят такие операции и имеют более длительный восстановительный период.
Ранние операции на брюшной полости или лучевая терапия затрудняют хирургическое вмешательство, но редко являются причиной отказа от хирургического вмешательства. Избыточный вес не влияет на выживание после операции, но влияет на риск осложнений в послеоперационном периоде.
Удаление мочевого пузыря включает удаление мочевого пузыря, нижний отдел мочеточников и тазовых лимфатических узлов. В зависимости от таких факторов, как расположение опухоли и метод дальнейшего отведения мочи, часть прилежащих половых органов (простата и семенные пузырьки у мужчин, вся уретра, матка у женщин) удаляются.
Как проводится удаление мочевого пузыря?
Удаление мочевого пузыря осуществляется через разрез в брюшной полости (открытый) пациент под общей анестезией (сочетание внутривенных препаратов и ингаляционных газов). Мочевой пузырь, нижний отдел мочеточников, расположенные близко к мочевому пузырю, тазовые лимфатические узлы и (часть) прилежащих половые органы удаляются. Теперь должен быть сформирован другой метод хранения и отведения мочи.
Стандартная методика на данный момент — открытая хирургия. Тем не менее, это может быть сделано менее инвазивно (лапароскопическая или роботизированная хирургия). В настоящее время в специализированных центрах, имеющих специальное оборудование и опытных специалистов, малоинвазивные операции считаются методом выбора для удаления мочевого пузыря.
Как подготовиться к процедуре?
При поступлении в стационар врач информирует вас о том, как нужно готовиться до и что делать после операции.
Часть вашей кишки будет использоваться для создания мочевого резервуара. Врач подробно объяснит, как подготовиться к данной процедуре.
Перед операцией врач подробно проинформирует вас о том, как подготовиться к анестезии. Если вы принимаете какие-либо лекарственные препараты, сообщите об этом своему врачу. Возможно, потребуется отмена некоторых препаратов за несколько дней до операции.
В течение первых нескольких дней вы находитесь под динамическим наблюдением. Врач подробно проинформирует вас о послеоперационном периоде.
Во время госпитализации вы узнаете, как обращаться с уростомой. После того, как вы научитесь использовать и опорожнять уростому, будет установлена дата выписки.
Химиотерапия перед удалением мочевого пузыря
Химиотерапию проводят перед удалением мочевого пузыря, чтобы потенциально уменьшить опухоль и убить опухолевые клетки, которые уже проникли в кровь или лимфатические узлы.
Химиотерапию перед операцией можно рекомендовать пациентам с мышечно-инвазивной формой. Это также необходимо, при опухолях большого размера (> 3 см) или если есть признаки распространения рака на лимфатические узлы (метастазы). Решение о проведении химиотерапии принимается врачебной комиссией (включая онколога, уролога и радиолога). Необходима адекватная функция почек.
Положительная реакция на химиотерапию улучшает выживаемость, но не исключает необходимость хирургического вмешательства.
Химиотерапия после удаления мочевого пузыря
Если опухоль большая (> 3 см), не может быть полностью удалена или распространяется на лимфатические узлы (определяется патологоанатомом), показана химиотерапия после удаления мочевого пузыря. Рак, который распространился на лимфатические узлы, указывает на системное заболевание и может потребоваться системное лечение (с химиотерапией) в определенных случаях.
Отведение мочи: недержание или удержание.
Важно понять двухэтапный подход к удалению мочевого пузыря. Сначала удаляют мочевой пузырь и лимфатические узлы. Затем, мочу нужно отвести. Это может быть достигнуто несколькими способами. Вообще мы различаем варианты, которые являются недержанием (непрерывный поток мочи сразу выходит за пределы тела), и удержание (моча, хранится в организме и отводится при необходимости). Биологический возраст, функция почек и другие заболевания, качество жизни пациента имеют решающее значение при выборе тактики операции. Чтобы определиться, какой вариант лучше подходит в вашей конкретной ситуации, вы должны знать и понимать ограничения после каждого вида операции и побочные эффекты.
В дополнение к вашим личным предпочтениям важна способность физически и морально привыкнуть, и уметь обращаться с таким отведением мочи.
Перемещение мочеточников
Выведение мочеточников через кожу (уретерокутанеостомия).
Перемещая мочеточники или вместе или отдельно через кожу сбоку живота для отведения мочи от почек (стома) (рис.1), моча может просто вытекать через стому в мешок. Это отведение мочи является самым простым. Хотя он редко используется. Данный метод безопасен и доступен для пациентов, с отягощенным анамнезом (предшествующие операции, множественные проблемы со здоровьем, паллиативный уход) или у пациентов, которые не могут позаботиться о себе после операции. Основные осложнения встречаются редко, однако рецидивирующие инфекции и затягивание отверстия (стеноз) являются общими и могут потребовать лечения. Пациентам часто необходимо стентирование мочеточника, который необходимо регулярно менять.
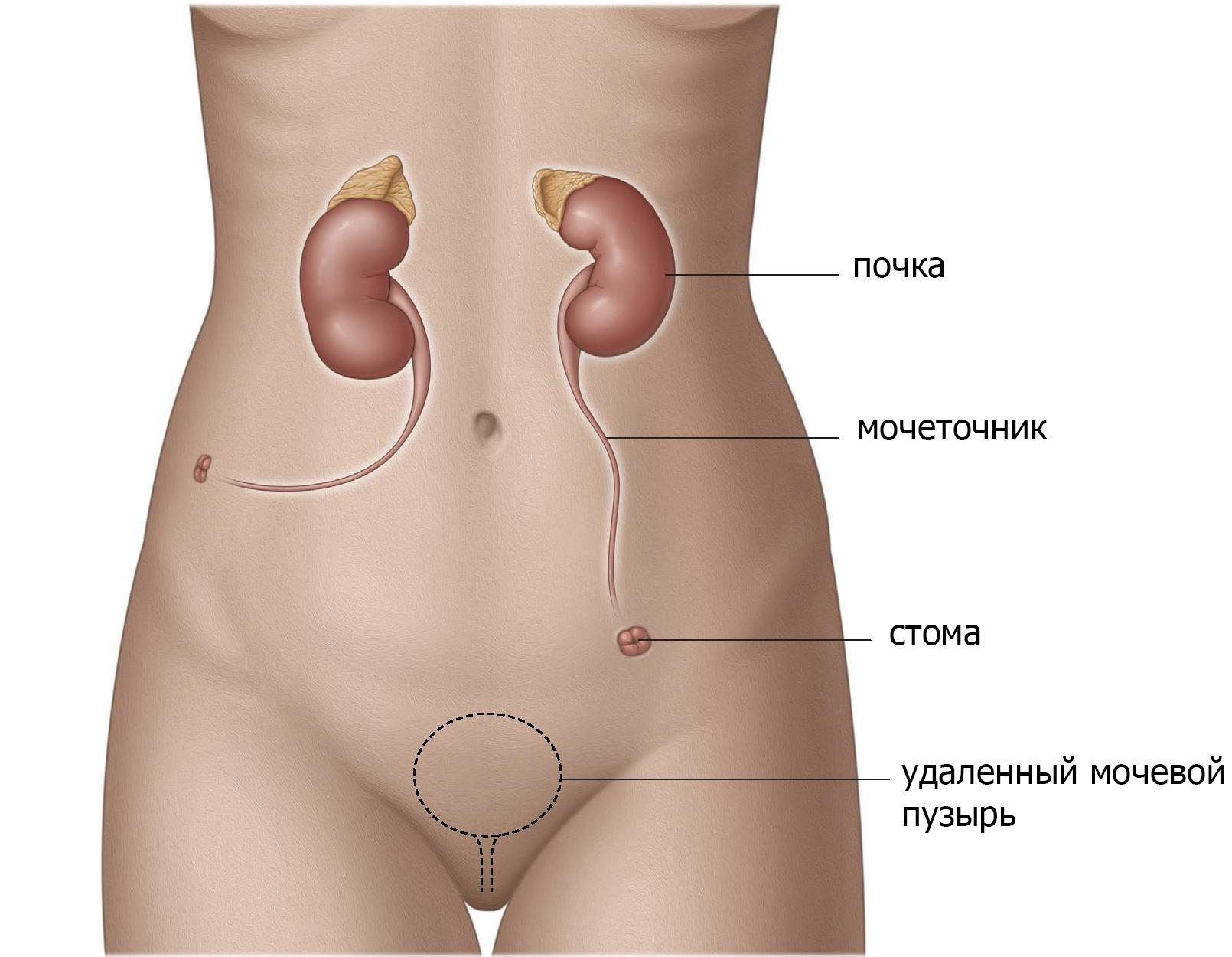
Рис. 1 уретерокутанеостома
Установить часть тонкой кишки между мочеточниками и кожей (подвздошный канал).
Подвздошный канал можно создать, поместив тонкую кишку между мочеточниками и кожей (рис.2). Эта «кишечная стома» создает большее расстояние между почками и кожей и снижает риск инфицирования. Другим преимуществом для пациентов является то, что эта стома легче обрабатывается и имеет меньше осложнений, таких как сужение выводного отверстия (стеноз). Данная операция технически относительно проста и надежна и поэтому является наиболее часто используемой.
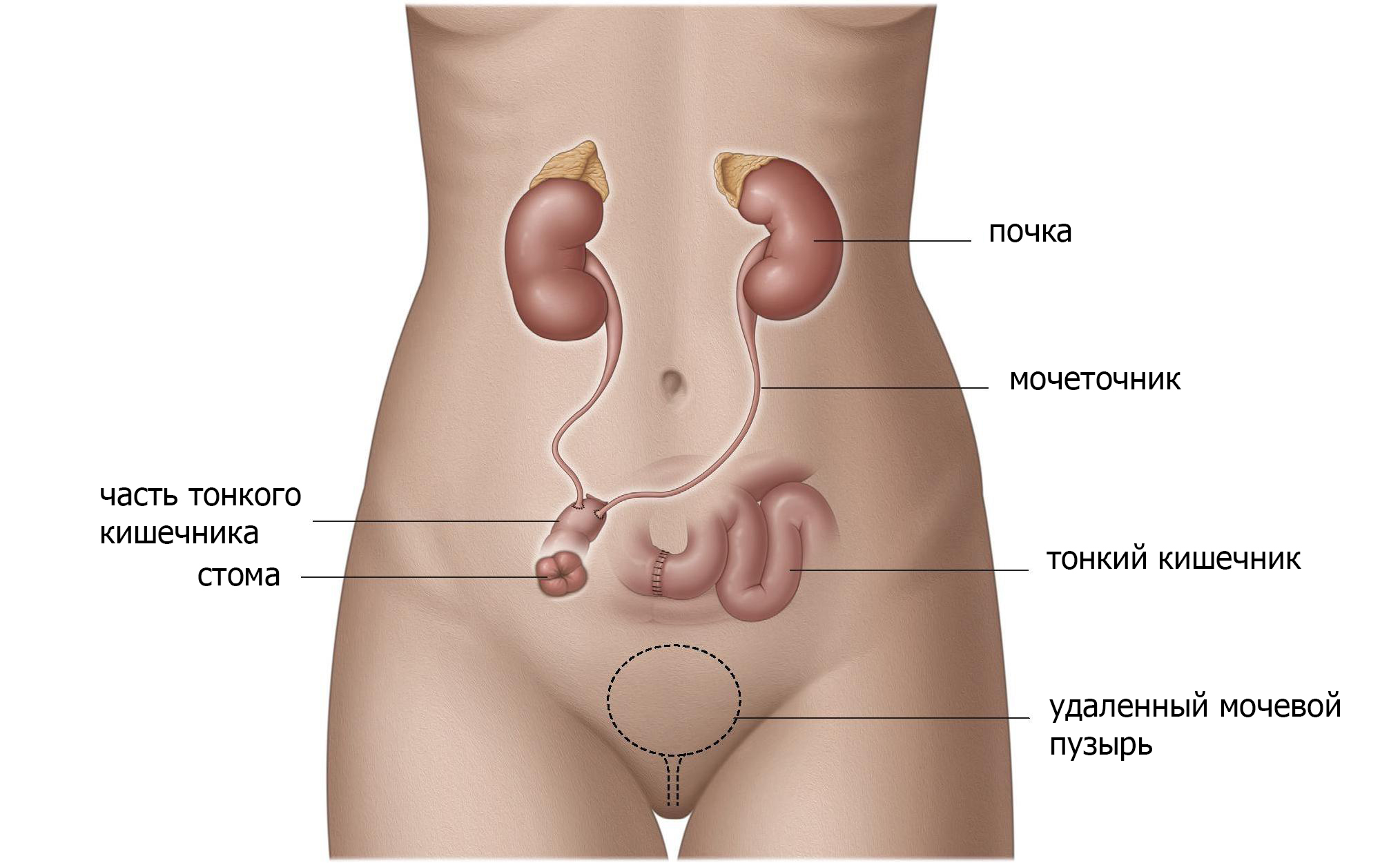
Рис. 2 Подвздошный канал
Выбирая данный вид отведения мочи, вы должны знать, что привыкнуть к жизни со стомой требует много времени и усилий.
Вновь сформированный мочевой пузырь. Создание резервуара внутри тела
Используя тонкую кишку или толстую кишку, а иногда и аппендикс, создается резервуар в брюшной полости, а затем соединяется с кожей с помощью клапанного механизма (рис. 3). С таким резервуаром низкого давления, моча может быть сохранена в теле. Цель этой процедуры — позволить контролировать опорожнение или обратный поток мочи в почки (рефлюкс). Резервуар опорожняется прерывистой катетеризацией небольшим пластиковым катетером каждые 2-6 часов. Отверстие может находиться где угодно на нижней части живота или в пупке.
Если выбран данный вид операции, вам потребуется регулярно катетеризировать и опорожнять данный резервуар. Функция печени и почек должна быть адекватной из-за реабсорбции мочевых компонентов (соли, мочевой кислоты, воды) в кишечной оболочке резервуара, что вызывает дополнительную нагрузку на эти органы.
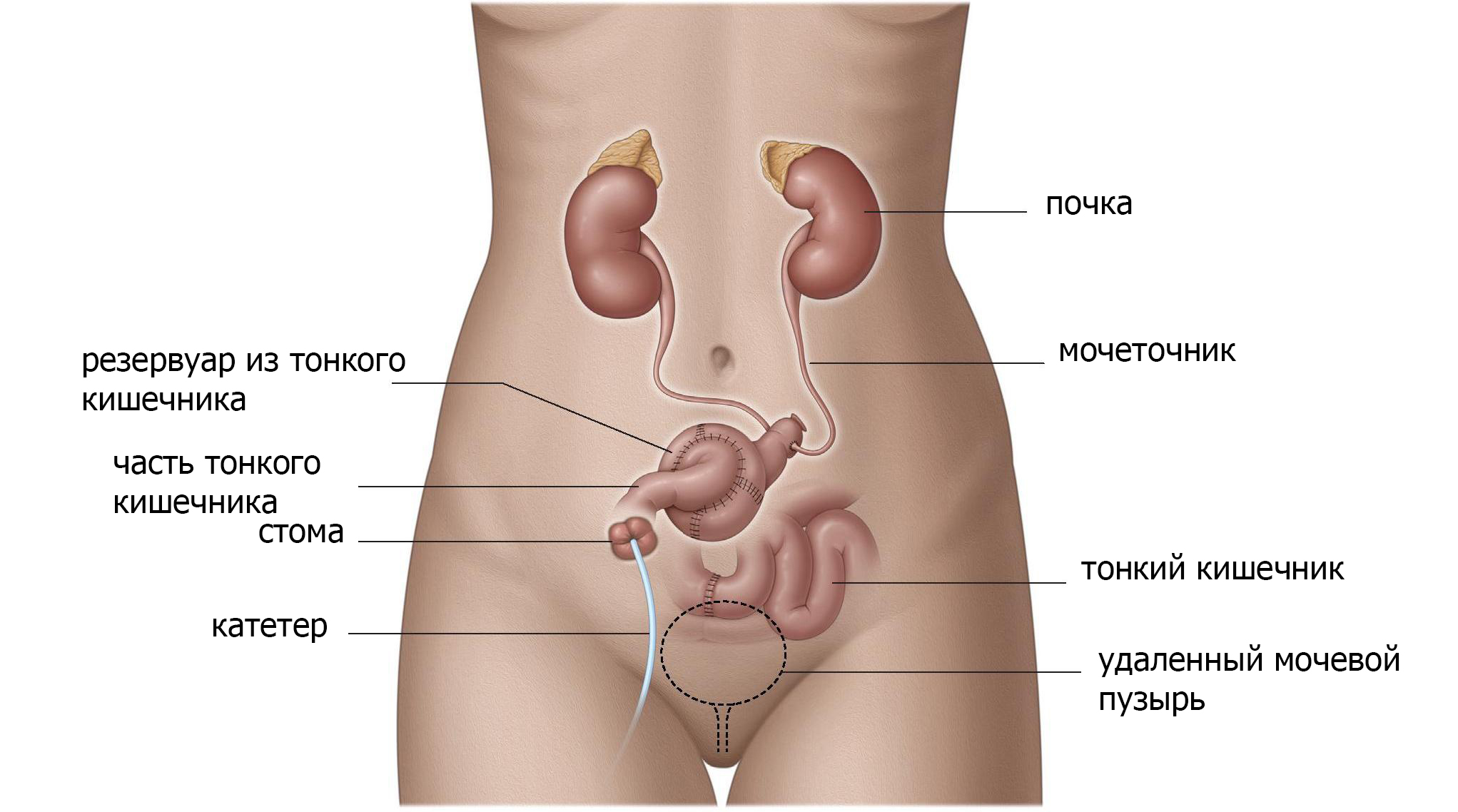
Рис. 3 Резервуар из кишечника
Осложнения включают инфекции, недержание мочи, грыжу, рефлюкс, затягивание отверстия (стеноз), а также синдром короткой кишки, метаболический и электролитный дисбаланс.
Поскольку эта операция имеет технические сложности, особенно при создание клапанного механизма, который не всегда бывает удачным, данный метод используется редко.
Имплантация мочеточников в прямую кишку (уретероректонеостомия)
Когда мочеточники имплантируют в прямую кишку, моча хранится в ампуле прямой кишки (рис.4). Анальное отверстие и тазовое дно становятся органом удерживающим мочу и должны функционировать должным образом. Данный вид отведения приводит к смешиванию фекалий с мочой, поэтому опорожнение и дефекация происходят одновременно. Этот метод имеет высокий уровень инфецирования, поэтому используется редко и только при определенных обстоятельствах. Краткосрочные осложнения включают повторяющиеся инфекции (включая воспаление брюшной стенки и почек), затягивание отверстия в прямой кишке (стеноз). Долгосрочные осложнения включают недержание мочи, раздражение кишечника и связанный с этим рак толстой кишки.
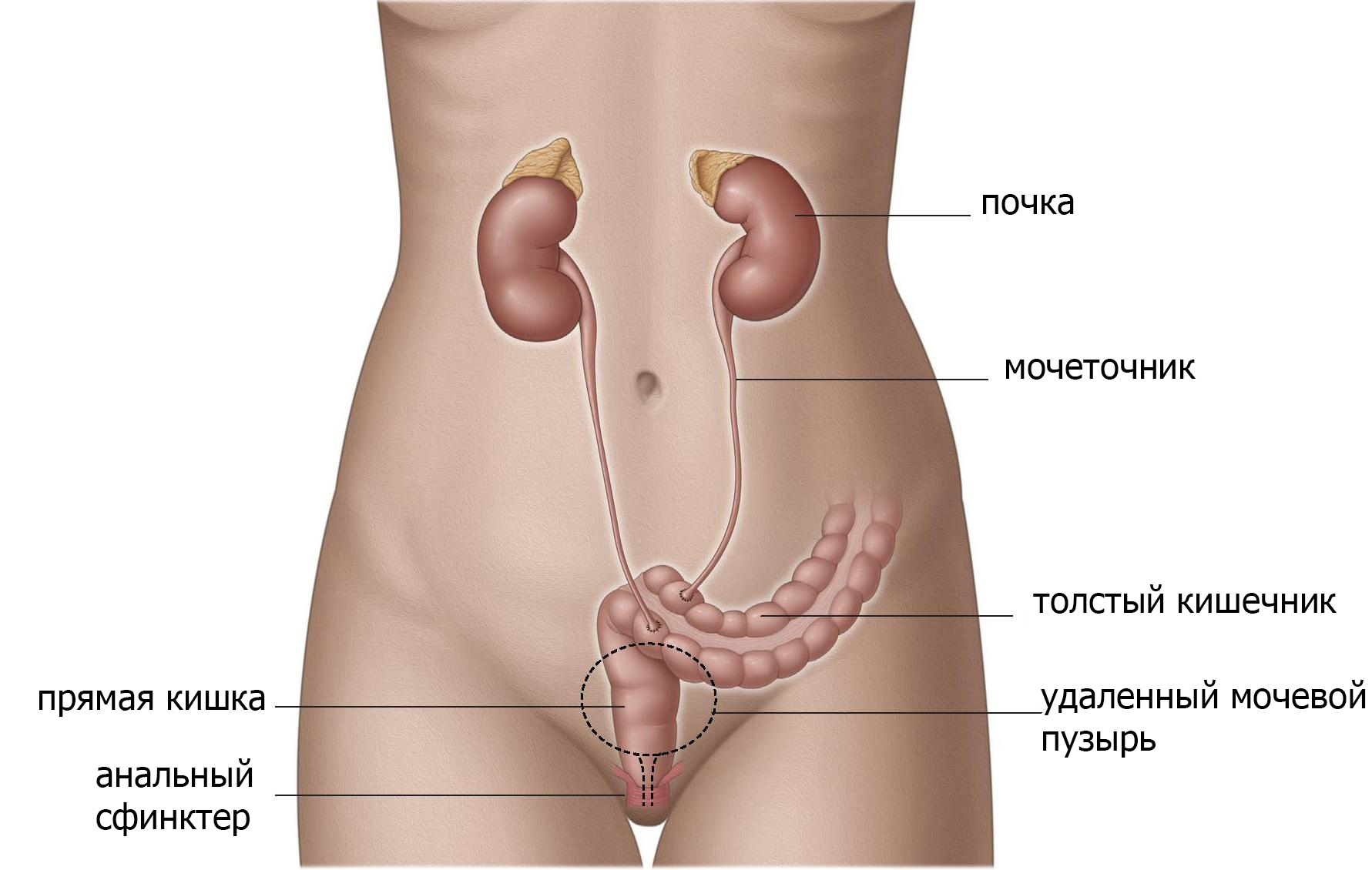
Рис. 4 Уретероректонеостома
Формирование мочевого пузыря из тонкой кишки
Новый мочевой пузырь может быть сформирован из тонкой кишки, которая изолируется от пищеварительного тракта (рис.5). Резервуар сформирован из тонкого кишечника и помещен в малый таз в качестве замены мочевого пузыря. В зависимости от используемой методики резервуар имеет сфероидальную форму, «W» или «V». Мочеточники прикреплены с обеих сторон, а нижний конец соединен с уретрой. Мочевой сфинктер сохраняется. При данный виде операции моча должна накапливаться а затем выводиться наружу как и при здоровом мочевом пузуре.
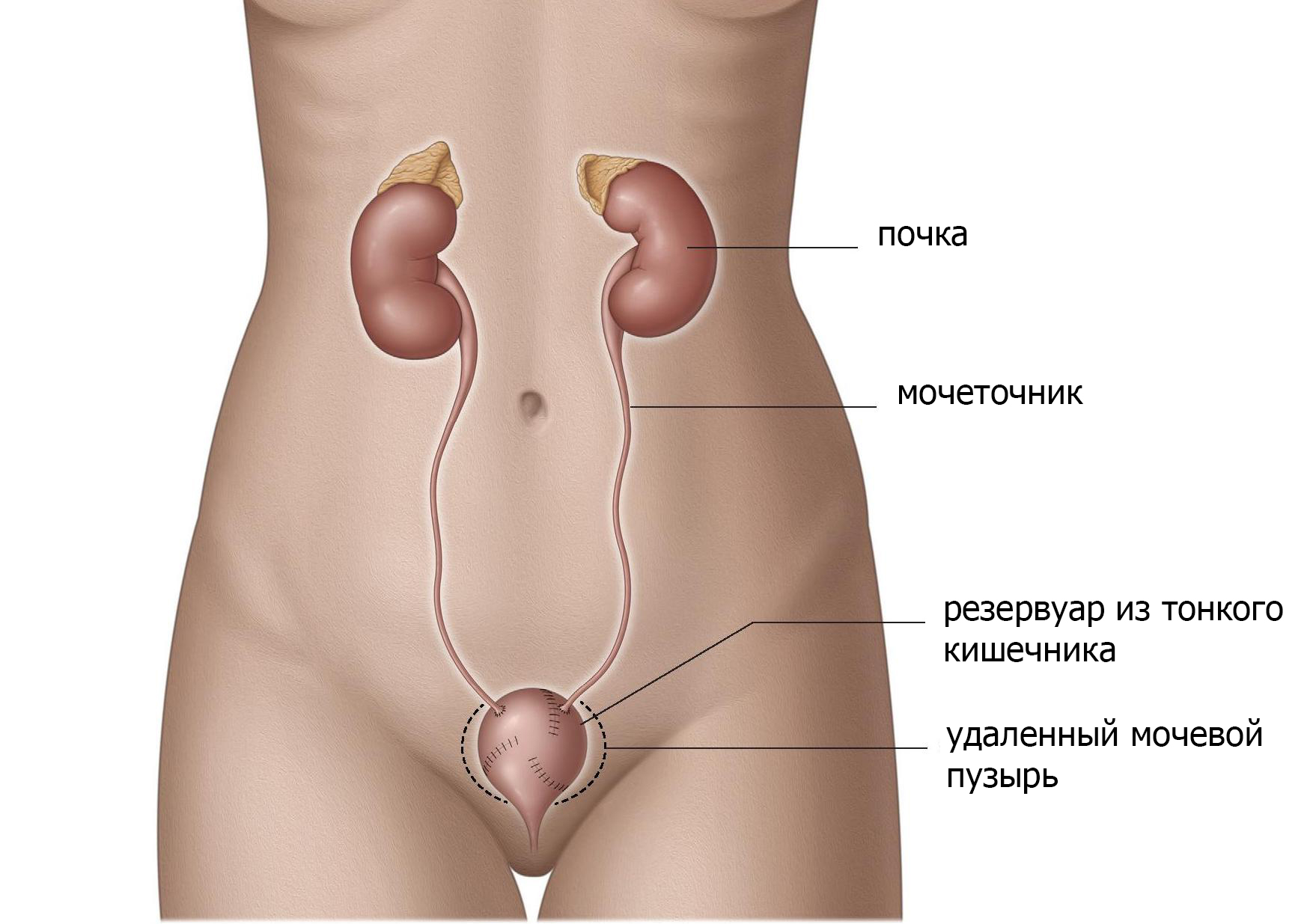
Рис. 5 мочевой пузырь из тонкой кишки
Вы не почувствуете наполнения мочевого пузыря или позыв к мочеиспусканию с пузырем из тонкого кишечника, поэтому опорожнение необходимо проводить каждые 2-4 часа. Пузырь освобождается, расслабляя мышцы тазового дна и сокращая брюшную полость (метод Вальсальвы). Нажатие на живот обеими руками может помочь для полного опорожнения. У 20% женщин необходимо выполнять периодическую самокатетеризацию для полного опорожнения, у мужчин этого не требуется.
При данном виде операции требуется удовлетворительная функция почек и печени, нормальное состояние мышц тазового дна. Осложнения после данного вмешательства включают в себя повторяющиеся инфекции (включая воспаление брюшной стенки и почек) и недержание мочи.
Долгосрочные осложнения включают затягивание отверстия в области анастамоза, изменения верхних мочевых путей, недержание мочи, синдром короткой кишки и грыжу, а также метаболический и электролитный дисбаланс.
Регулярный анализ крови поможет оценить количество мочевой кислоты которая реабсорбируется используемым участком кишечника, вызывая дисбаланс pH, который часто требует медикаментозного лечения пероральными препаратами (бикарбонат натрия — пищевая сода).
Для вновь образованного резервуара требуется время для его укрепления и начала работы. Для увеличить емкость сформированного пузыря, вам нужно будет его тренировать. Врач предоставит вам инструкции по тренировке мочевого пузыря. В начале недержание мочи может случиться из-за послеоперационного отека тазового дна.
Источник
Научный журнал
Фундаментальные исследования
ISSN 1812-7339
«Перечень» ВАК
ИФ РИНЦ = 1,441
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Лелявин К.Б. 1
1 ГБОУ ВПО «Иркутский государственный медицинский университет»
Изучены непосредственные и отдаленные результаты одномоментной радикальной цистэктомий (РЦЭ) выполненной в отделении урологии ГБУЗ «Областной онкологический диспансер» у 277 больных по поводу рака мочевого пузыря (T1-T4b). Выполнение одномоментной радикальной цистэктомии с различными методами отведения мочи обеспечивает общую — 51,6 % (медиана 16,9 мес.), скорректированную — 88,7 % (медиана 26,5 мес.), безрецидивную — 48,1 % (медиана 24,8 мес.) и безрецидивную скорректированную — 78,7 % (медиана 29,6 мес.) выживаемость больных РМП (T1-T4b). Использование для реконструкции нижних мочевых путей после РЦЭ современных пластических методик позволяет ожидать у большинства больных раком мочевого пузыря (T1-T4b) статистически значимого повышения 5-летней безрецидивной скорректированной выживаемости с 68,2 % после УКС и 75,0 % после УСС до 91,4 % после операции Bricker, до 93,8 % после Studer, до 92,3 % после Mainz pouch II, до 91,7 % после Reddy и до 100,0 % после ортотопической и гетеротопической пластики желудком по Митчеллу (p = 0,00314). Наиболее высокие показатели 5-летней выживаемости отмечаются у больных с опухолями, ограниченными мочевым пузырем, скорректированная 5-летняя выживаемость — 95,2 %. При распространении опухоли за пределы органа данный показатель снижается: при pT2a до 89,4 %, pT3a до 71,1 %, pT3b до 77,5 %, pT4a до 60,5 % и при pT4b до 75,0 % (р = 0,00004).
мышечно-инвазивный рак мочевого пузыря
радикальная цистэктомия
кишечная пластика
выживаемость
1. Красный С.А. Радикальная цистэктомия в лечении злокачественных опухолей мочевого пузыря / С.А. Красный, О.Г. Суконко, С.Л. Поляков // Онкологический журнал. 2009. — Т.3. — № 4 (12). — С. 7-15.
2. Матвеев Б.П. Клиническая онкоурология. — М.: Издательский дом «АБВ-пресс», 2011. — 934 с.
3. Петрова Г.В. Характеристика и методы расчета статистических показателей применяемых в онкологии. Практическое пособие / Г.В. Петрова, О.В. Грецова, В.В. Старинский и др. — М.: ФГУ МНИОИ им. П.А. Герцена Росздрава, 2005. — 39 с.
4. Gerharz E.W., Mansson A., Hunt S., Skinner E.C., Mansson W. Quality of life after cystectomy and urinary diversion: an evidence based analysis // J. Urol. 2005. no. 174(5). pp. 1729-36.
5. Hautmann R.E., De Petriconi Ft., Gottfried H.W. The ileal neobladder: complications and al results in 363 patients after 11 years of followup // J. Urol. 1999. no. 161(2). pp. 422-8.
6. Konety B.R., Dhawan V., Allareddy V., Joslyn S.A. Impact of malpractice caps on use and outcomes of radical cystectomy for bladder cancer: data from the surveillance, epidemiology, and end results program // J. Urol. 2005. no. 73(6). pp. 2085-9.
Фундаментальные основы радикального хирургического лечения рака мочевого пузыря (РМП) изложены в работах М.И. Когана, В.А. Перепечай (2002), А.С. Переверзева, С.Б. Петрова (2002), И.В. Чернышева (2004), В.Р. Латыпова (2005), С.А. Красного (2010), Б.П. Матвеева (2011), E.W. Gerharz et al., 2004; J.P. Stein, D.G. Skinner (2005), R.E. Hautmann (2005), A. Stenzl (2005), U.E. Studer (1997) и мн. др. Несоответствие в показателях периоперационной смертности (от 2,0 до 26,9 %) при выполнении радикальной цистэктомии (РЦЭ) у больных мышечно-инвазивным РМП, в частоте развития осложнений раннего (от 11 до 70 %) и позднего (от 12 до 23,4 %) послеоперационного периода, количестве повторных операций (от 8,7 до 30 %) не может удовлетворять онкоурологов [1, 2, 4, 5, 6].
Разноречивые результаты радикального хирургического лечения РМП высвечивают пробелы и отсутствие единой позиции различных школ в отношении необходимого и достаточного объёма оперативного вмешательства. В то же время при оценке результатов лечения РМП следует быть прагматичным и различать, с одной стороны, результаты так называемых «авторских серий» и данные отдельных высокоспециализированных центров и, с другой стороны, результаты многоцентровых рандомизированных исследований, метаанализов и национальных регистров. Имеющийся клинический материал, значительный период наблюдения за больными позволяют проанализировать собственный опыт радикального хирургического лечения больных злокачественными опухолями МП в практике специализированного стационара — ГБУЗ «Областной онкологический диспансер» г. Иркутска.
Нами была поставлена цель: на основании изучения результатов 5-летней выживаемости (общей, скорректированной, безрецидивной и безрецидивной скорректированной) и анализа послеоперационных осложнений оценить эффективность радикального хирургического лечения больных РМП (T1-T4b), включающего проведение одномоментной радикальной цистэктомии с различными методами реконструкции нижних мочевых путей.
Материалы и методы исследования
Изучены непосредственные и отдаленные результаты одномоментной радикальной цистэктомии (РЦЭ), выполненной в отделении урологии ГБУЗ «Областной онкологический диспансер» у 277 больных по поводу РМП (T1-T4b). Возраст больных находился в пределах от 34 до 82 лет (медиана 59; интерквартильный диапазон от 50 до 66 лет; 95 % ДИ: [57,0-59,4]). В возрастной структуре пациентов преобладали больные РМП в возрасте от 60 до 69 лет — 38,6 %, далее следовала возрастная группа от 50 до 59 лет — 28,9 %, на третьем месте были больные в возрасте от 40 до 49 лет — 18,4 %. Мужчин было 232 (83,8 %), женщин 45 (16,2 %). Опухоль, ограниченная МП, диагностирована у 152 (54,9 %) пациентов: рТ1 — 22,7 %, рТ2а — 17,0 %, pT2b-15,2. Опухоль МП распространялась за пределы органа у 125 (45,1 %) пациентов: pT3a — 13,7 %, pT3b — 14,4 %, pT4a — 15,5 %, pT4b — 1,4 %. Метастатическое поражение регионарных лимфатических узлов (ЛУ) выявлено у 45 (16,2 %). Отдаленные метастазы (М1) в 9 (3,2 %) случаях. По гистологической градации случаи низкодифференцированного рака отмечены — у 48,4 %, высоко и умеренно дифференцированные опухоли МП зарегистрированы в 10,1 % (G1) и 41,5 % (G2) случаях соответственно.
Для реконструкции нижних мочевых путей после РЦЭ использовали различные сегменты желудочно-кишечного тракта: накожное инконтинентное отведение мочи (операция Бриккера) выполнено у 70 (25,3 %) больных; наружное отведение мочи с созданием влажной стомы (уретерокутонеостомия, далее УКС) — у 148 (53,4 %); внутреннее отведение мочи в непрерывный кишечник (уретеросигмостомия, далее УСС) — у 12 (4,3 %); отведение мочи в сигморектальный резервуар (по Mainz pouch-2) — у 13 (4,7 %) больных; ортотопическое отведение мочи в сформированный кондуит из сигмовидной кишки (по Reddy) — у 12 (4,3 %); ортотопическая пластика мочевого пузыря (илеоцистопластика по Штудеру) — в 16 (5,8 %) случаях, ортотопическая и гетеротопическая пластика желудком по Митчеллу у 4 (1,4 %) и 2 (0,7 %) больных соответственно. Следует отметить, что УКС и УСС, выполненные у 160 (57,8 %) больных, чаще применяли в период освоения методики и у ослабленных больных. Во многих случаях этот метод деривации мочи был выбран пациентом (низкий уровень комплаенса).
Основные результаты исследования представлены с использованием доверительных интервалов, включающих истинное значение рассматриваемого параметра во всей популяции с вероятностью 95 %. Все анализируемые в работе показатели были формализованы и введены в единую электронную базу данных. Их статистическая обработка проводилась с помощью программ: istica 6.0; istica 7.0 (Soft, USA); SPSS 16.0 (SPSS Inc., USA); Microsoft Excel 2003 (Microsoft Corporation, USA). При проверке гипотез использовался 5 % уровень значимости. При анализе 5-летней выживаемости использовали общепринятые методы, рекомендованные Московским научно-исследовательским онкологическим институтом им. П.А. Герцена — это прямой метод расчета выживаемости и актуриальные методы [3].
Результаты исследования и их обсуждение
Интраоперационные осложнения зарегистрированы у 6 (0,8 %) оперированных: ранение прямой кишки — у 9 (3,2 %) пациентов, профузное кровотечение из варикозно расширенных вен таза — у 5 (1,8 %) и острая сердечно-сосудистая недостаточность — у 6 (2,2 %) пациентов. Смерть в течение 30 дней после радикальной хирургии наступила у 17 больных, послеоперационная летальность составила 6,1 %. Во время операции скончались 2 (0,7 %) пациента, причиной смерти явились кровотечения и последующая острая сердечно-сосудистая недостаточность.
После 277 РЦЭ в раннем послеоперационном периоде зарегистрировано 119 (43,0 %) осложнений у 88 (31,8 %) пациентов. В 38 (13,7 %) случаях потребовалось выполнение повторного хирургического вмешательства. В структуре ранних осложнений превалировали: обострение хронического пиелонефрита — у 23 (8,3 %) больных; перитонит и эвентерация кишечника — у 14 (5,1 %); нагноение послеоперационной раны — у 11 (4,0 %); несостоятельность межкишечного анастомоза — у 7 (2,5 %). Ранние послеоперационные осложнения встречались при всех видах отведения мочи за исключением гетеротопической пластики желудком по Митчеллу.
Из поздних послеоперационных осложнений возникших у 137 (52,7 %) пациентов, представительной группой являлись: камни мочевыводящих путей — у 33 (13,0 %) больных, стенозирование стом — у 5 (1,9 %), острый и обострение хронического пиелонефрита — у 11 (4,2 %) и 16 (6,2 %) больных соответственно; послеоперационная грыжа передней брюшной стенки — у 7 (2,7 %); стриктура уретро-кишечного соустья — у 3 (1,2 %); стриктура уретеро-кишечного соустья — у 6 (2,3 %); спаечная кишечная непроходимость — у 10 (3,8 %); лимфоцеле — у 4 (1,5 %); кишечные свищи — 4 (1,5 %) больных. Применение оперативных методов лечения при возникновении поздних послеоперационных осложнений потребовалось у 58 (22,3 %) больных.
Продолжительность одномоментной РЦЭ с различными вариантами отведения мочи составила: средняя 235,3 мин, мода 250; минимум 102; 1 — квартиль 150; медиана 240; 3 — квартиль 300; максимум 645; размах 543 (95 % ДИ: [223,6-246,8]).
Интраоперационная кровопотеря не зависела от метода отведения мочи и составила: средняя 1639,9 мл, мода 1000; минимум 100; 1 — квартиль 800; медиана 1600; 3 — квартиль 2400; максимум 5800; размах 5700 (95 % ДИ: [1525,5-1754,3]). Установлено, что средний объем интраоперационной кровопотери при выполнении РЦЭ до 2005 г. составил 2228,9 ± 1118,9 мл. (95 % ДИ: [1998,5-2459,4]), а после 2005 г. 1342,2 ± 718,6 мл. (95 % ДИ: [1237,6-1446,7]).
Местные рецидивы чаще возникали в малом тазу — у 21 (37,5 %), в регионарные лимфатические узлы — у 11 (19,6 %) пациентов. Отдаленными метастазами были поражены легкие, печень и кости — у 18 (32,1 %) больных. Возникновение рецидивов в верхних отделах мочевого тракта мы наблюдали реже — у 6 (10,7 %) больных. Длительность безрецидивного периода (мес.): среднее 23,3; мода множ.; минимум 5,6; 1 — квартиль 13,5; медиана 22,1; 3 — квартиль 34,0; максимум 49,5; размах 43,9 (95 % ДИ: [20,3-26,4]).
Общая 5-летняя выживаемость больных, включенных в исследование, составила 51,6 % (n = 143), медиана времени жизни — 16,9 мес. (рис. 1).
Рис. 1. Общая 5-летняя выживаемость больных после РЦЭ (Каплан-Майер)
Скорректированный (поправленный) показатель 5-летней выживаемости больных РМП после РЦЭ составил 88,7 % (n = 795). От прогрессирования основного заболевания в течение пяти лет скончалось 49 (17,7 %) пациентов (рис. 2).
Рис. 2. Скорректированная 5-летняя выживаемость больных после РЦЭ (Каплан‒Майер)
Лучшие показатели скорректированной выживаемости достигнуты при РМП с глубиной инвазии опухоли T1 (95,2 %) и T2b (92,9 %). При опухолевой инвазии поверхностного мышечного слоя (Т2а) данный показатель составил 89,4 %. В случае инвазии опухоли за пределы МП с прорастанием в паравезикальную клетчатку (рТ3) скорректированная 5-летняя выживаемость снижалась до 71,1 %, при pT3b ‒ до 77,5 %, а при опухолевой инвазии соседних органов (pT4a) ‒ до 60,5 % и при распространении онкологического процесса на стенку таза или брюшную стенку ‒ до 75,0 %. Различия между сравниваемыми выборками признаны статистически значимыми (p = 0,00004).
Статистически значимые результаты получены при изучении зависимости скорректированной пятилетней выживаемости от степени вовлечения в онкологический процесс ЛУ: pN0 — 85,8 %, pN1 — 50,0 %, pN2 — 67,8 %, при pN3 размер выборки недостаточный (p = 0,00579). Установлено, что метод реконструкции мочевого резервуара не оказывает статистически значимого влияния на показатель 5-летней скорректированной выживаемости больных РМП (р = 0,06156).
Показатель 5-летней общей безрецидивной выживаемости после радикального хирургического лечения РМП (n = 277) составил 48,1 % (n = 133) и имел выраженную тенденцию к улучшению при глубине инвазии РМП T1 (85,7 %) и Т2а (72,3 %), а также при отсутствии регионарного (56,9 %) и отдаленного (49,6 %) метастазирования. При всех анализируемых выборках больных различия признаны статистически значимыми. Медиана времени жизни — 24,8 месяца. Установлено, что метод реконструкции мочевого резервуара оказывает статистически значимое влияние на показатель 5-летней безрецидивной выживаемости больных РМП (T1-T4b), р = 0,000001 (рис. 3).
Рис. 3. Общая безрецидивная выживаемость больных после РЦЭ (Каплан‒Майер)
Наиболее точным показателем, отражающим излеченность от РМП, является безрецидивная скорректированная выживаемость. Безрецидивная скорректированная 5-летняя выживаемость составила 78,7 % (n = 218), медиана выживаемости 29,6 мес. (рис. 4).
Высокая безрецидивная скорректированная выживаемость отмечена у больных с опухолями, ограниченными мочевым пузырем — 89,8 %. При распространении опухоли за пределы мочевого пузыря этот показатель значительно снижался до 67,2 %. При прорастании опухоли в поверхностную мышцу (T2a) 5-летняя безрецидивная скорректированная выживаемость после цистэктомии составила 87,2 %, а при инвазии глубокого мышечного слоя (T2b) — 90,5 %. В случае инвазии опухоли за пределы МП с макроскопическим прорастанием в паравезикальную клетчатку (рТ3b) 5-летняя безрецидивная скорректированная выживаемость снижалась до 67,5 %. Аналогичная тенденция отмечена и при изучении зависимости 5-летней безрецидивной скорректированной выживаемости от степени поражения регионарных лимфоузлов. Выполнение в ходе РЦЭ регионарной лимфодиссекции позволяло при единичных и множественных регионарных метастазах добиться пятилетней безрецидивной скорректированной выживаемости, сравнимой с выживаемостью пациентов с интактными лимфоузлами, однако полученные различия не имели статистической значимости (p = 0,06703).
Рис. 4. Безрецидивная скорректированная выживаемость больных после РЦЭ (Каплан‒Майер)
Несмотря на крайне низкую общую (наблюдаемую) пятилетнюю выживаемость больных РМП после РЦЭ с последующей уретрокутанео- и уретросигмостомией (28,4 % и 25,0 % соответственно), были достигнуты приемлемые показатели скорректированной (75,0 и 75,0 % соответственно) и безрецидивной скорректированной (68,2 и 75,0 % соответственно) выживаемости. Столь низкие показатели общей пятилетней выживаемости больных РМП связаны с неблагоприятными онкологическими характеристиками, наличием тяжелой интеркурентной патологии и преклонным возрастом больных.
Выводы
Таким образом, выполнение одномоментной радикальной цистэктомии с различными методами отведения мочи обеспечивает общую — 51,6 % (медиана выживаемости 16,9 мес.), скорректированную — 88,7 % (медиана выживаемости 26,5 мес.), безрецидивную — 48,1 % (медиана выживаемости 24,8 мес.) и безрецидивную скорректированную — 78,7 % (медиана выживаемости 29,6 мес.) выживаемость больных РМП (T1-T4b). Неблагоприятными факторами, оказывающими влияние на показатели общей выживаемости, являются распространение онкологического процесса за пределы органа, поражение лимфатических узлов и метастатическое распространение процесса. Использование для реконструкции нижних мочевых путей после РЦЭ современных пластических методик позволило добиться статистически значимого повышения 5-летней безрецидивной выживаемости больных РМП (T1-T4b) с 25,0 % после УКС и 75,0 % после УСС до 78,6 % после операции Bricker, до 93,8 % после Studer, до 61,5 % после Mainz pouch II, до 75,0 % после Reddy и до 100,0 % после ортотопической и гетеротопической пластики желудком по Митчеллу (р = 0,000001) и безрецидивной скорректированной выживаемости с 68,2 % после УКС и 75,0 % после УСС до 91,4 % после операции Bricker, до 93,8 % после Studer, до 92,3 % после Mainz pouch II, до 91,7 % после Reddy и до 100,0 % после ортотопической и гетеротопической пластики желудком по Митчеллу (p = 0,00314). Метод реконструкции мочевого резервуара не оказывает статистически значимого влияния на показатель 5-летней скорректированной выживаемости больных РМП (р = 0,06156).
Наиболее высокие показатели 5-летней выживаемости отмечаются у больных с опухолями, ограниченными МП, скорректированная 5-летняя выживаемость — 95,2 %. При распространении опухоли МП за пределы органа данный показатель снижается при pT2a до 89,4 %, pT3a до 71,1 %, pT3b до 77,5 %, pT4a до 60,5 % и при pT4b до 75,0 % (р = 0,00004).
Рецензенты:
Дворниченко В.В., д.м.н., профессор, заведующая кафедрой онкологии, ГБОУ ВПО ИГМУ Минздрава России, Российская Федерация, г. Иркутск;
Лалетин В.Г., д.м.н., профессор кафедры онкологии и лучевой терапии, ГБОУ ВПО ИГМУ Минздрава России, Российская Федерация, г. Иркутск.
Работа поступила в редакцию 15.01.2014.
Библиографическая ссылка
Лелявин К.Б. РАДИКАЛЬНАЯ ЦИСТЭКТОМИЯ В ЛЕЧЕНИИ БОЛЬНЫХ РАКОМ МОЧЕВОГО ПУЗЫРЯ (T1-T4b). НЕПОСРЕДСТВЕННЫЕ И ОТДАЛЕННЫЕ РЕЗУЛЬТАТЫ // Фундаментальные исследования. — 2013. — № 12-2. — С. 243-249;
URL: https://fundamental-re.ru/ru/article/view?id=33314 (дата обращения: 10.05.2021).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник