Радиология лечение мочевого пузыря
учевая терапия рака мочевого пузыря
Лучевая терапия рака мочевого пузыряУчитывая эффективность радикальной лучевой терапии в лечении карциномы мочевого пузыря, правомерно задать вопрос, а нельзя ли вообще отказаться от цистэктомии как от метода первичного лечения? На этот вопрос попытались ответить в Великобритании, проведя большие совместные исследования. Были отобраны 200 больных, которые получили только курс лучевой терапии (60 Гр на протяжении 6 недель), или предоперационное облучение (40 Гр на протяжении 4 недель). Через месяц больным во второй группе провели радикальную цистэктомию. Спустя пять лет в этой группе была обнаружена тенденция в сторону увеличения выживаемости (38%) по сравнению с группой, получившей только курс радкальной лучевой терапии (29%). Хотя общий результат не достиг статистически достоверного уровня, сочетание предоперативного облучения и последующей операции оказалось более эффективным на контингенте больных молодого возраста мужского пола. Различие между группами может быть завышено, поскольку 20% больных из группы, произвольно отобранной для проведения лучевой терапии и последующей операции, не смогли завершить курс лечения. После лучевой терапии у некоторых больных отмечались случаи рецидивов опухоли, и поэтому им была проведена «спасительная цистэктомия» со впечатляющим результатом: 52% для 5-летней выживаемости. Такие же результаты были получены в США и в Дании. Недавно несколько больших коллективов сообщили о результатах радикальной лучевой терапии, которые оказались близкими к полученным после операции. Биологическая эффективность лучевой терапии при лечении рака мочевого пузыря иллюстрируется также феноменом «снижения стадии развития опухоли», который наблюдается после облучения. В нескольких исследованиях показано, что при исследовании образцов опухоли, взятых у больных после проведения курса лучевой терапии, индекс Р-стадии часто оказывается ниже, чем можно было предположить, исходя из первоначальной оценки состояния опухоли (Т-стадии). Например, в исследовании из клиники Royal Marsden этот эффект подтвердился почти для половины (47%) образцов ткани мочевого пузыря, взятых после лучевой терапии. С помощью лучевой терапии также достигается стерилизация лимфатических узлов, пораженных опухолью. В том же исследовании частота метастазирования узлов после облучения оказалась равной 23%, в то время как для необлученной опухоли в стадии Т3 ожидаемая величина должна быть порядка 40-50%. Лишь у 8% больных, перенесших лучевую терапию, было отмечено поражение регионарных лимфатических узлов, требующее проведения цистэктомии. Это позволяет предполагать, что лучевая терапия перед операцией будет особенно полезна для тех больных, у которых узлы поражены либо в ограниченной степени, либо в них присутствуют микрометастазы.
(а) Облучаемая область в вертикальной проекции, I — на первой стадии проводится облучение мочевого пузыря и тазовых лимфатических узлов; II — на второй стадии мочевой пузырь облучается в радикальной дозе. Облучение на первой стадии проводится с заполненным мочевым пузырем, для того, чтобы свести к минимуму радиационное поражение тонкого кишечника, (б) Схема радикального облучения во второй стадии (размеры нолей указаны в см). Подробное объяснение см. в тексте По-видимому, к числу наиболее важных результатов всех этих исследований относится вывод о том, что в случаях, когда наблюдается снижение стадии развития опухоли, 5-летняя выживаемость больных составляет 51%. Для больных, у которых этот эффект не проявлялся, 5-летняя выживаемость оказалась на уровне 22%. Хотя цистэктомия остается широко распространенным методом лечения больных с опухолями в стадии Т3, представленные выше данные, а также другие результаты позволяют предполагать, что лучевая терапия столь же эффективна, и обладает существенным преимуществом, поскольку является безболезненной процедурой. Качество жизни больных, которые перенесли операцию отвода мочи, хуже, чем у пациентов с сохраненным мочевым пузырем. Наряду с общими трудностями, больные страдают от запаха, утечки мочи, психологических трудностей, мешающих приспособиться к стоме, а также от ощущения чувства потери сексуальной привлекательности. При проведении операции на должном уровне остроту многих проблем удается снизить, однако больные, безусловно, нуждаются в поддержке и в проведении с ними разъяснительной работы как в предоперационном периоде, так и после операции. Для проведения сеансов лучевой терапии рака мочевого пузыря требуется высоковольтное оборудование. Обычно применяется метод многопольного облучения с использованием трех или четырех полей. Необходимо уделять внимание тщательному планированию схемы и режима облучения. Существуют различные точки зрения в отношении целесообразности облучения тазовых лимфатических узлов и самого мочевого пузыря. Хотя трудно продемонстрировать увеличение выживаемости больных после облучения тазовых лимфатических узлов, описанный выше феномен снижения стадии развития опухоли свидетельствует в пользу сторонников их облучения. Последствия облучения тазовой области сказываются сильнее, даже если оно проводится в относительно умеренной дозе — 40 Гр. При поражении лимфатических узлов общая 5-летняя выживаемость составляет менее 10%. Это позволяет предполагать, что при обнаружении поражения узлов распространение опухоли обычно продолжается. Большинство современных исследований (в том числе, проведенных MRC и EORTC), свидетельствуют в пользу применения новых и более обоснованных схем химиотерапии, которые используются совместно с облучением небольших участков тела. Эти схемы вполне подходят для тех же больных, у которых после облучения тазовой области проявился феномен «снижения стадии развития опухоли». Вопросы химиотерапии рака мочевого пузыря подробно рассматриваются ниже. После лучевой терапии, наряду с проявлением терапевтического эффекта, снимаются такие симптомы, как боли и гематурия. Она является наиболее ценным паллиативным методом, который применяется даже на поздних стадиях рака мочевого пузыря (стадия IV), когда практически не остается надежды на излечение.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021 — Также рекомендуем «Химиотерапия рака мочевого пузыря» — Вернуться в оглавление раздела «Онкология» Оглавление темы «Опухоли мочеполовой системы»:
|
Источник
Лечение поздних лучевых повреждений мочевого пузыря
В статье проанализированы результаты лечения больных с поздними лучевыми повреждениями мочевого пузыря (осложненными и неосложненными циститами). Отмечается, что выбор метода лечения должен основываться на данных субъективных жалоб и объективных методов исследования. Так, при выраженном болевом синдроме и инкрустированной форме лучевого цистита наилучшие результаты отмечались на фоне внутрипузырного применения Димексида. При выраженном воспалительном процессе, сопровождающемся поверхностным нарушением слизистой мочевого пузыря, а также атрофии слизистой предпочтение следует отдать инстилляциям УРО-ГИАЛА. Рексод продемонстрировал эффективность у больных с геморрагическим синдромом, при язвенном лучевом цистите и сниженном объеме мочевого пузыря.
Таблица 1. Сравнительная характеристика результатов лечения больных первой группы до и после внутрипузырного применения Димексида
Таблица 2. Сравнительная характеристика цистоскопических признаков лучевых циститов у больных первой группы до и после внутрипузырного применения Димексида
Таблица 3. Сравнительная характеристика больных второй группы до и после внутрипузырного применения УРО-ГИАЛА
Таблица 4. Сравнительная характеристика цистоскопических признаков лучевых циститов у больных второй группы до и после внутрипузырного применения УРО-ГИАЛА
Таблица 5. Сравнительная характеристика больных третьей группы до и после внутрипузырного применения Рексода
Таблица 6. Сравнительная характеристика цистоскопических признаков лучевых циститов у больных третьей группы до и после внутрипузырного применения Рексода
Введение
В настоящее время лучевая терапия является одним из основных методов лечения злокачественных новообразований органов малого таза. При отсутствии метастазов в регионарные лимфоузлы применение лучевой терапии позволяет добиться полной или частичной регрессии опухоли (рак тела и шейки матки, рак предстательной железы, в меньшей степени рак мочевого пузыря и прямой кишки) в среднем в 70-75% случаев. При этом продолжительность жизни после окончания курса лечебных мероприятий остается относительно высокой и составляет около четырех-пяти лет [1-3].
К сожалению, у части таких больных (10-15%) формируются лучевые повреждения органов малого таза: мочевого пузыря, прямой кишки и внутритазовой клетчатки [4, 5]. Оценивая данные литературы, можно констатировать неудовлетворительные результаты диагностики и лечения лучевых повреждений органов малого таза. Это выражается в частых рецидивах цистита с исходом в сморщивание мочевого пузыря, внутритазовом лучевом фиброзе со сдавлением интрамурального и юкставезикального отделов мочеточников и развитии хронической почечной недостаточности [7-8].
Проведение лучевой терапии может осложниться развитием радиационно-индуцированного фиброза, выраженность которого прямо пропорциональна величине суммарной поглощенной дозы, режиму фракционирования и времени после проведения лучевой терапии. Микроскопическое исследование тканей с радиационно-индуцированным фиброзом показало, что его формирование сопровождается развитием каркаса в подслизистом слое стенки мочевого пузыря, в сетях которого фиксируются стенки мелких артерий и вен. Происходит лучевое повреждение и самой сосудистой стенки, особенно ее адвентиции, что приводит к потере сосудами эластичности и появлению ломкости. Клинически это обнаруживается различной степенью гематурии, вплоть до профузного кровотечения. Развитие в последующем лучевого фиброза всей стенки мочевого пузыря значительно отягощает клинические симптомы и выраженность лучевого цистита [9-11].
В диагностике лучевых циститов важное значение имеют общеклинические, рентгенологические и инструментальные методы исследования. Ведущим методом исследования мочевого пузыря остается цистоскопия, позволяющая достоверно установить локализацию и степень выраженности лучевого повреждения, то есть выявить органические изменения слизистой оболочки, наличие камней и видимых опухолевых элементов, оценить состояние устьев мочеточников.
Материал и методы
В настоящей работе проведено исследование эффективности новых методов местного лечения осложненных и неосложненных лучевых циститов. 139 больных были разделены на три группы. Первую группу составили 49 пациентов (17 с неосложненными циститами и 32 — с осложненными). Они получали традиционное местное лечение: Димексид, Колларгол, синтезоновая эмульсия и облепиховое масло. Во вторую группу вошли 52 больных (26 с неосложненными циститами и 26 — с осложненными), у которых для местного лечения использовался препарат УРО-ГИАЛ. В местной терапии третьей группы — 38 пациентов (13 с неосложненными циститами и 25 — с осложненными) — применялась супероксиддисмутаза (препарат Рексод). Кроме того, всем пациентам была назначена антибактериальная, антикоагулянтная, вазоактивная, симптоматическая и иммунная терапия.
Местное лечение больных первой группы начиналось с инстилляций 10%-ного Димексида в объеме 20 мл. Применение этого препарата патогенетически обосновано, поскольку он обладает выраженным противовоспалительным, противоотечным и обезболивающим эффектом. В связи с тем что Димексид является органическим растворителем и легко проникает в ткани, в раствор добавлялись антибиотики (гентамицин, амикацин), фибролизирующие (Лидаза) и противовоспалительные препараты (преднизолон). Инстилляции проводились ежедневно по 20 мл (от 10 до 15 процедур). У больных с микрогематурией или неинтенсивной примесью крови в моче для инстилляций мочевого пузыря дополнительно применялся 3%-ный Колларгол 20 мл на одно введение. При неэффективности монотерапии Колларголом для усиления гемостатического эффекта его чередовали с охлажденной аминокапроновой кислотой. После стихания воспалительных процессов внутрипузырно в подогретом виде один раз в сутки в течение 10-15 дней вводились синтезоновая эмульсия и облепиховое масло. Действие этих препаратов направлено на усиление репараторных процессов в стенке мочевого пузыря. Благодаря жировой основе они оказывают выраженное обволакивающее и обезболивающее действие.
Местное лечение больных второй группы подразумевало применение препарата на основе гиалуроновой кислоты УРО-ГИАЛ. УРО-ГИАЛ — вязкоэластичный протектор межклеточного вещества уротелия мочевого пузыря и уретры. УРО-ГИАЛ позволяет создать вязкоэластичную пленку на слизистой, тем самым защищая ее от агрессивного воздействия мочи и препятствуя адгезии микробов к поврежденной поверхности. Инстилляции УРО-ГИАЛА проводились через день в течение 12-15 дней, затем в режиме одно введение в неделю.
В третьей группе пациентам назначался препарат супероксиддисмутазы Рексод. Рексод прямо инактивирует свободные радикалы, блокирует реакцию перекисных радикалов с арахидоновой кислотой, ослабляет активное действие лейкотриена В4, ингибирует хемотаксис лейкоцитов, значительно уменьшает синтез коллагена фибробластами (способствует регрессии радиационно-индуцированного фиброза). Рексод вводился внутрь мочевого пузыря, при этом содержимое флакона растворяли непосредственно перед введением в 10 мл стерильного физиологического раствора. Инстилляции проводились один раз в сутки на протяжении 15-20 дней.
Результаты и обсуждение
Результаты лечения больных первой группы представлены в таблице 1. Приведенные данные свидетельствуют о значительном уменьшении частоты ночного мочеиспускания и снижении бактериурии у большинства больных как с осложненными, так и с неосложненными циститами. Несмотря на по-прежнему высокий уровень лейкоцитурии, она носила менее выраженный характер. Макрогематурия после лечения не выявлялась у пациентов с неосложненными циститами, но сохранялась у 18% пациентов с осложненными циститами.
Сравнительный анализ УЗИ-признаков лучевых циститов у больных первой группы продемонстрировал, что внутрипузырное применение Димексида позволило очистить мочевой пузырь от солевой инкрустации более чем в 50% случаев. К сожалению, основные УЗИ-признаки воспаления (взвесь в просвете мочевого пузыря и утолщение его стенок) были купированы у незначительного числа пациентов.
Динамика выраженности цистоскопических признаков лучевых циститов у больных первой группы до и после лечения продемонстрирована в таблице 2. У пациентов как с неосложненными, так и осложненными циститами сохранялись воспаление (гиперемия и отек) и телеангиоэктазии. Таким образом, внутрипузырное применение Димексида было наиболее эффективным у пациентов с выраженным болевым синдромом и инкрустированной формой лучевого цистита.
Результаты лечения больных второй группы представлены в таблице 3. Следует отметить выраженное противовоспалительное действие УРО-ГИАЛА. Так, частота ночного мочеиспускания сократилась в два раза более чем у 56% пациентов с неосложненными циститами и у 59% с осложненными циститами. Лейкоцитурия уменьшилась в два раза у больных с осложненными циститами и практически не выявлялась у пациентов с неосложненными циститами (12%), а бактериурия сохранилась только у 27 и 25% больных в обеих подгруппах соответственно.
Основные УЗИ-признаки воспаления (взвесь в просвете мочевого пузыря и утолщение его стенок) исчезли у подавляющего числа больных. Однако УРО-ГИАЛ практически не оказал действия на инкрустированные циститы, особенно у больных со сниженным объемом мочевого пузыря.
Характеристика цистоскопических признаков лучевых циститов у больных второй группы до и после лечения продемонстрирована в таблице 4. Гиперемия и отек беспокоили менее чем 25% больных как с неосложненной, так и осложненной формой цистита. Частота эрозии у пациентов с неосложненными циститами уменьшилась в четыре раза. Однако более чем у 70% пациентов сохранились телеангиоэктазии. Язва мочевого пузыря у больных с осложненными циститами уменьшилась в размерах и очистилась от фибрина.
Можно сделать вывод, что применяемая схема лечения — инстилляции УРО-ГИАЛА — наиболее эффективна у пациентов с выраженным воспалительным процессом и болевым синдромом, связанным с воспалением стенок мочевого пузыря, и может применяться у больных с любой формой лучевого цистита, осложненного бактериальной инфекцией.
Результаты лечения больных третьей группы представлены в таблице 5. Почти у половины больных с неосложненными и осложненными циститами в два раза уменьшилась частота ночного мочеиспускания. У 75 и 90% пациентов соответственно сохранилась лейкоцитурия. Однако бактериурия почти у половины больных в обеих подгруппах не определялась, а макрогематурия исчезла у всех пациентов.
Сравнительная характеристика УЗИ-признаков лучевых циститов у больных третьей группы продемонстрировала достоверное увеличение объема мочевого пузыря у пациентов с микроцистисом, однако в меньшей степени Рексод оказал положительное действие на инкрустацию стенок мочевого пузыря и наличие взвеси в его просвете.
Что касается выраженности цистоскопических признаков лучевых циститов у больных третьей группы (табл. 6), то в результате лечения язва мочевого пузыря исчезла у всех больных, однако более чем у 60% пациентов с осложненными циститами сохранялись признаки воспаления (гиперемия и отек). Таким образом, Рексод можно рекомендовать больным с геморрагическим синдромом, при язвенном лучевом цистите и сниженном объеме мочевого пузыря.
Заключение
Следует отметить, что используемые препараты (Димексид, УРО-ГИАЛ и Рексод) имеют разную направленность действия. В частности, при выраженном фиброзе стенки мочевого пузыря предпочтение следует отдавать применению инстилляций раствора Димексида. При выраженном воспалительном процессе, сопровождающемся поверхностным нарушением слизистой мочевого пузыря, а также атрофии слизистой наиболее эффективным оказалось применение УРО-ГИАЛА. У больных с гематурией и глубокими нарушениями целостности слизистой мочевого пузыря (язвенно-некротический цистит) наиболее высокие результаты продемонстрировало применение супероксиддисмутазы. Выбор метода лечения должен основываться на данных субъективных жалоб и объективных методов исследования.
Источник
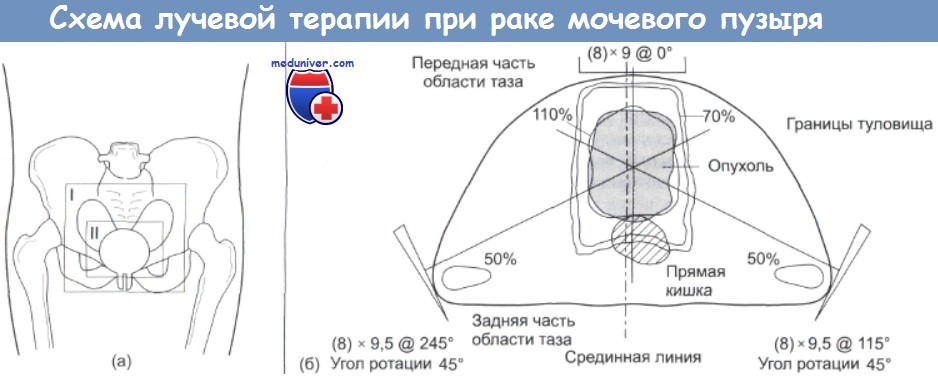 Схема, иллюстрирующая типичную процедуру облучения внешним пучком при инвазивном раке мочевого пузыря (в стадии Т3).
Схема, иллюстрирующая типичную процедуру облучения внешним пучком при инвазивном раке мочевого пузыря (в стадии Т3).