Повреждение сфинктера мочевого пузыря
Содержание статьи
Травма мочевого пузыря
Травма мочевого пузыря — это нарушение целостности стенки органа, вызванное механической травмой, воздействием химических веществ, редко – давлением мочи при некоторых заболеваниях. Проявляется болью в животе, припухлостью и синюшностью кожи над лоном, учащенными ложными позывами к мочеиспусканию, снижением или отсутствием диуреза, макрогематурией, подтеканием мочи из раневого отверстия, нарастанием симптоматики травматического шока. Диагностируется с помощью ретроградной цистографии, катетеризации, УЗИ, КТ, МРТ мочевого пузыря, общего анализа мочи, лапароскопии. В легких случаях возможно консервативное ведение с установкой катетера, при внутрибрюшинных и крупных внебрюшинных разрывах выполняется реконструктивная пластика органа.
Общие сведения
В структуре общего травматизма механические повреждения мочевого пузыря составляют от 0,4 до 15% (в России — от 1 до 7%). В последние годы отмечается более частое травмирование органа, что связано с усилением интенсивности транспортного сообщения, износом автопарка, увеличением количества тяжелых техногенных катастроф и локальных военных конфликтов.
Пик травматизации наблюдается в 21-50-летнем возрасте, около 75% пострадавших — мужчины. Особенностью травм является преимущественно сочетанный характер поражения (в 100% открытых ранений и в 85% тупых травм кроме мочевого пузыря повреждаются кости таза, позвоночник, другие органы). Актуальность своевременной диагностики и экстренных лечебных мероприятий обусловлена неблагоприятным прогнозом – в соответствии с оценочными шкалами 31,4% пострадавших относятся к категории тяжелых, 49,2% — крайне тяжелых больных, уровень смертности превышает 25%.
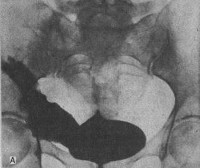
Травма мочевого пузыря
Причины
У большинства пациентов травматическое повреждение мочевого пузыря связано с воздействием на его стенку внешних механических факторов различного происхождения. В редких случаях травма обусловлена влиянием агрессивных химических веществ, инсталлированных в мочевой пузырь, или наличием заболеваний, препятствующих мочеиспусканию. Причинами травм являются:
- Дорожно-транспортные происшествия. Более чем в четверти случаев мочевой пузырь травмируется во время ДТП. Повреждение возникает при прямом ударе в проекцию органа, сильном сдавлении в транспортном средстве, ранении осколками тазовых костей, конструктивными элементами автомобиля, предметами окружающей среды.
- Ятрогенные факторы. 22-23% пациентов получают травму во время медицинских манипуляций. Стенка органа может повреждаться при его катетеризации, бужировании уретры, выполнении операций — трансуретральных вмешательств, кесарева сечения, экстирпации матки, миомэктомии, аденомэктомии, резекции толстой кишки и др.
- Бытовой и производственный травматизм. В 10% случаев повреждение происходит из-за падения с высоты на твердый предмет. При наличии предпосылок (переполнении мочой, рубцовых изменениях и др.) возможен разрыв органа из-за резкого сотрясения тела при прыжке. У 4,2% пострадавших травма возникает под действием производственных факторов.
- Насильственные действия. Целостность мочевого пузыря может нарушаться при тупых ударах в живот, ранении ножом или другими острыми предметами в драках, при криминальных абортах. В военное время в 3-4 раза увеличивается количество огнестрельных травм и открытых ранений органа осколками взрывных боеприпасов.
- Урологические заболевания. Крайне редко самопроизвольный разрыв мочевого пузыря отмечается у пациентов, которые страдают заболеваниями, нарушающими мочеиспускание, — аденомой и раком простаты, стенозом уровезикальной шейки, стриктурами уретры. Чаще урологическая патология играет роль предрасполагающего фактора, усиливая растяжение органа.
Риск возникновения наиболее тяжелых повреждений — частичных или полных разрывов — зависит не только от силы травматического воздействия, но и от места его приложения, направления, внезапности. Вероятность получения травмы существенно возрастает при алкогольном опьянении, которое способствует переполнению мочевого пузыря из-за притупления позывов к мочеиспусканию и провоцирует травмоопасное поведение. Предполагающими факторами также являются опухолевые поражения, фиброзные изменения стенки органа после перенесенных операций, лучевой терапии, воспалительных заболеваний.
Патогенез
Механизм травмы мочевого пузыря зависит от типа факторов, вызвавших повреждение. При тупом ударе в надлобковую область, противоударе о крестец, сдавлении резко повышается внутрипузырное давление, усиливается нагрузка на мочепузырную стенку. Возникновение гидродинамического эффекта способствует внутрибрюшинному разрыву органа на участке наименее развитой мускулатуры (обычно по задней стенке пузыря возле его верхушки).
Рана обычно рваная, с неровными краями. При меньшей силе механического воздействия удар вызывает закрытые повреждения (ушибы, кровоизлияния в стенку). Аналогичный патогенез характерен при наличии урологических заболеваний с нарушением пассажа мочи. Значительное смещение пузыря при механических травмах приводит к резкому натяжению поддерживающих боковых и пузырно-простатических связок с внебрюшинным разрывом мягко-эластичной стенки органа. Сильный удар способен вызвать разрыв связок, мочепузырных кровеносных сосудов, отрыв шейки.
При закрытых и открытых повреждениях везикальных оболочек острыми предметами, инструментами, осколками костей происходит поверхностное, глубокое надсечение или сквозное рассечение стенки. Рана при этом обычно линейная. Сочетание с гидродинамическим ударом при огнестрельных и оскольчатых ранениях приводит к дополнительным радиальным надрывам круглого раневого отверстия.
Классификация
Критериями систематизации травматических повреждений являются степень тяжести, возможное сообщение с окружающей средой, расположение разрыва по отношению к брюшине, сочетание с травмами других органов. Такой подход позволяет спрогнозировать течение патологического процесса и вероятные осложнения, выбрать оптимальную тактику ведения пациента. В зависимости от тяжести повреждения мочепузырной стенки травмы могут быть глухими (ушиб, поверхностное ранение наружной оболочки, надрыв слизистой) или сквозными (полный разрыв, отрыв шейки). В свою очередь, сквозные повреждения разделяют на три группы:
- Интраперитонеальные разрывы. Наблюдаются более чем у 60% пострадавших. Обычно обусловлены прямыми ударами в переполненный мочевой пузырь. Из-за истечения мочи в брюшную полость быстро осложняются перитонитом.
- Экстраперитонеальные разрывы. Возникают в 28% случаев. Чаще провоцируются избыточным натяжением поддерживающего связочного аппарата. Травмированный мочевой пузырь не сообщается с брюшной полостью, моча истекает в малый таз.
- Комбинированные разрывы. Наблюдаются у 10% пострадавших. Множественное повреждение стенки органа обычно сочетается с переломами тазовых костей. Сообщение между мочевым пузырем, брюшной и тазовой полостями обуславливает особую тяжесть патологии.
До 90% травм мирного времени являются закрытыми, благодаря сохранению целостности кожи поврежденный мочевой пузырь не сообщается с внешней средой. В военный период, при насильственных действиях с использованием холодного и огнестрельного оружия возрастает частота открытых травм, при которых нарушается целостность кожи, возникает сообщение между оболочками или полостью органа и окружающей средой. По наблюдениям специалистов в сферах травматологии и клинической урологии, сочетанные повреждения превалируют над изолированными. У 40-42% пациентов выявляются переломы костей таза, у 4-10% — разрывы кишечника, у 8-10% — травмы других внутренних органов.
Симптомы
Важная клиническая особенность данного повреждения — частое преобладание общей симптоматики над локальной. Из-за выраженного болевого синдрома и кровотечения у пострадавших нарастают признаки гемодинамических нарушений, у 20,3% наблюдается травматический шок: снижается уровень АД, ускоряется частота сердечных сокращений, кожные покровы бледнеют, покрываются липким холодным потом, возникает слабость, головокружение, оглушенность, спутанность, а затем и потеря сознания.
Из-за раздражения брюшины мочой пациенты с интраперитонеальными разрывами ощущают интенсивную боль в надлонной области, в нижней части брюшной полости, которая впоследствии распространяется на весь живот, сопровождается тошнотой, рвотой, задержкой газов и стула, напряжением брюшной мускулатуры. Специфические симптомы травмы мочепузырной стенки — боль и локальные изменения области повреждения, дизурия. При открытых ранениях на передней стенке живота, реже — в зоне промежности выявляется зияющая рана, из которой может истекать моча.
Для закрытых внебрюшинных травм характерно образование болезненной припухлости над лобком, в паху, синюшный цвет кожных покровов из-за их пропитывания кровью. Пострадавшие испытывают частые ложные позывы к мочеиспусканию со значительным уменьшением либо полным отсутствием диуреза, выделением капель крови из мочеиспускательного отверстия. При сохранении мочевыделения у пациентов с надрывами слизистой моча окрашена кровью.
Осложнения
Летальность при травматических повреждениях мочевого пузыря, особенно открытых и сочетанных, достигает 25% и более. Причинами смерти обычно являются запущенные формы перитонита, болевой, инфекционно-токсический, геморрагический шок, сепсис. Сквозные травмы стенки мочевого пузыря быстро осложняются вовлечением в процесс других органов. Анатомические особенности паравезикальной, забрюшинной клетчатки, фасциальных пространств способствуют мочевой инфильтрации, распространению затеков, образованию урогематом.
При внутрибрюшинном разрыве возникает уроасцит. Вторичное инфицирование приводит к формированию абсцессов, флегмон. У 28,3% пациентов развивается мочевой перитонит, у 8,1% — уросепсис. Восходящее распространение инфекции провоцирует начало острого пиелонефрита. В 30% случаев при сочетании травмы пузыря с повреждениями других органов наблюдается ДВС-синдром. В отдаленном периоде у больных иногда формируются мочевые свищи, наблюдается недержание мочи.
Диагностика
С учетом серьезности прогноза всем пациентам с подозрением на травму мочевого пузыря назначают комплексное обследование, позволяющее выявить разрывы мочепузырной стенки, определить их особенности и количество, обнаружить возможное повреждение смежных органов. Рекомендованными методами лабораторной и инструментальной диагностики являются:
- Общий анализ мочи. Исследование удается провести только при сохраненном мочеиспускании. Объем разовой порции зачастую уменьшен. В анализе в большом количестве присутствуют эритроциты, подтверждающие наличие кровотечения.
- УЗИ. По данным эхографии мочевого пузыря, орган обычно уменьшен в объеме, рядом с ним определяются скопления крови. Исследование дополняют УЗИ почек, при проведении которого обнаруживаются признаки постренального нарушения оттока мочи, и УЗИ брюшной полости для выявления свободной жидкости.
- Рентген. Ретроградная цистография считается «золотым стандартом» диагностики этого вида травм. Разрывы органа проявляются затеками рентгеноконтрастного вещества в пузырно-прямокишечную ямку, околопузырную клетчатку, область крыльев подвздошной кости, полость брюшины.
- Томография мочевого пузыря. С помощью КТ удаётся получить трехмерное изображение поврежденного органа, в ходе МРТ он изучается послойно. Результаты томографии позволяют точно оценить повреждения, объем урогематом, выявить сочетанные травмы.
- Диагностическая лапароскопия. Осмотр мочевого пузыря через лапароскоп дает возможность определить особенности травмированной стенки, обнаружить затеки мочи, крови. При выполнении лапароскопии визуализируются повреждения соседних органов.
Большое диагностическое значение играет катетеризация мочевого пузыря, дополненная вливанием в него жидкости (проба Зельдовича). О наличии разрывов свидетельствует отсутствие мочевыделения через катетер или поступление небольшого количества мочи с кровью. Жидкость, введенная в травмированный орган, обратно выделяется слабой струей и не в полном объеме. При интраперитонеальных разрывах возможно отхождение в 2-3 раза большего объема жидкости, что обусловлено проникновением катетера в брюшную полость и выделением ранее попавшей в нее мочи.
Экскреторную урографию назначают с осторожностью, чтобы не спровоцировать развитие контраст-индуцированной нефропатии на фоне шоковых изменений гемодинамики. Цистоскопия обычно не проводится из-за риска занесения инфекции. В общем анализе крови определяются признаки анемии — эритропения, снижение уровня гемоглобина, возможен умеренный лейкоцитоз и повышение СОЭ.
Дифференциальная диагностика проводится с повреждением заднего отдела уретры, травмами печени, селезенки, различных отделов кишечника, разрывами сосудов брыжейки. Кроме врача-уролога пациента осматривает травматолог, хирург, анестезиолог-реаниматолог, терапевт, по показаниям — проктолог, гинеколог, кардиолог, гастроэнтеролог, невропатолог, нейрохирург.
Лечение травмы мочевого пузыря
Пострадавшего срочно госпитализируют в травматологическое или урологическое отделение, переводят на строгий постельный режим. Консервативное ведение в виде катетеризации (обычно на 3-5 суток до прекращения макрогематурии) возможно только при контузии мочевого пузыря, надрывах слизистой при грубых медицинских манипуляциях, небольших экстраперитонеальных разрывах с сохраненной уровезикальной шейкой. Остальным пострадавшим показано экстренное проведение реконструктивного хирургического вмешательства с дренированием брюшной или тазовой полостей.
На этапе предоперационной подготовки назначаются гемостатические, антибактериальные, противовоспалительные, анальгезирующие препараты, средства для стабилизации гемодинамики. Объем операции зависит от особенностей повреждения. При внутрибрюшинных разрывах мочевой пузырь перед ушиванием раны экстраперитонизируют для прекращения подтекания мочи и проведения полноценной ревизии, после реконструкции поврежденного органа брюшную полость в обязательном порядке санируют.
Внебрюшинные повреждения ушивают без экстраперитонизации. Вне зависимости от типа травмы после восстановления целостности стенки мужчинам накладывают эпицистостому , женщинам устанавливают уретральный катетер. Брюшную или тазовую полость дренируют. После операции продолжают введение антибиотиков, анальгетиков, противошоковую инфузионную терапию.
Прогноз и профилактика
Нарушения целостности стенок мочевого пузыря обоснованно считаются тяжелыми, прогностически неблагоприятными травмами. Соблюдение алгоритма хирургического лечения больных обеспечивает достоверное снижение частоты осложнений даже при тяжелых повреждениях. Профилактика направлена на создание безопасных производственных условий, соблюдение правил дорожного движения, выполнение требований безопасности при занятиях травмоопасными хобби и видами спорта, отказ от злоупотребления алкоголем. Для уменьшения предпосылок к травматизму пациентам с диагностированными заболеваниями простаты, уретры, мочевого пузыря рекомендуется регулярное наблюдение и лечение у уролога.
Источник
Лечение функциональных нарушений опорожнения мочевого пузыря | #09/04 | «Лечащий врач» – профессиональное медицинское издание для врачей. Научные статьи.
Лечение больных с функциональными нарушениями опорожнения мочевого пузыря является насущной проблемой нейроурологии. Это связано с тем, что до настоящего времени не разработано эффективных и этиопатогенетически обоснованных методов лечения таких больных.

Выделяют нейрогенные, миогенные (миопатии) и психогенные (неврозы, шизофрения, истерия и др.) факторы, лежащие в основе функциональных нарушений опорожнения мочевого пузыря. Нейрогенные нарушения и повреждения — основная причина таких нарушений. В отсутствие причины функциональных нарушений опорожнения мочевого пузыря следует думать об идиопатических формах заболевания.
Согласно классификации Международного общества по удержанию мочи, функциональные нарушения опорожнения мочевого пузыря — это результат недостаточной функции мочевого пузыря, гиперактивности уретры или следствие комплексного воздействия обоих нарушений [1]. Недостаточная функция мочевого пузыря возникает вследствие снижения или отсутствия сократительной способности детрузора (арефлексия), которые встречаются при локализации повреждения или неврологического поражения в области фронтальных долей и моста головного мозга, сакрального отдела спинного мозга, при повреждении волокон конского хвоста, тазового сплетения и нервов мочевого пузыря, а также при рассеянном склерозе. Гиперактивность уретры — это следствие наружной детрузорно-сфинктерной диссинергии (ДСД) или нерасслабляющегося (спастического) поперечно-полосатого (п/п) сфинктера уретры, также может проявиться как вариант синдрома Фоулера у женщин. При этом наружная ДСД наблюдается при супрасакральном уровне поражения спинного мозга.
В литературе имеются лишь единичные сообщения о распространенности функциональных нарушений опорожнения мочевого пузыря. Так, P. Klarskov и соавт., оценивая обращаемость в лечебные учреждения Копенгагена, выявили, что ненейрогенные формы нарушения опорожнения мочевого пузыря встречаются в среднем у 7 женщин на 100 000 населения [2]. По данным T. Tammela и соавт., после оперативных вмешательств на органах брюшной полости нарушения опорожнения мочевого пузыря встречаются у 2,9 % пациентов, а после проктологических операций — у 25% больных [3]. Многие авторы считают данную проблему особенно значимой у неврологических больных.
Клиническим проявлением снижения сократительной способности детрузора и нерасслабляющегося п/п сфинктера уретры являются симптомы нарушения опорожнения мочевого пузыря, к которым относятся затрудненное мочеиспускание тонкой, вялой струей, прерывистое мочеиспускание, необходимость прилагать усилия и натуживаться, чтобы начать мочеиспускание, ощущение неполного опорожнения мочевого пузыря.
При отсутствии сократительной способности детрузора в сочетании с паралитическим состоянием п/п сфинктера уретры больные опорожняют мочевой пузырь, искусственно увеличивая внутрибрюшное давление, что клинически проявляется мочеиспусканием слабой струей мочи. При отсутствии сократительной способности детрузора в сочетании со спастическим состоянием наружного сфинктера уретры в большинстве случаев самостоятельное мочеиспускание невозможно и отмечается хроническая задержка мочи.
Нерасслабляющийся п/п сфинктер уретры приводит к инфравезикальной обструкции с симптомами нарушения опорожнения мочевого пузыря.
Клинические проявления наружной ДСД (непроизвольное сокращение п/п сфинктера уретры во время мочеиспускания или непроизвольного сокращения детрузора) включают два вида симптомов, а именно: нарушения опорожнения и накопления мочи в мочевом пузыре. Последние включают учащенное и ургентное мочеиспускание нередко в сочетании с ургентным недержанием мочи и никтурией. Для наружной ДСД характерно неполное опорожнение мочевого пузыря и развитие пузырно-мочеточникового рефлюкса.
Таким образом, различные формы нарушения опорожнения мочевого пузыря могут иметь во многом сходную клиническую картину. В связи с этим правильная и своевременная диагностика функциональных нарушений опорожнения мочевого пузыря является залогом успешного лечения.
Диагностика функциональных нарушений опорожнения мочевого пузыря складывается из сбора жалоб и анамнеза, урологического и неврологического обследования, а также дополнительных методов обследования, среди которых основное место занимает уродинамическое исследование. На начальном этапе обследования обязательна оценка симптомов нижних мочевых путей на основании вопросника I-PSS (Internanional Prostate Symptom Score). Вопросник I-PSS был предложен для оценки нарушений акта мочеиспускания вследствие заболеваний предстательной железы, однако в настоящее время он с успехом применяется и в случаях проявления симптомов заболеваний нижних мочевых путей, вызванных различными факторами, в том числе и неврологического характера.
Для уточнения поведения детрузора и его сфинктеров в фазу опорожнения мочевого пузыря наиболее информативным методом исследования больных является комплексное уродинамическое исследование.
Уродинамическими признаками наружной ДСД, характерной для надкрестцовой локализации патологического процесса, особенно в шейном отделе спинного мозга, являются регистрируемые с помощью электромиографии во время мочеиспускания «всплески» сократительной активности п/п сфинктера уретры и мышц тазового дна. Сокращение мышц тазового дна затрудняет или полностью прерывает поток мочи. Для нерасслабляющегося сфинктера уретры характерно отсутствие снижения электромиографической активности п/п сфинктера уретры во время мочеиспускания. Снижение или отсутствие сократительной способности детрузора уродинамически проявляется отсутствием плавного повышения детрузорного давления в ходе цистометрии или отсутствием позыва к акту мочеиспускания.
Следует подчеркнуть, что только уродинамическое обследование дает возможность достоверно установить форму нарушения функции нижних мочевых путей, приводящих к нарушению опорожнения мочевого пузыря, и во многом определить выбор метода лечения.
Ультразвуковое исследование почек и мочевого пузыря, также как и экскреторная урография, позволяет уточнить анатомическое состояние верхних мочевых путей и количество остаточной мочи в мочевом пузыре. По количеству остаточной мочи в мочевом пузыре после акта мочеиспускания (в норме до 50 мл) можно косвенно судить о функциональном состоянии детрузора и наличии инфравезикальной обструкции.
В таблице перечислены методы лечения больных с функциональными нарушениями опорожнения мочевого пузыря, из которых только медикаментозная терапия и дорзальная ризотомия с электростимуляцией передних корешков могут действительно считаться методами лечения, тогда как другие скорее являются способами опорожнения мочевого пузыря. При этом даже медикаментозная терапия во многом является симптоматическим методом лечения. Несмотря на это, назначение лекарственных средств представляет собой первый этап лечения больных с функциональными нарушениями опорожнения мочевого пузыря. Выбор медикаментов зависит от вида нарушения функции нижних мочевых путей. Так, в случае нарушения сократительной способности детрузора применяют антихолинэстеразные средства и М-холиномиметики, а при гиперактивности уретры — центральные миорелаксанты и α-блокаторы.
У 22 больных со сниженной сократительной способностью детрузора использовали дистигмина бромид (убретид) в дозе 5 мг через день за 30 мин до завтрака в течение 2 мес. При этом через каждые 2 нед делали 7-дневный перерыв в приеме препарата. Механизм действия дистигмина бромида заключается в блокировании ацетилхолинэстеразы, что сопровождается увеличением концентрации ацетилхолина в синаптической щели и соответственно приводит к облегчению передачи нервного импульса.
У всех больных терапевтический эффект развивался в первую неделю приема препарата и выражался в снижении среднего балла I-PSS c 15,9 до 11,3, а количества остаточной мочи — с 82,6 до 54,3 мл. Субъективно пациенты отмечали усиление ощущения позыва и облегчение начала акта мочеиспускания.
Следует отметить, что до настоящего времени остается открытым вопрос о продолжительности лечения антихолинэстеразными средствами. По нашим данным, у 82% больных в разные сроки после окончания 2-месячного курса лечения отмечалось возобновление симптомов, потребовавшее повторного назначения препарата.
К сожалению, мы не накопили собственного опыта применения бетанехола у больных со сниженной сократительной способностью детрузора, так как данный препарат не зарегистрирован для клинического применения в нашей стране и соответственно отсутствует в аптечной сети. Механизм действия бетанехола аналогичен действию ацетилхолина на гладкие миоциты. Данные других авторов показывают, что бетанехол может применяться при лечении больных с легкой степенью нарушения сократительной способности детрузора [4, 5].
α1-адреноблокатор доксазозин (кардура) использовали в ходе лечения 30 больных с гиперактивностью уретры, в том числе 14 пациентов с наружной ДСД и 16 с нарушением произвольного расслабления п/п сфинктера уретры. Доксазозин назначали в дозе 2 мг/сут на ночь.
Через 6 мес средний балл по шкале I-PSS у больных с наружной ДСД снизился с 22,6 до 11,4, количество остаточной мочи уменьшилось с 92,6 до 32,4 мл, а максимальная скорость потока мочи увеличилась с 12,4 до 16,0 мл/сек.
Кроме того, через 6 мес у больных с нарушением произвольного расслабления п/п сфинктера уретры средний балл I-PSS снизился с 14,6 до 11,2, количество остаточной мочи — с 73,5 до 46,2 мл, а максимальная скорость потока мочи увеличилась с 15,7 до 18,4 мл/сек.
Баклофен и тизанидин (сирдалуд) являются центральными миорелаксантами. Они снижают возбуждение моторных нейронов и интернейронов и могут ингибировать передачу нервного импульса в спинном мозге, уменьшая спастичность п/п мышц. По нашим данным, после применения баклофена в дозе 20 мг/сут и тизанидина в дозе 4 мг/сут не было выявлено существенной динамики субъективных и объективных симптомов как у больных с наружной ДСД, так и у пациентов с нарушением расслабления п/п сфинктера уретры. Выраженная слабость мускулатуры конечностей на фоне приема этих препаратов не позволяет увеличивать дозу препаратов, что существенно ограничивает их применение в клинической практике.
Следует отметить, что медикаментозная терапия эффективна у больных с начальными и легкими формами нарушения опорожнения мочевого пузыря. Тем не менее ее целесообразно использовать в качестве первого этапа лечения. В случае недостаточной эффективности медикаментозной терапии необходимо искать новые пути решения проблемы адекватного опорожнения мочевого пузыря.
Предложенная Lapides и соавт. в 80-е гг. прошлого столетия интермиттирующая аутокатетеризация мочевого пузыря до настоящего времени остается одним из основных методов опорожнения мочевого пузыря [6]. Однако этот метод имеет ряд осложнений, к которым относятся инфекции нижних мочевых путей, стриктуры уретры и, самое главное, значительное снижение качества жизни. При невозможности выполнения (неврологические больные с тетраплегией, больные с ожирением) или отказе пациента от аутокатетеризации, у лиц с наружной ДСД и нерасслабляющимся сфинктером уретры, а также со сниженной сократительной способностью детрузора для адекватного опорожнения мочевого пузыря применяют в последние годы имплантацию специальных стентов (производства фирм Balton, Mentor, МедCил) и инъекции ботулинического токсина в зону п/п сфинктера уретры.
 |
| Рисунок 1. Временный уретральный стент |
Временные уретральные стенты имеют форму цилиндра, выполненного из проволочной спирали толщиной 1,1 мм, изготовлены они на основе полимолочной и полигликоликовой кислот с различным периодом разрушения (от 3 до 9 мес) посредством гидролиза (рис. 1). Механические свойства и время разрушения временных стентов зависят от степени поляризации, места и формы зоны имплантации.
Мы имеем опыт применения временных уретральных стентов у семи мужчин с наружной ДСД и у четырех пациентов, у которых отсутствовала сократительная способность детрузора. Временный уретральный стент устанавливали при уретроцистоскопии таким образом, чтобы он «шинировал» как простатический, так и мембранозный отделы уретры. Такое положение стента обеспечивает адекватное опорожнение мочевого пузыря.
У всех больных отмечалось восстановление самостоятельного мочеиспускания сразу после имплантации уретрального стента. Пациенты с наружной ДСД осуществляли мочеиспускание по позыву, а больные с отсутствием сократительной способности детрузора с интервалом 4 ч (6 раз в сутки) с использованием приема Креда. По данным ультразвукового сканирования, через 10 нед после установки стента у больных с наружной ДСД не отмечалось остаточной мочи, а у больных с отсутствием сократительной способности детрузора среднее количество остаточной мочи составило 48 мл и зависело от адекватности выполнения приема Креда. Очень важно, что у больных с наружной ДСД было выявлено снижение максимального детрузорного давления во время мочеиспускания в среднем с 72 до 35 см вод. ст. (профилактика развития пузырно-мочеточникового рефлюкса).
Мы считаем, что временные уретральные стенты обеспечивают адекватное опорожнение мочевого пузыря и показаны тем больным с нарушением опорожнения мочевого пузыря, которым не может быть выполнена интермиттирующая катетеризация мочевого пузыря или которые воздерживаются от нее по различным причинам. Временные стенты могут являться методом отбора больных для установки постоянных (металлических) стентов.
В последние годы в литературе появились сообщения об успешном использовании ботулинического токсина у больных с функциональными нарушениями опорожнения мочевого пузыря. В нашей клинике ботулинический токсин применялся у 16 больных с нарушением опорожнения мочевого пузыря, в том числе у девяти с наружной ДСД, у трех с нерасслабляющимся п/п сфинктером уретры и у четырех с нарушением сократительной способности детрузора. Мы использовали ботулинический токсин типа А фармацевтической фирмы Allergan. Коммерческое название препарата — ботокс (Botox), он представляет собой лиофилизированный порошок белого цвета в вакуумных стеклянных флаконах объемом 10 мл, закрытых резиновой пробкой и герметичным алюминиевым затвором. В одном флаконе содержится 100 ЕД ботулинического токсина типа А.
 |
| Рисунок 2. Введение ботулинического токсина у мужчин |
Механизм действия ботокса заключается в блокировании выброса ацетилхолина из пресинаптической мембраны в нервно-мышечном синапсе. Фармакологическим эффектом этого процесса является стойкая хемоденервация, а клиническим проявлением — расслабление мышечных структур.
Согласно рекомендациям фирмы-производителя, лиофилизированный порошок разводили 8 мл стерильного 0,9% раствора натрия хлорида без консервантов (1 мл полученного раствора содержит 12,5 ЕД ботокса). Использовали трансперинеальную методику введения препарата. У мужчин под контролем указательного пальца, введенного в прямую кишку, специальную иглу с изоляционным покрытием вводили в точку, находящуюся на 2 см латеральнее и выше анального отверстия (рис. 2). У женщин иглу под контролем указательного пальца, введенного во влагалище, вводили в точку на 1 см латеральнее и выше наружного отверстия уретры на глубину 1,5–2,0 см (рис. 3). Во всех случаях положение иглы контролировали электромиографически по характерному звуку динамика электромиографа. В каждую точку вводили по 50 ЕД ботокса.
 |
| Рисунок 3. Введение ботулинического токсина у женщин |
У всех больных через 10 дней после введения ботулинического токсина исчезла остаточная моча и было отмечено увеличение максимальной скорости потока мочи. Важно, что хемоденервация сфинктера уретры после инъекции ботокса у всех пациентов с нерасслабляющимся п/п сфинктером и наружной ДСД приводила к снижению детрузорного давления, а у больных с нарушением сократительной способности детрузора — к снижению максимального абдоминального давления, вызывающего выделение мочи из наружного отверстия уретры. Это наблюдение представляется крайне важным в отношении профилактики развития пузырно-мочеточникового рефлюкса и сохранения функциональной способности почек. Только у одного больного клинический эффект после инъекции ботокса продолжал сохраняться на протяжении 16 мес, остальным пациентам потребовались повторные инъекции препарата с периодичностью 3–8 мес.
В отдельных случаях, при выраженной инвалидизации больных с нарушением опорожнения мочевого пузыря, используют трансуретральную инцизию или резекцию наружного сфинктера уретры, дренируют мочевой пузырь постоянным уретральным катетером или выполняют цистостомию.
Таким образом, нарушение опорожнения мочевого пузыря может быть следствием различных форм дисфункции нижних мочевых путей. Требуются проведение комплексного уродинамического обследования для уточнения функционального состояния мочевого пузыря и его сфинктеров и выбор адекватного метода опорожнения мочевого пузыря. Отсутствие высокоэффективных и универсальных способов лечения больных с функциональными нарушениями опорожнения мочевого пузыря диктует необходимость поиска новых методов терапии таких больных.
Г. Г. Кривобородов, доктор медицинских наук
М. Е. Школьников, кандидат медицинских наук
РГМУ, Москва
Источник