Недержание мочи при травме таза
Оперативное лечение последствий повреждений костей таза и нижних мочевыводящих путей — одна из сложных и наименее разработанных проблем современной хирургии, травматологии и урологии. Большое количество неудовлетворительных результатов лечения больных с данной патологией является следствием неоправданного применения консервативного лечения и неудачных оперативных вмешательств. Количество пациентов с данным видом травмы из года в год постоянно увеличивается, что связано в первую очередь с ростом транспортного травматизма.
Ситуация усугубляется отсутствием четко разработанной схемы обследования и оказания совместной квалифицированной медицинской помощи урологами и травматологами этой группе пациентов. При этом одной из главных проблем при оперативном лечении в этом случае данной группы пациентов является правильный и научно обоснованный выбор травматологами и урологами не только того или иного оперативного пособия, но и последовательности выполнения урологического и/ или травматологического этапов.
Несомненная социальная значимость и актуальность этой проблемы побудила нас создать совместную группу, состоящую из травматологов и урологов ведущих учреждений России — ЦИТО им. Н.Н. Приорова и НИИ урологии Минздравсоцразвития РФ. Основной задачей созданной группы была разработка алгоритма обследования пациентов с сочетанными застарелыми травмами таза и уретры и выработка наиболее адекватной лечебной тактики, включая этапность оперативного лечения.
Абсолютное большинство повреждений таза в результате переломов костей, разрывов фиброзно-хрящевых структур сочленений характеризуется нарушением непрерывности и стабильности тазового кольца и относится к категории дезинтегрирующих повреждений. В большинстве случаев отмечается множественный характер повреждений таза — возникновение нескольких травматических очагов в одном или разных анатомических отделах (переднее полукольцо, заднее полукольцо, вертлужная впадина). По данным ЦИТО повреждения органов мочевыделительной системы при таких травмах составляют 45 % всех сочетанных повреждений, причем в половине случаев они характеризуются нарушением анатомической целостности органов — разрывом почек (8,3%), мочевого пузыря (25%), уретры и мочевого пузыря (4,2% всех повреждений органов мочевыделительной системы) [1].
Преобладающей причиной образования стриктуры уретры в настоящее время является последствия травмы мочеиспускательного канала. Закрытые повреждения мочеиспускательного канала в мирное время, как правило, бывают следствием транспортного и промышленного травматизма, реже — бытового, в военное время — результатом насыщенности современной армии техникой и применения оружия, обладающего большой разрушительной силой [2-5]. При травматическом повреждении уретры полный ее разрыв наблюдается в 65% наблюдений, частичный — в 35% [6].
В 68-84% причиной повреждения заднего отдела уретры является автомобильная травма, в 25-60% — падение на промежность [4, 5, 7]. По данным Palmer J.K. et al. переломы костей таза сочетаются с повреждением уретры в 10% наблюдений [8]. В свою очередь, практически все повреждения мембранозного отдела уретры, вызванные тупой травмой, сочетаются с повреждением костей таза. Кроме того, по данным Carlin B.I. et al. повреждение уретры сочетается с травмой мочевого пузыря в 10-20% [9]. Повреждения тазовых органов чаще всего встречаются у лиц в возрасте до 30 лет [10]. По данным Perry M.O. и Husmann D.A. повреждения уретры при травме таза у женщин встречается в 1-6% наблюдений, они обусловлены воздействием костных отломком и часто сочетаются с повреждениями прямой кишки (30%) и влагалища (75%) [11, 12].
Повреждения переднего отдела уретры у мужчин встречаются в три раза реже, чем повреждения заднего ее отдела, что связано с анатомическими особенностями отдела уретры, в частности высокой подвижностью висячего отдела уретры [13]. Травмы переднего отдела уретры составляют лишь 10% из всех повреждений нижних мочевыводящих путей [14]. Основной причиной повреждений переднего отдела уретры является тупая травма или проникающее ранение. При тупой травме промежности в 85% случаев повреждается бульбозный отдел уретры [15]. Причиной этого является анатомическая фиксация данного отдела уретры к лобковым костям и ее сдавление между ними и травмирующим предметом. В отличие от повреждений заднего отдела уретры, которые очень часто сочетаются с повреждениями других органов, травма переднего отдела уретры чаще бывает изолированной. Более того, травма переднего отдела уретры часто остается незамеченной пациентами, и они обращаются за медицинской помощью через несколько месяцев с жалобами на затруднение мочеиспускания из-за развития стриктуры [16].
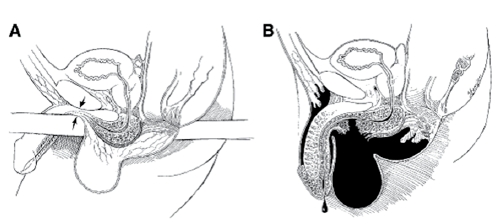 |
| Рисунок 1. Механизм повреждения передней уретры при тупой травме. |
| А — Повреждение уретры вследствие сдавления между предметом и лобковым симфизом. В — Мочевые затеки вследствие повреждения передней уретры |
Механизм и локализация травмы передней уретры и пути распространения мочевых затеков при ее повреждении представлены на рисунке 1.
Анатомо-физиологической особенностью тазового кольца является его жесткость, что позволяет удерживать тело в вертикальном состоянии. Кости тазового кольца отличаются малой подвижностью и большой прочностью, способны выдерживать давление массой от 200 до 1115 кг. Жесткость тазового кольца обеспечивается за счет сухожильного и связочного аппаратов. Менее прочно лонно-седалищное сочленение, составляющее переднее полукольцо. Более прочными характеристиками обладают крестцово-повздошные сочленения (заднее полукольцо).
Особенностью связочного аппарата костей таза является то, что при травме со смещением костей по плоскости более 2-3 мм происходят различные необратимые повреждения связочного аппарата переднего и/или заднего полукольца. Поэтому при различных переломах костей таза почти всегда повреждается и связочный аппарат переднего и/или заднего полукольца.
Внутри тазового кольца равномерно и индивидуально «растянут», в зависимости от конфигурации таза, мембранозный отдел уретры, состоящий из мышечно-фасциальных образований. Тазовый отдел диафрагмы анатомически располагается внутри малого таза, спереди прикрепляется к внутренним поверхностям лонно-седалищных костей, а сзади — к крестцу. За счет этого тазовые органы удерживаются от выпадения. Через тазовый отдел диафрагмы проходит уретральный канал, который располагается в непосредственной близости от переднего полукольца таза (рисунок 2).
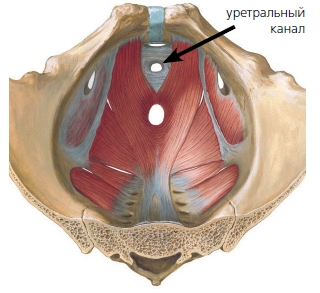
Рисунок 2. Тазовое кольцо мочеполовой диафрагмы у мужчин
Протяженность мембранозного отдела уретры составляет 1-1,5 см, толщина стенки уретры — 0,15 мм. Этот отдел является наружным сфинктером уретры, отвечающим за удержание мочи. Именно тесное анатомо-топографическое расположение мембранозного отдела уретры внутри тазового кольца при травмах таза с повреждением переднего его полукольца приводит часто к различным повреждениям в области этого отдела уретры. У мужчин с обеих сторон от нижних поверхностей седалищных костей располагаются кавернозные тела и поэтому, как правило, при травмах переднего полукольца таза повреждается не только уретральный канал, но и кавернозные тела, что приводит к различным формам нарушений эректильной функции [8, 10].
При травме таза нарушается конфигурация тазового кольца, меняется степень натяжения тазового отдела диафрагмы, особенно это выражено на стороне повреждения. Внешний удар в область костей таза может быть причиной деформаций тазового отдела диафрагмы. Травма и возникновение болевого синдрома приводят к резкому сокращению тазового отдела диафрагмы в противоположную сторону от нанесенного внешнего воздействия, что приводит к различным нарушениям мочеиспускательного канала. Степень и характер повреждения мембранозного отдела уретры (от надрыва до разрыва) зависят от силы, скорости сокращения тазового отдела диафрагмы и степени повреждения и смещения костей таза. Протяженность и локализация различных повреждений тазового отдела диафрагмы зависят от механизма и места повреждения. При различных переломах костей таза, и особенно переднего полукольца, наиболее часто повреждаются мембранозный и/или бульбозный отдел уретры. На рисунке 3 представлен механизм нарушения целостности костных структур таза и повреждения тазовой диафрагмы фиксированной к этим структурам.
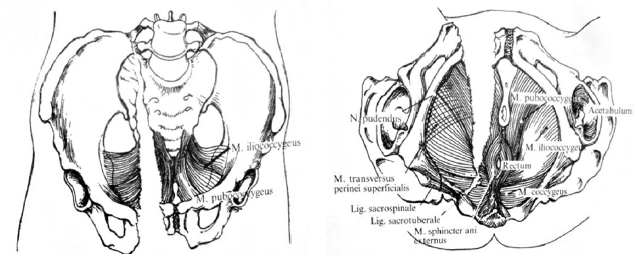
Рисунок 3. Механизм повреждения мочеполовой диафрагмы при травме костей таза (переднего полукольца) в прямой и задней проекции
Застарелые переломы костей таза, сочетающиеся с повреждениями уретры, относятся к наиболее сложным в оперативном смысле вмешательствам. Это, в первую очередь, связано с тем, что выполнение различных уретропластик с целью восстановления самостоятельного мочеиспускания в некоторых случаях бывает невозможно из-за выраженных различных посттравматических деформаций костей таза.
Сочетанная или комбинированная политравма относится к разряду наиболее тяжелых и, как правило, сопровождается не только с повреждениями костей таза и уретры, но и поражением жизненно важных органов — головного мозга, позвоночника, органов брюшной полости и т. д. Поэтому в остром периоде при поступлении пациентов в стационар в состоянии шока и кровотечения, угрожающих жизни, медицинская помощь направлена на спасение пострадавшего. Оценке степени выраженности травматологических и урологических повреждений на этом этапе уделяется минимальное внимание, если нет повреждений тазовых органов, требующих ушивания и дренирования. При поступлении в стационар пациентов с травмами таза и нарушением самостоятельного мочеиспускания или различной степени уретроррагии урологи ограничиваются установкой эпицистостомы с целью дренирования мочевого пузыря. При поступлении таких пациентов в травматологические отделения травматологи ограничиваются консервативным лечением — постельный режим и вынужденное положение на спине на 1,5-3 месяца. На этом этапе мало кто из специалистов обращает необходимое внимание на характер и степень повреждений костей таза и органов мочеполовой системы [2, 4, 17, 18].
Именно это в большинстве наблюдений становится основной причиной неудач различных видов уретропластики и возникающих после нее осложнений. К осложнениям уретропластики в этих ситуациях относится формирование рецидивных стриктур и облитераций, образование свищей различных локализаций. При восстановлении проходимости мочеиспускательного канала после уретропластики могут возникнуть такие осложнения, как различные формы недержания мочи, связанные с повреждением мембранозного отдела уретры, а также развитие ретроградной эякуляции при повреждении шейки мочевого пузыря.
Эти осложнения могут быть связаны как с выраженными посттравматическими деформациями костей таза, так и с отсутствием проведения необходимого обследования на предоперационном этапе для получения полноценной информации о состоянии больного, как травматологами, так и урологами.
Различные застарелые травматические деформации тазового кольца, как правило, сочетаются с переломами переднего полукольца со смещением и/или наличием отломков в проекции мочеиспускательного канала и/или передней стенки мочевого пузыря. Как правило, повреждение уретры при травме таза возникает в области бульбо-мембранозного отдела. Один из факторов повреждения уретры связан со смещением костных фрагментов таза в проекцию мочеиспускательного канала, что может приводить к частичному или полному сдавливанию или/и повреждению уретры с формированием в дальнейшем ее стриктуры или/и облитерации или свища. На рисунке 4 представлена совмещенная антеградная фиброцистоуретрография с ретроградной уретрографией в прямой проекции с неправильно сросшимся переломом седалищной кости слева, посттравматической облитерацией уретры и цистостомой. На снимке определяются множественные остеофиты, механическое сдавление уретры, а в проксимальной части бульбозного отдела уретры определяется облитерация уретры. Убедительно судить о наличии костных фрагментов в проекции облитерации уретры не представляется возможным. При выполнении компьютерной томографии костей таза с уретроцистографией, у этого пациента определяется механическое сдавление уретры фрагментом седалищной кости (рисунок 5).
У мужчин повреждение переднего полукольца таза и седалищных костей, особенно со смещением, часто приводит к эректильной дисфункции. Причинами этого могут быть повреждения кавернозных тел у мест прикрепления к костям таза, нарушение иннервации и повреждение сосудов полового члена.
Таким образом, осложнения после травмы таза у мужчин и женщин клинически проявляются не только различными нарушениями опорнодвигательного аппарата, но различными расстройствами мочеиспускания от острой его задержки до тотального недержания мочи. Неэффективность неоднократных попыток уретропластики в дальнейшем может привести к необходимости пожизненного дренирования мочевого пузыря цистостомой. При возникновении недержания мочи она может быть устранена установкой искусственного сфинктера мочевого пузыря или слинговой операцией, как у мужчин, так и у женщин. Серьезными осложнениями травмы таза у мужчин является нарушение потенции (эректильная дисфункция) и/или возникновение ретроградной эякуляции, что приводит к бесплодию. В связи с увеличением количества сочетанных травм костей таза и мочевыводящих путей последние годы резко увеличилось число инвалидов и количество разводов в этой группе пациентов.
Таким образом, серьезные осложнения со стороны нижних мочевых путей в результате травмы таза вызывают необходимость разработки и внедрения в практику травматологов и урологов алгоритма диагностики и лечения этих тяжелых осложнений не только для их лечения, но и для социальной адаптации пострадавшего.
Ключевые слова: травма костей таза, травма уретры, стриктура уретры, механизм повреждения уретры при травме.
Keywords: pelvic trauma, urethra trauma, urethral stricture, mechanism of urethral injury in pelvic trauma.
ЛИТЕРАТУРА
- Травматология. Национальное руководство / Под ред. Котельников Г.П., Миронов С.П. М. ГЭОТАР-Медиа. 2008.
- Pokorny M., Pontes J.E., Pierce J.M. Jr. Urological injuries associated with pelvic trauma // J Urol. 1976. Vol. 121. P. 455-457.
- Flaherty J.J., Kelley R., Burnett B., Bucy J., Surian M., Schildkraut D., Clarke B.G. Relationship of pelvic bone fracture patterns to injuries of urethra and bladder // J Urol. 1968. Vol. 99. P. 297-300.
- Fallon B., Wendt J.C., Hawtrey C.E. Urological injury and assessment in patients with fractured pelvis // J Urol. 1984. Vol. 131. P. 712-714.
- Шевцов И.П., Глухарев А.Г. Повреждения органов мочеполовой системы. Л. 1972. С. 101-159.
- Webster G.D. Perineal repair of membranous urethral stricture // Urol Clin North Am. 1989. Vol. 16. P. 303-312.
- Koraitim M.M. Pelvic fracture urethral injuries: evaluation of various methods of management // J Urol. 1996. Vol. 156. № 4. P. 1288-1291.
- Palmer J.K., Benson G.S., Corriere J.N. Jr. Diagnosis and initial management of urological injuries associated with 200 consecutive pelvic fractures // J Urol. 1983. Vol. 130. P. 712-714.
- Carlin B.I., Resnick M.I. Indications and techniques for urologic evaluation of the trauma patient with suspected urologic injury // Semin Urol. 1995. Vol. 13. № 1. P. 9-24.
- Mundy A.R. Pelvic fracture injuries of the posterior urethra // World J Urol. 1999. Vol. 17. № 2. P. 90-95.
- Perry M.O., Husmann D.A. Urethral injuries in female subjects following pelvic fractures // J Urol. 1992. Vol. 147. № 1. P. 139-143.
- Venn S.N., Greenwell T.J., Mundy A.R. Pelvic fracture injuries of the female urethra // BJU Int. 1999. Vol. 83. № 6. P. 626-630.
- Chapple C.R. Urethral injury // BJU Int. 2000. Vol. 86. № 3. P. 318-326.
- Morey A.F., McAninch J.W. Reconstruction of traumatic posterior urethral strictures // Tech Urol. 1997. Vol. 3. № 2. P. 103-107.
- Armenakas N.A., McAninch J.W. Acute anterior urethral injuries: diagnosis and initial management / In: McAninch J.W., editor. Traumatic and reconstructive urology. Philadelphia: W.B. Saunders; 1996. p. 54.
- Hernandez J., Morey A.F. Anterior urethral injury // World J Urol. 1999. Vol. 17. № 2. P. 96-100.
- Morey A.F., Hernandez J., McAninch J.W. Reconstructive surgery for trauma of the lower urinary tract // Urol Clin North Am. 1999. Vol. 26. № 1. P. 49-46.
- Christopher M. Dixon, M.D. Diagnosis and Acute Management of Posterior Urethral Disruptions / In: McAninch J.W., editor. Traumatic and reconstructive urology. Philadelphia: W.B. Saunders; 1996. Р. 347-357.
Источник
Нейрогенные расстройства мочеиспускания при травме позвоночника и спинного мозга: взгляд невролога и уролога
Статья посвящена проблеме нейрогенных расстройств мочеиспускания при травме позвоночника и спинного мозга
Путь пациента с осложненной травмой позвоночника, т. е. сопровождающейся повреждением спинного мозга, начинается с нейрохирургического оперативного вмешательства и продолжается многоэтапной реабилитацией, направленной на коррекцию сопутствующих осложнений и восстановление утраченных функций организма [1]. Для таких больных есть специфический термин — «спинальные».
Одним из тяжелейших последствий травмы спинного мозга является расстройство произвольного мочеиспускания, обусловленное нарушением проводимости спинномозговых путей. По данным М.Р. Касаткина, подобное осложнение встречается в 92,1% случаев закрытых повреждений спинного мозга [2]. Патогенез изменений функции нижних мочевых путей при травме спинного мозга, проявляющийся в утрате рефлекторной деятельности, сложен и многообразен [3].
Механизм нормального мочеиспускания и характер его расстройства у спинальных пациентов напрямую связаны с особенностями физиологии этой области. Периферическую иннервацию нижних мочевых путей осуществляют тазовый нерв, представляющий парасимпатическую нервную систему, гипогастральный нерв, реализующий симпатическую регуляцию, и пудендальный соматический нерв. Афферентную информацию несут волокна всех трех нервов — вегетативных от детрузора (гладкой мышцы мочевого пузыря) и уретры и полового нерва от тканей промежности. Первичным анализатором для парасимпатического тазового нерва являются нейроны сакрального центра мочеиспускания, расположенного на уровне S2‒S4 сегментов спинного мозга. Здесь же, в анатомическом соседстве, находится ядро Онуфа, представляющее собой скопление нервных клеток, аксоны которых образуют пудендальный нерв [4]. Симпатическая афферентная иннервация, опосредованная гипогастральным нервом, являющимся частью подчревного и поясничного сплетения, осуществляется через пограничный симпатический ствол и вставочные интернейроны боковых рогов спинного мозга на уровне его Th20‒L2 сегментов. Эти же нервы несут и эфферентные сигналы к иннервируемым органам. Регулирующие структуры спинного мозга связаны с вышерасположенными центрами иннервации проекционно, а также с помощью нейрогуморальных и рефлекторных механизмов [5]. Однако следует отметить, что концепции регуляции функции нижних мочевых путей в норме и патологии являются в большей степени эмпирическими, и единого понимания этого вопроса на сегодняшний день нет.
Клиническая картина
Врачу-неврологу, курирующему пациента с осложненной травмой позвоночника, необходимо оценить уровень и степень повреждения спинного мозга и учесть посттравматические сроки. Клиническая картина в острый и ранний периоды после получения травмы обусловлена спинальным шоком, что проявляется арефлексией и задержкой мочи. По мере восстановления можно наблюдать активизацию рефлекторной деятельности и формирование «в сухом остатке» нейрогенного расстройства мочеиспускания. При повреждении спинного мозга на уровне сакрального центра мочеиспускания и периферических нервных волокон развивается атония или гипотония детрузора, при этом за счет интактности симпатических структур иннервации внутренний уретральный сфинктер сохраняет сократительную способность. Таким образом, нарушается взаимосвязь симпатических и парасимпатических влияний [6]. Клинически наблюдается нейрогенная задержка мочеиспускания с элементами парадоксальной ишурии (выделения мочи по каплям на фоне переполненного мочевого пузыря). При локализации травмы выше сакрального центра и ядра Онуфа повреждаются проводниковые нервные волокна, осуществляющие взаимосвязь регулирующих структур, однако сами центры иннервации могут быть интактны. В этом случае и детрузор, и внутренний сфинктер уретры способны к циклическому сокращению и расслаблению, но рассогласованность в работе приводит не к нормальному акту мочеиспускания, а к детрузорно-сфинктерной диссинергии. Поражение на уровне нижнегрудного и верхнепоясничного отделов позвоночника, вовлекающее симпатические регулирующие структуры, вызывает нарушение сократительной способности внутреннего сфинктера уретры и недержание мочи. Травма спинного мозга на уровне шейного и верхнегрудного отделов позвоночника ведет к прерыванию взаимосвязи спинальных и стволовых, а также кортикальных структур регуляции. В ситуации, когда центры иннервации спинного мозга и нервные проводники между ними сохраняют свою анатомическую целостность, клинически может сформироваться автономный процесс мочеиспускания, а также гиперактивность мочевого пузыря. В этом случае накопление и выделение мочи происходят рефлекторно, в т. ч. с участием аксон-рефлексов, без контроля центров, отвечающих за произвольную составляющую физиологического процесса [7].
Описанные клинические нарушения достаточно вариабельны и зависят от характера и тяжести повреждения, а также сроков, прошедших с момента травмы, поэтому можно наблюдать переход одной формы нейрогенного расстройства мочеиспускания в другую.
Невролог, понимая обусловленность клинической картины уровнем поражения спинного мозга, определяет тактику ведения спинального пациента и дальнейший прогноз. Осуществление адекватной коррекции урологических осложнений лежит, несомненно, в междисциплинарной плоскости. В связи с этим нейроурологическая практика, а вернее, четкое и скоординированное взаимодействие невролога и уролога способно обеспечить квалифицированную и своевременную помощь. И если врач-невролог сосредоточен на повреждении спинного мозга и нарушении иннервации, то уролог контролирует непосредственное функциональное состояние нижних мочевых путей и коррекцию сопутствующих воспалительных и нефротических осложнений. Отсюда вытекает необходимость тесной взаимосвязи специалистов для полноценной коррекции нейрогенных расстройств мочеиспускания.
В представлении уролога, оказывающего специализированную помощь пациентам с неврологическими расстройствами, процесс мочеиспускания выглядит несколько сложнее, чем простой циклический акт, состоящий из чередования фаз накопления и выведения мочи, обеспеченный двумя основными функциями мочевого пузыря: резервуарной и эвакуаторной. Функционально этот процесс определяется синергией детрузора с гладкомышечным сфинктером уретры и мышцами тазового дна, включающими наружный уретральный сфинктер.
Физиологически мочевой пузырь, природой созданный резервуар для сбора мочи, обладает способностью к полному опорожнению в подходящее время и в удобном для совершения акта мочеиспускания месте согласно социально-поведенческим нормам. Эта крайне важная способность реализуется в результате сложной регуляции с участием центральной и периферической нервных систем. Фундаментально акт мочеиспускания — это спинальный рефлекс, обеспечиваемый работой центров головного мозга, реализация и подавление этого рефлекса находятся под волевым контролем. Возможность произвольного управления делает функцию нижних мочевых путей уникальной по сравнению, например, с сердечно-сосудистой системой, и в то же время более уязвимой при неврологических заболеваниях [8]. Таким образом, основными функциями нижних мочевых путей являются накопление мочи в мочевом пузыре, длящееся относительно продолжительное время, и мочеиспускание, занимающее в норме несколько секунд. Реципрокные отношения — расслабление/напряжение детрузора, закрытие уретрального сфинктера и сокращение/расслабление детрузора, открытие уретрального сфинктера — обеспечивают скоординированность процессов накопления и удаления мочи и находятся под нейромедиаторным контролем [9].
Нейрогенная дисфункция нижних мочевых путей является следствием патологии центральной нервной системы или периферических нервных окончаний ‒ отделов нервной системы, выполняющих контроль над актом мочеиспускания. В этом состоит главное отличие рассматриваемого нарушения от нарушений нижних мочевых путей ненейрогенной этиологии, развивающихся вследствие поражения непосредственно мочеполовой системы.
В урологическом сообществе длительное время основной опорой для определения формы нейрогенного расстройства мочеиспускания являлась классификация, предложенная профессором Г. Мадерсбахером в 1980 г. и рекомендуемая Европейской ассоциацией урологов (рис. 1) [10]. В ней автор выделяет 8 основных форм нейрогенных расстройств мочеиспускания в зависимости от состояния детрузора и внутреннего сфинктера уретры. Подразумевается, что указанные структуры могут быть в гипертонусе, гипотонусе и в нормальном состоянии. Однако сложность в постановке диагноза и категоричность в выборе одной из 8 форм нарушений мочеиспускания сегодня заставляют говорить о пересмотре форм расстройств мочеиспускания. С клинической точки зрения все возможные виды нарушений мочеиспускания рассмотреть в рамках одной из существующих классификаций невозможно. В определении поражения у пациента наиболее часто специалисты основываются на преобладающем нарушении эвакуаторной или резервуарной функции мочевого пузыря, различных видах детрузорно-сфинктерной диссинергии и уродинамических показателях максимального детрузорного давления в точке утечки. При этом важность знания о максимальном детрузорном давлении и максимальном давлении в точке утечки делает необходимым проведение специализированного уродинамического исследования практически каждому пациенту с нарушениями мочеиспускания на фоне неврологического заболевания.
Лечение
Основными задачами урологической помощи на всех этапах нейрореабилитации являются:
1) сохранение и обеспечение функции верхних мочевыводящих путей;
2) независимость регуляции функции нижних мочевыводящих путей;
3) улучшение качества жизни.
С практической точки зрения важны борьба с вторичными осложнениями нейрогенной дисфункции мочеиспускания, а также их профилактика. К таким осложнениям относятся манифестация инфекции мочевыводящих путей (исключая бессимптомную бактериурию), уролитиаз, микроцистис, гидронефротическая трансформация и почечная недостаточность, стриктура уретры и т. д. [11].
Наименьшего риска осложнений со стороны верхних мочевыводящих путей следует ожидать при сохранении резервуарной функции мочевого пузыря с низким внутрипузырным давлением, например при гипотонии детрузора, его достаточной функциональной емкости и нормальном состоянии поперечно-полосатого сфинктера уретры или его гипотонии. В этом случае к хорошим результатам коррекции, в т. ч. улучшению качества жизни спинального пациента, приводит адекватное дренирование нижних мочевых путей, при этом следует руководствоваться международными стандартами и отечественными клиническими рекомендациями. При нарушении функции опорожнения мочевого пузыря вследствие повреждения позвоночника и спинного мозга методом выбора является асептическая периодическая катетеризация. Она подразумевает использование одноразового стерильного лубрицированного катетера. Процедура выполняется самостоятельно или с посторонней помощью каждые 4‒6 ч [12].
Иные методы дренирования мочевого пузыря, такие как приемы Креде или Вальсальвы, длительное использование постоянного мочевого катетера, должны быть строго обоснованы, т. к. несут значительные риски развития вторичных нейрогенных осложнений работы мочевого пузыря, достигающих 34% [13].
Периодическая катетеризация 4‒6 раз в сутки при условии отсутствия выраженных нарушений со стороны верхних мочевыводящих путей, шокового состояния, гнойно-инфекционных процессов в уретре и мочевом пузыре может быть назначена любым специалистом, курирующим пациента. Вопрос о том, когда переводить пациента на периодическую катетеризацию для постоянного уретрального дренажа, находится в стадии обсуждения сообщества специалистов по нейроурологии [14]. Формальных ограничений и четких рекомендаций по срокам нет, однако считается, что при отсутствии противопоказаний и достаточной укомплектованности отделения средним и младшим медицинским персоналом следует избавлять пациента от постоянных дренажей как можно раньше.
Гиперактивный мочевой пузырь, встречающийся на фоне детрузорно-сфинктерной диссинергии и без нее, является другой формой нейрогенного расстройства мочеиспускания вследствие травмы позвоночника и спинного мозга. Если такой тип нарушения клинически проявляется недержанием мочи, то он не несет значительного риска осложнений со стороны верхних мочевыводящих путей. К проблемам нейрогенного гиперактивного мочевого пузыря следует отнести снижение качества жизни.
Детрузорно-сфинктерная диссинергия характеризуется тем, что в момент напряжения мочевого пузыря для его опорожнения происходят различные по силе и продолжительности сокращения внутреннего и наружного сфинктеров уретры, обеспечивающих функцию удержания. В норме сокращения детрузора синхронны с расслаблением этих сфинктеров, что способствует свободному выведению мочи по уретре. Нарушение функции опорожнения в сочетании с высоким внутрипузырным давлением ‒ наиболее опасная форма нейрогенной дисфункции мочеиспускания из-за развития пузырно-мочеточникового рефлюкса, а также возможности структурных повреждений самого мочевого пузыря. В этом случае перед урологом стоят две основные задачи: 1) подавление высокого внутрипузырного давления, 2) обеспечение оттока мочи по уретре.
Для подавления детрузорной гиперактивности в качестве первой линии терапии применяются антихолинергические средства, в дополнение к которым можно назначать препараты из группы бета-3-адреномиметиков [15]. Вторая линия лечения включает инъекционное введение в стенку мочевого пузыря 200 ЕД ботулинического нейропептида. Надо понимать, что терапия направлена на создание низкого внутрипузырного давления в мочевом пузыре, необходимого для нормальной работы верхних мочевых путей. Одним из результатов купирования гиперактивности, особенно при сохранении нормального или повышенного тонуса поперечно-полосатого сфинктера уретры, будет увеличение количества остаточной мочи или отсутствие мочевыделения. Поэтому крайне важно объяснить пациенту необходимость проведения указанной терапии с назначением периодической катетеризации мочевого пузыря.
При своевременной коррекции нарушений мочеиспускания у спинальных пациентов, применении рекомендованного метода отведения мочи, компенсации избыточного внутрипузырного давления вследствие гиперактивности детрузора или детрузорно-сфинктерной диссинергии удается избежать многих вторичных осложнений.
В комплексной программе реабилитационного лечения пациентов с травмой позвоночника и спинного мозга используются методики немедикаментозной коррекции, показавшие различный терапевтический потенциал в ходе исследований. В частности, применение электростимуляции мочевого пузыря с помощью имплантируемых электродов в работе А.В. Лившица и соавт. показало, что создать управляемый акт мочеиспускания невозможно, т. к. возбуждение детрузора распространяется на внутренний сфинктер уретры, моделируя детрузорно-сфинктерную диссинергию [16]. Несмотря на то что исследователи представили некоторые положительные результаты, методика не нашла клинического применения в связи с высокой инвазивностью и риском вторичных осложнений.
Применение электростимуляции переменным пульсирующим током по лонно-сакральной методике и электрофореза с прозерином на передней брюшной стенке в проекции мочевого пузыря в настоящий момент представляется несостоятельным вследствие особенностей физиологии нижних мочевых путей и неучастия мышц живота в акте мочеиспускания.
Перспективно использование современных методик: сакральной инвазивной электронейростимуляции с помощью имплантируемых электродов и ритмической периферической магнитной стимуляции в области сакрального центра мочеиспускания и крестцовых корешков [17, 18]. В настоящее время механизм действия магнитной стимуляции на физиологию нижних мочевых путей остается неясным. Многоступенчатость и сложность нервной регуляции процесса удержания мочи и акта мочеиспускания предполагают возможность вовлечения различных структур в ответ на внешнее воздействие. Клинические и уродинамические эффекты магнитной стимуляции, вероятно, связаны с восстановлением интеграции регуляторных рефлексов, при этом наблюдается эффект нейромодуляции, когда происходит изменение активности (торможение или возбуждение) структур центральной, периферической и вегетативной нервных систем [19, 20].
Нейрогенное нарушение мочеиспускания, обусловленное травмой позвоночника и спинного мозга, клинически чрезвычайно гетерогенно вследствие вариабельности уровня и степени тяжести поражения [21, 22]. Этот аспект диктует необходимость индивидуального диагностического подхода, выбора адекватного метода коррекции работы нижних мочевых путей. Реабилитационный путь спинального пациента в настоящее время невозможно представить без тесного сотрудничества невролога и уролога. Совместный современный подход специалистов к проблеме урологических осложнений травмы спинного мозга обеспечивает пациенту верное понимание собственного состояния и адекватную прогностическую оценку, а также возможность социальной адаптации и повышения качества жизни [23, 24].
Источник