Как происходит развитие мочевого пузыря
Содержание статьи
Развитие мочевых и половых (мочеполовых) органов.
Оглавление темы «Развитие мочевых и половых ( мочеполовых ) органов.»:
1. Развитие мочевых и половых ( мочеполовых ) органов.
2. Аномалии органов мочеотделения. Аномалии матки, труб и влагалища.
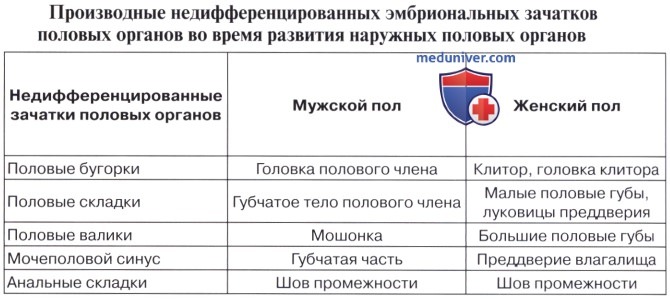
3. Развитие наружных половых органов.
Развитие мочевых и половых (мочеполовых) органов
Понимание гомологии строения мужских и женских половых органов, так же как и истолкование наблюдавшихся иногда аномалий и уродств, возможно лишь при ознакомлении с основными фактами развития мочевой и половой систем. Мочевая и половая системы в своем развитии тесно связаны друг с другом, и их выводные протоки открываются в общий мочеполовой синус, sinus urogenitalis. При этом мочевая система имеет ту особенность, что она не развивается из одного зачатка, постепенно растущего и усложняющегося, а представлена рядом морфологических образований, последовательно сменяющих друг друга (головная почка, первичная почка, постоянная почка).
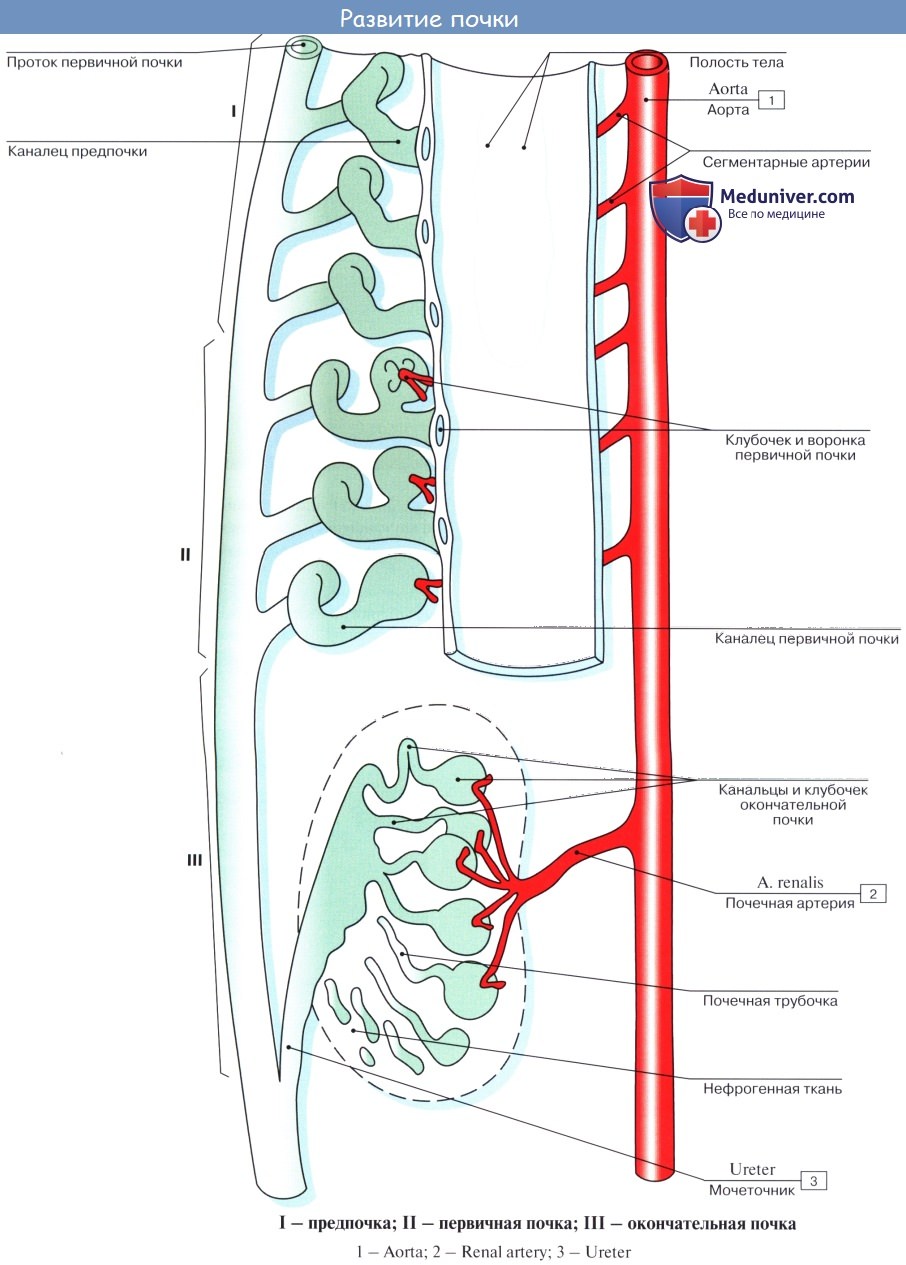
К морфологическим образованиям, принимающим участие в развитии мочеполовых органов, относятся следующие.
1. Головная почка, или предпочка, pronephros. У человека и высших позвоночных она уже у зародыша быстро исчезает, заменяясь более важной первичной почкой.
2. Первичная почка, mesonephros, и ее проток, ductus mesonephricus. Ductus mesonephricus является самым ранним из образований, идущих на постройку мочеполовых органов. На 15-й день он появляется в мезодерме в виде нефротического тяжа на медиальной стороне полости тела (celom), а на 3-й неделе в нем образуется полость и проток достигает клоаки. Mesonephros состоит из ряда поперечных канальцев, расположенных медиально от верхнего отдела мезонефрального протока и одним концом впадающих в этот последний, тогда как другой конец каждого канальца оканчивается слепо. Mesonephros является первичным секреторным органом, выводным протоком служит мезонефральный проток.
3. Ductus paramesonephricus. В конце 4-й недели вдоль наружной стороны каждой первичной почки появляется продольное утолщение брюшины вследствие развития здесь эпителиального тяжа. В начале 5-й недели тяж превращается в проток. Своим краниальным концом ductus paramesonephricus открывается в полость тела несколько кпереди от переднего конца первичной почки. В отличие от ductus mesonephricus, открывающихся каждый особо, ductus paramesonephricus своим каудальным концом, подходя к sinus urogenitalis, соединяется по средней линии с соименным протоком.
4. Половые железы. Они развиваются сравнительно позднее в виде скопления зародышевого эпителия с медиальной стороны mesonephros. Семенные трубочки яичка и содержащие яйца фолликулы яичника развиваются из зародышевых эпителиальных клеток. От нижнего полюса половой железы тянется вниз по стенке брюшной полости соединительнотканный тяж, gubernaculum testis, который своим нижним концом уходит в паховый канал.
Окончательное формирование мочеполовых органов происходит следующим образом. На смену первоначальных почек начинают образовываться постоянные почки, metanephros, из того же нефрогенного тяжа, из которого образовалась первичная почка. Из нефрогенного тяжа развивается собственно паренхима постоянных почек (мочевые канальцы). Начиная с 3-го месяца, постоянные почки заменяют собой mesonephros как функционирующие выделительные органы.
Так как туловище растет книзу более быстро, то почки как бы передвигаются кверху и занимают свое место в поясничной области.
Лоханка и мочеточник развиваются из дивертикула каудального конца мезонефрального протока (в начале 4-й недели); каудальный конец дивертикула отделяется от мезонефрального протока и впадает в ту часть клоаки (sinus urogenitalis), из которой развивается дно мочевого пузыря, куда и открываются мочеточники.
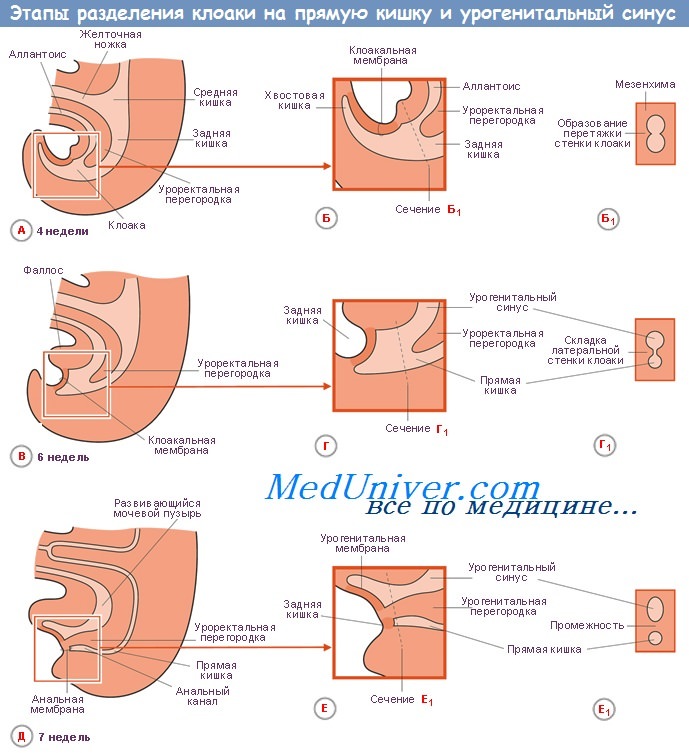
Развитие мочевого пузыря связано с преобразованием клоаки
Клоака — это общая полость, куда первоначально открываются мочевые, половые пути и задняя кишка. Она имеет вид слепого мешка, закрытого снаружи клоакальной перепонкой, membrdna cloacalis. В дальнейшем внутри клоаки возникает фронтальная перегородка, membrdna urorectdle, которая делит клоаку на 2 части: вентральную — sinus urogenitalis и дорсальную — rectum.
После прорыва membrana cloacalis обе эти части открываются наружу двумя отверстиями: sinus urogenitalis — передним (отверстие мочеполовой системы), и rectum — задним проходом (anus).
С мочеполовым синусом связан мочевой мешок, allantbis, который у низших позвоночных служит резервуаром для продуктов выделения почек, а у человека часть его превращается в мочевой пузырь.
Аллантоис состоит из 3 отделов: самый нижний отдел — это часть sinus urogenitalis, из которой образуется треугольник мочевого пузыря; средний расширенный отдел, который превращается в остальную часть мочевого пузыря, и верхний суженный отдел, представляющий мочевой ход, urachus, идущий от мочевого пузыря к пупку. У низших позвоночных по нему отводится содержимое аллантоиса, а у человека он к моменту рождения запустевает и становится фиброзным тяжом, lig. umbilicale medianum.
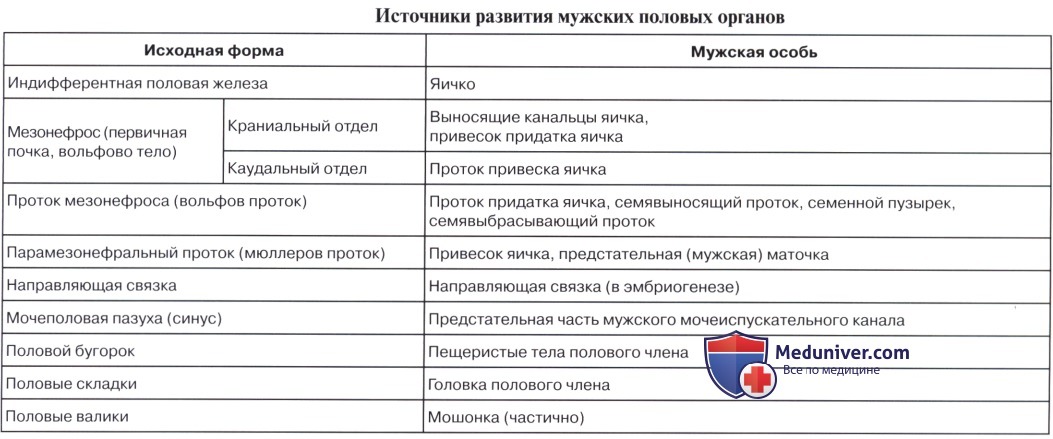

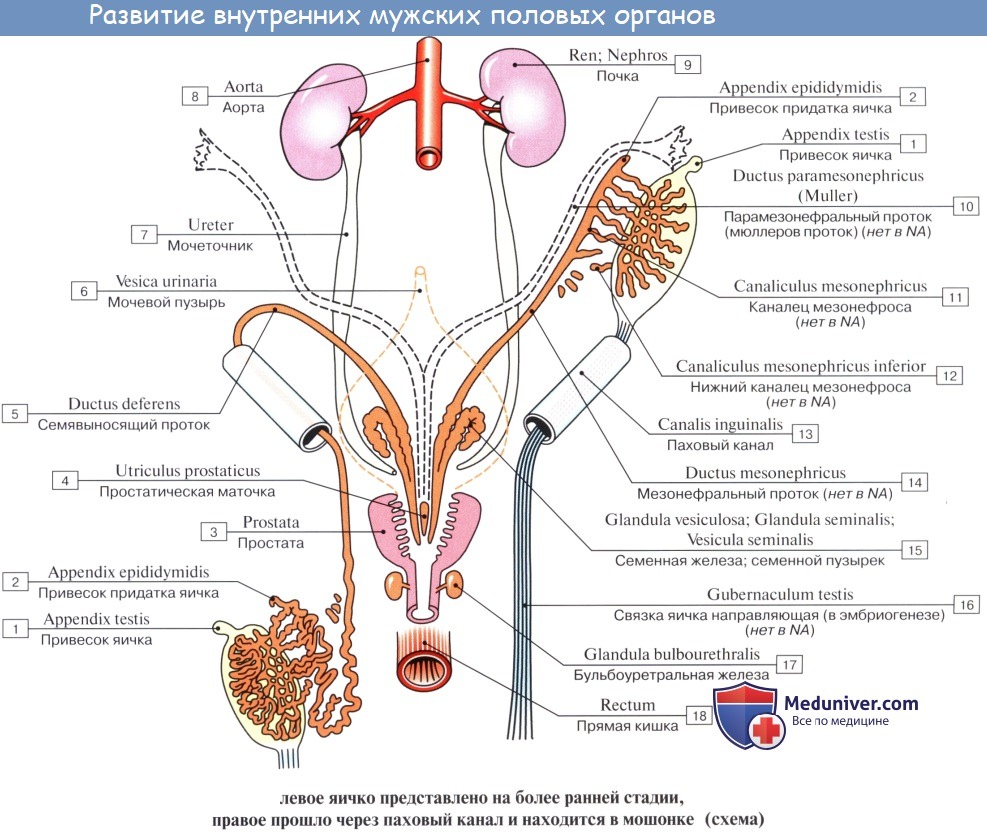
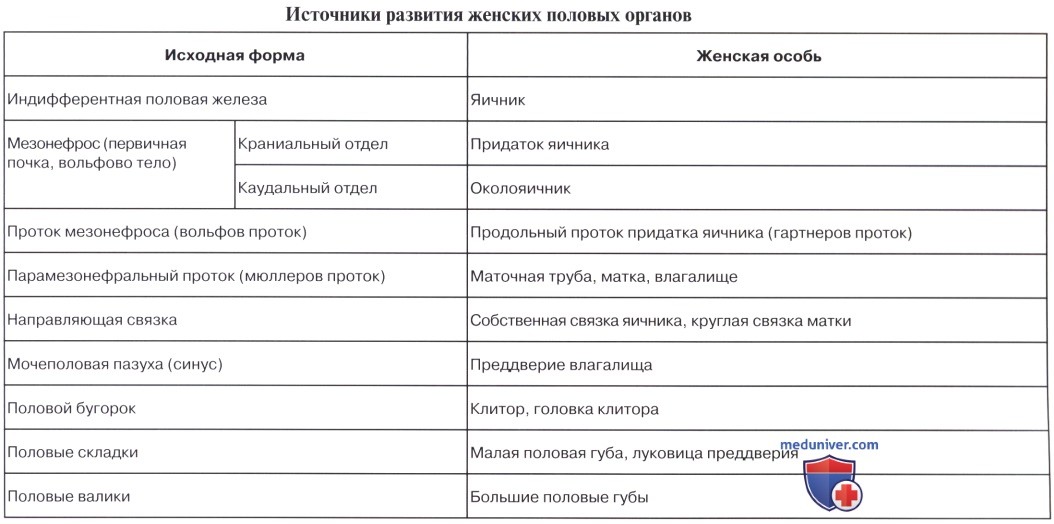
Остатками канальцев mesonephros у мужчины являются: tubuli recti, rete testis, ductuli efferentes, ductuli aberrantes и рудиментарное образование — paradidymis. У женщины — рудиментарные канальцы epoophoron и paroophoron. Из мезонефрального протока у мужчины образуются ductus epididymidis, ductus deferens и ductus ejaculatorius, у женщины — рудиментарный ductus epoophori longitudinalis.
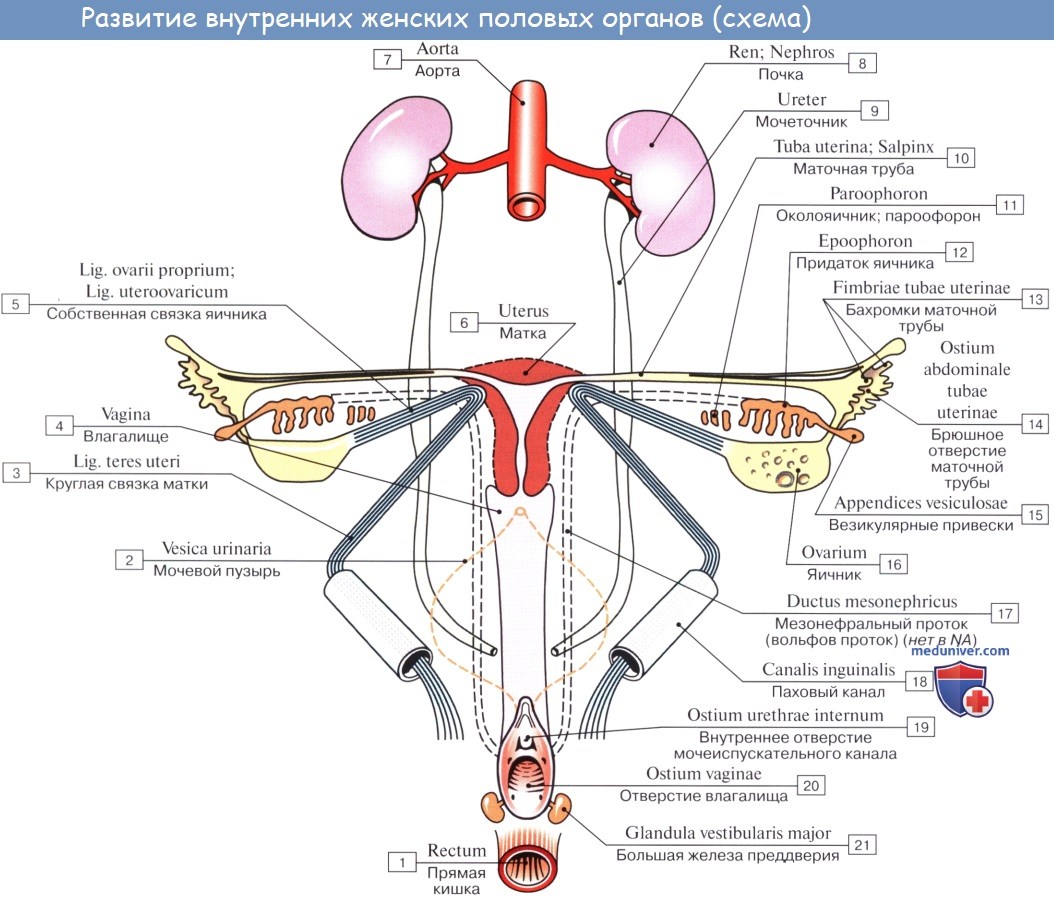
Ductus paramesonephrici дают начало развитию у женщины маточных труб, матки и влагалища. При этом грубы образуются из неслившихся верхних частей ductus paramesonephrici, а матка и влагалище — из слившихся нижних частей.
У мужчин ductus paramesonephrici редуцируются, и от них остаются только appendix testis и utriculus prostaticus (простатическая маточка). Таким образом, у мужчин редукции и превращению в рудиментарные образования подвергаются ductus paramesonephrici, у женщин — ductus mesonephrici.
— Также рекомендуем «Аномалии органов мочеотделения. Аномалии матки, труб и влагалища.»
Источник
Глава 1. ЭМБРИОГЕНЕЗ ОРГАНОВ МОЧЕВОЙ СИСТЕМЫ И ОСНОВЫ РАЗЛИЧНЫХ НАРУШЕНИЙ УРОГЕНЕЗА
Глава 1. ЭМБРИОГЕНЕЗ ОРГАНОВ МОЧЕВОЙ СИСТЕМЫ И ОСНОВЫ РАЗЛИЧНЫХ НАРУШЕНИЙ УРОГЕНЕЗА
В процессе онтогенеза и филогенеза органы мочевыделения проходят три стадии развития: пронефрос, мезонефрос и метанефрос.
Пронефрос (предпочка)
является онтогенетическим остатком выделительной системы низших
позвоночных. Это парное рудиментарное образование, не функционирующее у
человека, развивается из 8-10 передних нефротомов (сегментных ножек)
тела зародыша. Предпочка человека не имеет клубочков, её канальцы не
связаны ни с кровеносной системой, ни с целомом. На 4-й неделе
эмбрионального развития (длина эмбриона — менее 6 мм) пронефрос
редуцируется полностью.
Ещё до его полной редукции, на 3-4-й неделе эмбриогенеза, закладывается мезонефрос (первичная
почка). Поскольку мезоне-фрос развивается из туловищных нефротомов, его
называют также туловищной почкой. Это образование, расположенное
каудальнее пронефроса, уже имеет функционирующие клубочки с короткими
канальцами, которые соединяются с парными мезонефральными (или
вольфовыми) протоками, растущими в каудальном направлении, достигая
клоаки. Кроме этого, развивается второй (пара-нефральный) парный
мюллеров проток, соединяющий брюшную полость с урогенитальным синусом.
Первичная
почка человека наиболее активно функционирует примерно с 4-й по 8-ю
неделю эмбрионального развития. Начиная с 3-го месяца гестации
наблюдается постепенная регрессия первичной почки с дегенеративными
изменениями канальцев. Лишь с 5-го месяца эмбрионального развития
первичная почка редуцируется полностью. В дальнейшем в мочевую систему
встраивается только моче-точниковый зачаток — производное вольфова
протока. Некоторые элементы первичной почки участвуют в формировании
структур половой системы. Вольфовы протоки дают начало выводным протокам
яичек мужских особей, мюллеровы протоки — матке, маточным трубам и
влагалищу женских особей. Рудименты вольфовых и мюл-
леровых протоков сохраняются примерно у трети мужчин и женщин в виде так называемых гидатид яичек и гидатид яичников.
Метанефрос (окончательная,
или тазовая, почка) закладывается в конце 1-го месяца эмбриогенеза из
двух зачатков: метанефрогенного тяжа (ткань несегментированной
мезодермы), называемого также метанефрогенной бластемой, и материала
мезонефральных (воль-фовых) протоков, которые каудально впадают в
клоаку, а в верхних отделах образуют расширения (дивертикулы),
врастающие в мета-нефрогенную бластему. Из широкой части дивертикула
образуется лоханка формирующейся почки, выросты стенки которой дают
начало генерациям чашечек и собирательных трубочек, а в метанеф-рогенной
ткани бластемы начинают дифференцироваться канальцы нефронов. Одни
концы канальцев присоединяются к собирательным трубкам, а другие
контактируют с терминальными отделами почечной артерии — артериолами,
ветвления которых образуют клубочки капилляров почечных телец, то есть
гломерулы. На 8-9-й неделе начинают дифференцироваться клетки
проксимальных и дисталь-ных извитых почечных канальцев. На 14-16-й
неделе эмбриогенеза все отделы нефрона уже сформированы полностью;
одновременно развивается интерстициальная ткань, сосудистая система и
иннервация почки. С возникновением капилляров почечных клубочков
неф-роны приобретают фильтрационную способность, а при образовании
тонкой петли нефрона (петли Генле) и других канальцев —
реабсорб-ционную. Нарушения кровоснабжения и развития метанефрогенной
бластемы приводят к развитию аномалий величины почек (аплазии и
гипоплазии).
Мочеточниковый
зачаток (образовавшийся ещё на 5-6-й неделе эмбриогенеза из материала
вольфовых протоков) растёт в двух направлениях. Краниально он
соединяется с метанефросом, делится, давая начало росту лоханки,
чашечек, а затем — и собирательных канальцев, прорастая метанефрогенную
бластему и стимулируя развитие почки. Каудальный конец мочеточникового
зачатка постепенно достигает урогенитального синуса, отделяется от
клоаки и трансформируется в мочеточниково-пузырный сегмент. Меняя
тубулярную форму на форму листка, мочеточники открываются в просвет
мочевого пузыря точечными отверстиями. Во внутриутробном периоде эти
отверстия затянуты тонкой плёнкой (мембраной Хвалла); если эта мембрана
сохраняется после рождения ребёнка, это может клинически проявиться
формированием уретероцеле или уретерогидронефроза.
Сначала
окончательные почки расположены низко в тазовой области вблизи друг от
друга выводными протоками кпереди. На 7-8-й неделе (длина эмбриона
составляет 13-25 мм) начинается процесс восхождения почек. Почки
кровоснабжаются множественными сосудами, отходящими от тазовых ветвей
аорты, за счёт образования новых артериальных стволов. Из стенки аорты
появляется выпячивание, которое вырастает в крупный ствол, врастающий в
паренхиму почки и обеспечивающий её кровоснабжение. Прежние артерии,
снабжавшие кровью почечный зачаток, облитерируют и рассасываются.
Укорачиваясь, новые артериальные стволы, вырастающие из аорты,
подтягивают почку кверху и несколько ротируют. Затем образуются новые
сосуды, и почки, как по лестнице, продолжают восхождение и пронацию
(рис. 1).
Рис. 1. Процесс восхождения и ротации почек (по Исакову Ю.Ф., 2006)
Нарушения
эмбриогенеза на столь раннем этапе внутриутробного развития могут
заканчиваться аренией или агенезией одного органа либо вести к
формированию различных видов аномалий положения — дистопий. Кроме того,
примерно у трети людей сохраняются аберрантные (добавочные) сосуды,
нередко вызывая сдавление мочеточника.
Близкое
расположение метанефрогенных бластем нередко приводит к различным
аномалиям взаимоотношения почек. Нарушения в процессе соединения двух
зачатков (фильтрационно-реабсорб-ционного и мочевыделительного)
способствуют развитию аномалий структуры, к которым относят кистозные
аномалии (такие как поликистоз и солитарная киста почки). Кроме того, к
аномалиям
структуры принадлежат
удвоения почек, причиной которых служит расщепление мочеточникового
зачатка перед его врастанием в мета-нефрогенную бластему.
Нарушения
развития мочевыделительного аппарата метанефро-са формируют
разнообразные обструктивные пороки на уровне от собирательных канальцев
до устья мочеточника. Именно поэтому пороки развития чаще локализуются в
местах состыковки зачатков (на супрауретеральном или на
мочеточниково-пузырном уровне). Супрауретеральные нарушения проявляются
мегаполикаликозом, гидрокаликозом и гидронефрозом. Полное отсутствие
экскреторного канала ведёт к развитию мультикистоза. Все эти ткани и
органы образуются из зачатков мезодермальной ткани, проходя сложные
процессы закладки, развития и дифференцировки.
Параллельно
и ниже (каудальнее) происходит состыковка мезо-дермальных тканей с
энтодермальным образованием хвостовой кишки — мочевым пузырём.
Вследствие этого пороки развития на уровне мочеточниково-пузырного
сегмента, проявляющиеся различными видами уретерогидронефрозов, также
часты и разнообразны.
Мочевой пузырь
Мочевой
пузырь формируется в течение 2-го месяца эмбриогенеза. При этом в
клоаку во фронтальной плоскости внедряется урорек-тальная складка,
удлинение которой приводит к разделению мочеполового синуса и прямой
кишки у эмбрионов 6-7 нед. Нарушения в разделении этих структур ведут к
образованию различных свищей, связывающих мочеполовую систему и прямую
кишку. Иногда в процессе развития положение половых бугорков, залегающих
под формирующимся мочевым пузырём, меняется, что на 4-7-й неделе
гестации (длина эмбриона достигает 6-13 мм) приводит к нарушению
замыкания, то есть формирования передней стенки мочевого пузыря, и к
слабому росту покрывающей их мезодермы, из которой образована клоачная
мембрана. Мембрана рвётся, разрыв распространяется вверх по брюшной
стенке. Именно с этими нарушениями связано развитие такого порока, как
экстрофия мочевого пузыря.
Уретра
На
4-7-й неделе гестации (длина эмбриона — 6-13 мм) под влиянием
тестостерона фетальных яичек происходит дифференцировка зачаточного
эпителия нижних мочевых путей и замыкание уретрального жёлоба. Этот
процесс может нарушаться: если нижняя стенка
уретры
не сформируется в дистальных отделах, то для оттока мочи образуются
свищи различной локализации. Отсутствие дистальной уретры приводит к
грубой рубцовой деформации кавернозных тел и искривлению полового члена.
Так формируется наиболее распространённый порок мочевой системы —
гипоспадия.
Практическое
значение имеют и изменения, происходящие с мочевым протоком — урахусом,
который служит у эмбриона и плода для отведения первичной мочи в
околоплодные воды. Это алланто-идный стебелёк — трубчатое образование,
исходящее из верхушки мочевого пузыря и идущее к пупку. В норме на 20-й
неделе внутриутробного развития (плод длиной 25 см массой 340 г) урахус
обли-терирует и превращается в срединную пупочную связку. Иногда
протяжённость или выраженность его облитерации оказывается
недостаточной. Клинически после рождения ребёнка эти пороки могут
проявляться:
• полным пузырно-пупочным свищом;
• дивертикулом мочевого пузыря;
• кистой мочевого протока;
• неполным пузырно-пупочным свищом (так называемый мокнущий пупок).
Яичко
Яичко
плода расположено в брюшной полости возле почки. К 12-й неделе гестации
оно мигрирует от нижнего полюса первичной почки к области глубокого
(внутреннего) пахового кольца. Затем яичко смещается кверху, а к 5-му
месяцу гестации вновь опускается вниз, и к 7-8-му месяцу яичко проходит
паховый канал, располагаясь уже у входа в мошонку, а к 9-му месяцу
достигает дна мошонки. Иногда это происходит на протяжении 1-го месяца
после рождения. Направляющий тяж (связка Гунтера) формируется раньше
начала миграции яичка через паховый канал. Он проходит через влагалищный
отросток брюшины, открытый на этом этапе эмбриогенеза, подготавливая
путь для нисхождения яичка в мошонку. После окончания этого процесса
гунтерова связка превращается в мошоночную связку. Различные препятствия
и нарушения процесса миграции яичка приводят к аномалиям положения
яичка (ретенции, эктопии).
Источник
Физиологические аспекты мочеиспускания у детей раннего возраста | #09/18 | «Лечащий врач» – профессиональное медицинское издание для врачей. Научные статьи.
Изучение уродинамики нижних мочевых путей является обязательным этапом обследования детей с пороками развития почек и верхних мочевых путей, расстройствами мочеиспускания и энурезом, рецидивирующим течением инфекции мочевыводящих путей, пиелонефритом. Наибольшую значимость и сложность эта проблема приобретает при лечении новорожденных и детей раннего возраста, стертости клинических проявлений нарушений мочеиспускания, сложности проведения специальных уродинамических исследований.
В данном аспекте особую значимость для урологов и нефрологов педиатрического профиля приобретают сведения о физиологии мочеиспускания новорожденных и детей младшего возраста, имеющие определяющее значение для ранней диагностики патологии мочевыделительной системы и предупреждения осложнений.
Физиология мочеиспускания у детей раннего возраста до настоящего времени остается не до конца изученной.
Акт мочеиспускания состоит из двух фаз — фазы накопления мочи и фазы эвакуации мочи. При этом детрузор мочевого пузыря и его сфинктеры (гладкомышечный и наружный, поперечно-полосатый) находятся в реципрокных отношениях: в фазу накопления мочи детрузор расслабляется, а сфинктер сокращен и удерживает мочу; в фазу опорожнения мочи — сокращается детрузор и расслабляется сфинктер, происходит опорожнение мочевого пузыря. Обеспечивает этот процесс сложная регуляторная система, в работе которой участвуют спинной мозг, субкортикальные и корковые центры, система биологически активных веществ и половые гормоны.
В фазу накопления мочи основная роль принадлежит детрузору мочевого пузыря, который обеспечивает адекватную резервуарную функцию (за счет эластичности мышц мочевого пузыря и благодаря системе детрузор-стабилизирующих рефлексов), при этом давление в мочевом пузыре, несмотря на его заполнение, поддерживается на низком уровне (5–10 см водного столба). Эвакуация мочи — сложный рефлекторный акт, во время которого происходит синхронное расслабление внутреннего и наружного сфинктеров мочевого пузыря и сокращение мышцы мочевого пузыря — детрузора. В эвакуации мочи принимают участие также мышцы брюшного пресса и промежности. Нормальное мочеиспускание определяется анатомической и функциональной полноценностью не только сфинктеров и детрузора, но и системой нервных структур, регулирующих этот сложный акт.
Основным вегетативным центром является спинальный центр регуляции мочеиспускания, располагающийся на уровне пояснично-крестцовых сегментов спинного мозга, который, в свою очередь, имеет симпатическое (Th XII — L II–III) и парасимпатическое (L IV–V) представительство. Следует помнить, что парасимпатический отдел отвечает за вегетативное обеспечение сократительной активности детрузора, а симпатический — за его адаптацию (по мере заполнения мочевого пузыря давление в нем не повышается). Соматическое обеспечение поперечно-полосатой мускулатуры тазового дна обеспечивается за счет сакральных сегментов. А вот связь соматического и вегетативного звеньев осуществляется благодаря системе рефлексов, стабилизирующих детрузор. Именно благодаря этой сложной системе и обеспечиваются реципрокные отношения между детрузором и сфинктером (при сокращении детрузора — сфинктер расслабляется, и, наоборот, прекращение мочеиспускания и сокращение сфинктера ведут к восстановлению резервуарной функции мочевого пузыря) [1, 2].
Динамический характер изменений мочеиспускания в процессе роста ребенка затрагивает как увеличение гидродинамических параметров мочеиспускания (объем мочевого пузыря, частота мочеиспусканий, изменение скорости тока мочи), так и контролируемые сознанием характеристики (позыв, умение прерывать мочеиспускание, поведенческие реакции), что в совокупности позволяет констатировать формирование «зрелого» типа мочеиспускания [1].
Традиционная концепция предполагает, что мочеиспускание новорожденного происходит автоматически, за счет спонтанно возникающего рефлекса, замыкающегося на уровне спинного мозга. Однако последние исследования фетальной уродинамики показали, что такое мнение довольно упрощенное. Появились доказательства того, что даже внутриутробно мочеиспускание имеет поведенческие зависимости: отмечены задержки мочеиспускания во время сна плода и максимально частое опорожнение пузыря во время бодрствования плода.
При изучении вопросов физиологии мочеиспускания плодов 19–40 недель гестации с использованием антенатальной ультразвуковой цистометрии при естественном наполнении оценены накопительная, эвакуаторная функции мочевого пузыря, характер мочеиспускания плодов. Уродинамика плодов оценивалась с помощью таких показателей, как максимальный объем мочевого пузыря, продолжительность микционного цикла, процент остаточной мочи, продолжительность выведения мочи, диурез [3, 4].
Отмечено, что с 19-й до 38–40 недели гестации размеры мочевого пузыря возрастают практически в 30–40 раз и составляют в 20 недель 0,65–1,0 мл, а в 40 недель — 25–30 мл. Закономерности темпов роста объема мочевого пузыря опережают темпы роста массы плода, которая за эти же сроки возрастает более чем в 10 раз.
При изучении продолжительности микционного цикла — показателя, эквивалентного ритму спонтанных мочеиспусканий, отмечено его увеличение по мере возрастания срока гестации. Предположено, что плод мочится 72 раза в сутки в 20 недель и 32–36 раз в 38–40 недель.
У большинства плодов опорожнение мочевого пузыря полное. При этом во II и III триместрах беременности допустимым является наличие 10–15% остаточной мочи [3–5].
Характер мочевыведения плода значительно отличается от такового у детей постнатального периода. Наряду с одномоментным мочеиспусканием отмечается фракционное мочеиспускание, чаще встречаемое в III триместре беременности.
Такие характеристики, как фракционный способ опорожнения мочевого пузыря и его неполная эффективность (с остаточной мочой 10–15%), определяют так называемый «фетальный тип мочеиспускания».
Эквиваленты фетальных поведенческих реакций проявляются в виде двигательной активности плода, предшествующей выведению мочи, или преждевременным опорожнением мочевого пузыря в ответ на шумовой раздражитель. Таким образом, в процессе антенатального периода становление мочеиспускания плода осуществляется за счет поддержания функционального режима чередования микционных циклов, формирования основных показателей мочеиспускания: пузырного рефлекса, «фетального» типа выведения мочи, эквивалентов фетальных поведенческих реакций [4, 5]. В течение последнего триместра беременности внутриматочной мочи производится намного больше, чем в постнатальный период (30 мл/час), а частота мочеиспускания плода приблизительно равна 30 раз в сутки [4–6].
В постнатальный период механизмы контроля мочеиспускания претерпевают дальнейшие изменения. Использование амбулаторного мониторинга мочевого пузыря в сочетании с методом полисомнографии показало, что у новорожденных во время сна мочевой пузырь находится в состоянии покоя и мочеиспускание во время сна не происходит [7].
Сразу после рождения мочеиспускание обычно редкое. Первый раз младенец может помочиться через 12 и более часов (до 24 часов). После первой недели частота мочеиспусканий быстро возрастает и достигает максимума в возрасте от 2 до 4 недель и составляет в среднем один раз в час. Затем частота уменьшается и остается стабильной до 6 месяцев — 10–15 раз в день. После первого года число мочеиспусканий уменьшается до 8–10 раз в день. У новорожденных мочеиспускание может иметь прерывистый характер, при этом более чем в 80 процентах мочевой пузырь опорожняется полностью [8]. Для детей до шести месяцев жизни характерным является частое и неполное опорожнение мочевого пузыря, мочеиспускание в два приема, относительно большой объем остаточной мочи, что указывает на функциональную нестабильность мочевого пузыря, которая уменьшается с возрастом и достигает определенной зрелости к одному году [9].
Установлено, что становление функции мочевого пузыря у здоровых детей протекает в три стадии, которые имеют определенную последовательность и четкие возрастные границы. На первой стадии формирования функции мочевого пузыря значительные изменения претерпевает емкость мочевого пузыря, которая на первом году жизни увеличивается в два раза, а к трем годам в шесть раз. Со второго месяца жизни происходят существенные колебания емкости мочевого пузыря в течение дня, что позволяет выделить максимальный и минимальный объемы. Эффективный объем первого после сна мочеиспускания формируется к середине второго года жизни. С 6–8 месяцев до одного года ребенок начинает ощущать и пытаться как-то «сигнализировать» о необходимости мочиться. Идет активное формирование условного рефлекса, формируются кортико-висцеральные (вертикальные) связи, осуществляемые через подкорковые, понтийные центры. Важным моментом на первой стадии формирования емкости мочевого пузыря является период, когда ребенок начинает ходить. В это время отмечается учащение мочеиспускания, уменьшение объема порции мочи, появление «прерывистого» мочеиспускания. С полутора лет у здоровых детей стабильно увеличивается эффективная емкость мочевого пузыря и уменьшается частота мочеиспусканий. В период становления основных черт зрелого мочеиспускания выявлены отличительные особенности уродинамики нижних мочевых путей у детей грудного и раннего возраста. Установлено, что процесс наполнения мочевого пузыря у них осуществляется в условиях базовой гипертензии. Реализация микционного цикла при относительно высоком давлении отражает свойственный этому периоду жизни ребенка гипертонус гладких мышц мочевого пузыря, обеспечивающий высокий автоматизм эвакуации мочи до появления произвольного контроля мочеиспускания [10].
Также отмечено, что давление вытеснения у мальчиков выше, чем у девочек, а до 70% младенцев имеют прерывистое мочеиспускание. Эти более высокие значения давления детрузора и прерывистый характер мочеиспускания постепенно уменьшаются с возрастом в течение 1–2 лет жизни, отражая процесс созревания детрузора и сфинктерной координации. Видеоуродинамические исследования подтверждают эти результаты [8, 11–14]. По мере взросления ребенка, в привитии навыков мочеиспускания и формирования зрелого типа контроля над ним, особую важность приобретают три основных фактора:
1) увеличение емкости мочевого пузыря для обеспечения его резервуарной функции;
2) появление произвольного контроля над поперечно-полосатой мускулатурой (наружный уретральный сфинктер) для обеспечения произвольного начала и окончания акта мочеиспускания, что обычно появляется к третьему году жизни;
3) формирование прямого произвольного контроля над микционным рефлексом, что позволяет ребенку управлять процессом сокращения детрузора собственным волевым усилием.
О «зрелом типе» мочеиспускания можно говорить тогда, когда оно становится полностью управляемым (контролируемым ребенком). Его клиническими признаками являются:
- соответствие объема мочевого пузыря возрасту ребенка;
- адекватное диурезу и объему мочевого пузыря число мочеиспусканий в сутки;
- полное удержание мочи днем и ночью;
- умение задерживать и прерывать при необходимости акт мочеиспускания;
- умение опорожнять мочевой пузырь без предшествующего позыва на мочеиспускание;
- адекватное поведение (стремление к уединению при появлении позыва, приемы непосредственной подготовки к опорожнению мочевого пузыря, переживание при наличии любых его расстройств и пр.) [15, 16].
Сформированный механизм контроля над микционным рефлексом, аналогичный взрослому, у большинства детей складывается к 4–5 годам. Контроль над мочеиспусканием в ночное время имеет более широкие возрастные границы (3–7 лет) [17].
Определение эффективной емкости мочевого пузыря у детей различных возрастов производится по формулам:
- у младенцев: емкость мочевого пузыря (мл) = 38 + (2,5 × возраст (мес)) [14];
- у детей с одного года жизни: емкость мочевого пузыря (мл) = 30 + 30n, где n — возраст в годах [18].
Таким образом, знание сложных и многокомпонентных регуляторных механизмов мочеиспускания поможет разобраться в этиопатогенезе расстройств мочеиспускания и недержания мочи у детей. Тем не менее, следуя диагностическому протоколу, разработанному на основании рекомендаций Международного общества по удержанию мочи у детей (International Children’s Continence Society, ICCS), можно, проведя необходимые исследования, четко дифференцировать различия в причинах и характере недержания мочи, назначить лечение, обоснованное патогенетически, провести курс реабилитации и добиться выздоровления [19].
Работа выполнена в рамках государственного задания Минздрава России «Разработка тактики постнатального лечения детей с антенатально выявленными пороками мочевыделительной системы».
Литература
- Джавад-Заде М. Д., Державин B. M., Вишневский Е. Л. и др. Нейрогенные дисфункции мочевого пузыря. М.: Медицина. 1989. 384 с.
- Franco I. Overactive bladder in children. Part 1: Pathophysiology // J Urol. 2007; 178 (3 Pt 1): 761–8.
- Дерюгина Л. А. Антенатальная диагностика врожденных заболеваний мочевыводящей системы и обоснование тактики ведения детей в постнатальном периоде. Автореф. дис. … д.м.н, 2008. 50 с.
- Дерюгина Л. А., Морозов Д. А. Становление мочевыведения плода на этапах гестации // Детская хирургия. 2007. № 6. С. 22–27.
- Дерюгина Л. А. Расстройства уродинамики нижних мочевых путей у плодов // Детская хирургия. 2007. № 3. С. 30–34.
- Goelllner M. H., Ziegler E. E., Fomon S. J. Urination duringtheFirst 3 yearsof life // Nephron. 1981; 28: 174–178.
- Yeung C. K., Godley M. L., Ho C. K. W., Ransley P., Duffy P. G., Chen C. N., Li A. K. C. Somt ntw insights into bladder function in infancy // Br J Urol. 1995; 6; 235–240.
- Yeung C. K., Godley M. L., Duffy P. G., Ransley P. G. Natural filing cystometry in infants and children // Br J Urol. 1995; 75: 531–537.
- Николаев Н. С. Диагностика и лечение дисфункций мочевого пузыря у детей раннего возраста. Автореф. дис. … к.м.н., 2003. 27 с.
- Рудакова Э. А. Дисфункции мочевого пузыря у детей раннего возраста. Автореф. дис. … д.м.н., 1995. 28 с.
- Yeung C. K., Godley M. L., Dhillon H. K., Duffy P. G., Ransley P. G. Urodynamic patterns in infants with normal lover urinary tracts or primary vesico-ureteric reflux // Br J Urol. 1998; 81: 461–467.
- Bachelard M., Sillen U., Hansson S., Hermansson G., Jodal U., Jacobsson B. Urodinamic pattern in asymptomatic infants: siblidings of children with vesico-ureteric reflux // J Urol. 1999; 162: 1733–1737.
- Sillen U., Solsnes E., Yellstrom A. I., Sandberg K. The voiding pattern of healthy preterm neonates // J Urol. 2000; 163: 278.
- Holmdahl G., Hansson E., Hansson M., Hellstrom A.-L., Hjälmås K., Sillen U. Four hour voiding observation in healthy infants // J Urol. 1996; 156: 1809–1812.
- Yeates W. K. Bladder function in normal Micturition. In: Kolvin I., MacKeith R. C., Meadow S. R. (eds). Bladder Control and Enuresis. London, W Heinemann Medical, 1973. 28–365.
- Вишневский Е. Л., Лоран О. Б., Вишневский А. Е. Клиническая оценка расстройств мочеиспускания. М.: Терра, 2001. 96 с.
- Hellstrom A. L., Hansson E., Hansson S., Hjälmås K., Jodal U. Micturition habits and incontinence in 7-year-old Swedish school entrants // Eur J Pediatr. 1990; 149 (6): 434–437.
- Koff S. A. Estimating bladder capacity in children // Urology. 1983; 21: 248–251.
- Основные принципы диагностики и лечения расстройств мочеиспускания у детей и подростков. Методические рекомендации № 10. М., 2013. 40 с.
Т. В. Отпущенникова, кандидат медицинских наук
ФГБОУ ВО СГМУ им. В. И. Разумовского, Саратов
Контактная информация: tkatina1@yandex.ru
Физиологические аспекты мочеиспускания у детей раннего возраста/ Т. В. Отпущенникова
Для цитирования: Лечащий врач № 9/2018; Номера страниц в выпуске: 26-28
Теги: энурез, пиелонефрит, нижние мочевые пути, условный рефлекс
Источник