Эрозия стенки мочевого пузыря
Содержание статьи
Склероз шейки мочевого пузыря
Склероз шейки мочевого пузыря — это рубцовая деформация уретро-везикального перехода, обусловленная травматическими воздействиями, воспалительными процессами. Проявляется затруднением мочеиспускания, вялостью струи мочи, дизурическими явлениями. Диагностируется при помощи урофлоуметрии, ретроградной и микционной уретрографии, УЗИ мочевыводящих органов, МСКТ цистоуретрографии, задней уретроскопии, цистоскопии. Лечится оперативно путем трансуретральной резекции склерозированного участка. Хирургическое вмешательство дополняют антибактериальной и противовоспалительной терапией, при выраженной обструкции или обтурации предваряют эпицистостомией.
Общие сведения
По результатам исследований в сфере клинической урологии, склеротическая деформация с сужением просвета мочепузырно-уретрального сегмента выявляется у 0,4-1,5% пациентов, перенесших операцию по поводу доброкачественной гиперплазии простаты. Менее распространены случаи заболевания, обусловленные другими причинами. Вероятность развития склероза зависит от способа выполнения аденомэктомии. Реже всего рубцовая деформация возникает после ТУР гольмиевым лазером и биполярной плазменно-кинетической резекции, чаще всего – после чрезпузырной аденомэктомии. Обычно заболевание диагностируют у мужчин в возрасте после 45 лет, идиопатическая врожденная форма болезни может проявляться даже у младенцев.
Склероз шейки мочевого пузыря
Причины
Заболевание имеет полиэтиологическую основу, может быть как приобретенным, так и врожденным. Склеротические процессы в области шейки пузыря обычно вторичны, развиваются на фоне другой урологической патологии или под действием различных повреждающих факторов. Непосредственными причинами возникновения склероза в зоне мочепузырного треугольника являются:
- Хирургическое лечение урологических заболеваний. Обычно склеротические изменения выявляются у пациентов, перенесших открытые и эндоскопические операции по поводу аденомы предстательной железы. Реже интенсивное склерозирование начинается после лучевой терапии рака мочевого пузыря или простаты.
- Воспаление органов мочевыделительной системы. Вероятность склероза в области мочепузырно-уретра льного перехода увеличивается при хронических простатитах и циститах. В таких случаях регенеративная фаза воспаления принимает патологический характер, в пораженных участках формируется плотная соединительная ткань.
- Дизэмбриогенез. Идиопатическая форма склероза мочепузырной шейки носит название болезни Мариона. Патология встречается редко, характеризуется кольцевидным фиброзом подслизистого и мускульного слоев на выходе из мочевого пузыря. Факторы, способствующие возникновению врожденного склероза, пока не установлены.
Анатомической предпосылкой к развитию заболевания являются особенности строения стенки пузыря в области мочепузырного треугольника. Соединительная ткань собственной пластинки под уротелием этой зоны отличается меньшей рыхлостью, из-за чего слизистая оболочка менее растяжима и практически не имеет складок. В результате склеротические изменения плохо компенсируются и быстро проявляются клинически.
Патогенез
Механизм склерозирования шейки мочевого пузыря основан на чрезмерном разрастании соединительнотканных элементов при патологической регенерации поврежденных тканей. Как правило, предрасполагающими факторами к появлению склеротических изменений являются нарушение энергетического метаболизма в стенке органа, локальная воспалительная реакция, клеточная дистрофия, микроциркуляторные нарушения, характерные для доброкачественной гиперплазии предстательной железы. Иногда процесс провоцируется действием прямых повреждающих факторов (операционной травмы, лучевого излучения).
Склероз мочепузырной стенки формируется поэтапно. Сначала после фагоцитоза разрушенных клеток и коллагеновых волокон макрофагами в зоне повреждения происходит активная пролиферация фибробластов, усиливается синтез коллагена. В условиях ишемии, посттравматического воспаления, дисциркуляторных явлений нарушается баланс между коллагеногенезом и коллагенолизисом с нарастанием избытка соединительной ткани, преобладанием массы волокон над клеточными элементами, уменьшением количества специализированных клеток. В результате шейка мочевого пузыря подвергается фиброзированию, склерозированию или рубцеванию с частичным сужением (стриктурой) или полным перекрытием (облитерацией) просвета, что проявляется соответствующей клинической картиной.
Симптомы
Основным клиническим признаком заболевания является нарастающее ухудшение оттока мочи вплоть до ее полной острой задержки. На начальных этапах патологического процесса пациенты жалуются на затруднения при мочеиспускании, отмечают вялость мочевой струи. По мере прогрессирования склероза и увеличения количества остаточной мочи в полости органа у больных появляется ощущение неполного опорожнения мочевого пузыря. О присоединении воспаления свидетельствуют частые позывы к мочеиспусканию, болезненное отхождение мочи, повышение температуры тела до субфебрильных цифр.
Осложнения
Нарушение оттока мочи постепенно приводит к увеличению ее остаточного объема и застою в вышерасположенных органах мочевыделительной системы. В крайних случаях расширение мочеточников и чашечно-лоханочной системы завершается развитием двухстороннего уретерогидронефроза и хронической почечной недостаточности. Наличие пузырно-мочеточникового рефлюкса способствует восходящему распространению уроинфекций с возникновением уретерита, пиелонефрита.
На фоне мочепузырного застоя мочи чаще наблюдаются хронические циститы, могут сформироваться микродивертикулы. У некоторых пациентов происходит сморщивание мочевого пузыря. Длительное нарушение мочеиспускания способствует появлению невротических расстройств, депрессии, социальной дезадаптации пациентов.
Диагностика
Обследование мужчин с подозрением на склероз шейки мочевого пузыря включает инструментальные методы, позволяющие выявить признаки сужения участка пузырно-уретрального перехода, исключив другие причины обструкции. Важную роль в диагностическом поиске играет связь патологического процесса с проведенной операцией на простате, лучевой терапией тазовых органов, урологическими инфекциями. Наибольшей информативностью обладают:
- Уродинамические исследования. При сохраненном мочеиспускании пациентам обычно назначают урофлоуметрию. Длительное нарастание и уменьшение объемной скорости тока мочи подтверждает обструкцию нижних отделов мочевыделительной системы, однако не позволяет выявить точное место стеноза. Поэтому методика обычно предваряет проведение других инструментальных исследований.
- Уретрография. Рентгенологический метод дает возможность обнаружить препятствие току мочи в области перехода мочевого пузыря в уретру, при этом уретральный канал остается полностью проходимым. Чаще применяется ретроградная уретрография, визуализирующая заполнение мочеиспускательного канала рентген-контрастным раствором, реже — микционное исследование процесса мочевыделения.
- Эхография. С помощью УЗИ мочевого пузыря оценивают анатомические особенности строения органа, в том числе пузырно-уретрального сегмента, определяют его вместимость и объем остаточной мочи, который при склерозе шейки обычно превышает 20 мл. Дополнительное ультразвуковое исследование почек, мочеточников, простаты (при ее наличии), уретры позволяет установить другие причины нарушения мочеиспускания.
- Мультиспиральная компьютерная томография. МСКТ цистоуретрография, обеспечивающая создание трехмерной модели пораженной области — один из наиболее точных неинвазивных методов диагностики склероза. Используя МСКТ, можно точно определить место стриктуры нижних мочевыводящих путей, выраженность склеротических изменений, толщину стенки везикально-уретрального перехода.
- Эндоскопия. Визуализация пораженной области при уретроцистоскопии дает возможность не только выявить участок стриктуры, но и оценить состояние слизистой оболочки, степень рубцовых изменений. При достаточном для прохождения эндоскопа просвете шейки осматривается полость мочевого пузыря. Обследование может дополняться биопсией для гистологического исследования тканей.
Общий анализ мочи при склерозе мочепузырной шейки играет вспомогательную роль, направлен на выявление возможных сопутствующих воспалительных процессов. Заболевание дифференцируют с аденомой предстательной железы, ложным ходом из мочеиспускательного канала в мочевой пузырь, предпузырем мочевого пузыря, склерозом простаты, злокачественными и доброкачественными опухолями мочевого пузыря. По показаниям врач-уролог может назначить консультацию онколога, андролога.
Лечение склероза шейки мочевого пузыря
Эффективная консервативная терапия заболевания не предложена. Единственный метод восстановления проходимости уретро-везикального сегмента — хирургическое иссечение рубцовой ткани. Эффект от ликвидации стриктуры с помощью бужирования временный, проведение этого вмешательства зачастую приводит к возникновению различных осложнений.
На этапе предоперационной подготовки и в послеоперационном периоде пациенту проводится антибактериальная терапия для профилактики инфекционных осложнений. При наличии признаков воспаления и болевого синдрома возможно дополнительное назначение нестероидных противовоспалительных средств. Для быстрой разгрузки мочевыделительной системы при значительной обструкции шейки предварительно может выполняться открытая или троакарная эпицистостомия.
Наиболее эффективным и наименее травматичным вмешательством для восстановления нормального пассажа мочи является ТУР шейки мочевого пузыря. При трансуретральной резекции склерозированные ткани полностью удаляются лазерными либо электрокоагуляционными ножами, что позволяет устранить обструкцию. Открытые инвазивные операции на мочепузырной шейке из-за травматичности и высокого риска осложнений в настоящее время практически не применяются.
Прогноз и профилактика
Эффективность хирургического лечения склеротической деформации мочепузырной шейки достигает 91%, однако при значительном сужении ее просвета возрастает риск послеоперационных рецидивов. Профилактика склероза направлена на адекватную своевременную терапию урологических заболеваний, щадящее выполнение аденомэктомии, других вмешательств на простате и мочевом пузыре. Для предотвращения рецидива обструкции после ТУР рекомендовано использование современных высокоэнергетичных генераторов, работающих в режиме менее травматичного биполярного резания и коагуляции.
Источник
Лейкоплакия мочевыводящих путей
Под лейкоплакией (или кератинизирующей плоскоклеточной метаплазией) понимают ороговевающее изменение эпителия, связанное с инфекционным процессом мочевыводящих путей, а также хроническим раздражением. Патология встречается достаточно редко и считается предраковым состоянием, предрасполагающим к развитию плоскоклеточного рака, особенно если поражение составляет более 50% поверхности. В порядке убывания частоты лейкоплакия может развиться в мочевом пузыре, почечной лоханке и мочеточнике.
С помощью только медикаментов это состояние не вылечить. Если поражен небольшой участок мочевого пузыря, применяется трансуретральная резекция. В последующем рекомендуется наблюдение за пациентами с ежегодной цистоскопией и множественными биопсиями, и проведением визуальной оценки состояния мочевыводящих путей.
Общие сведения о лейкоплакии мочевыводящих путей
Мочевыводящие пути (лоханки, мочеточники, мочевой пузырь, проксимальный участок уретры) выстилает уротелий или переходноклеточный эпителий. Его замена/преобразование слоями плоских клеток называется плоскоклеточной метаплазией.
Плоскоклеточная метаплазия может быть ороговевающей или неороговевающей:
- Некератинизирующая/неороговевающая плоскоклеточная метаплазия. Преимуществено возникает в мочепузырном треугольнике. Это состояние называется тригонит. Как правило, оно не вызвано хроническим раздражением, клеточная атипия отсутствует. Такое изменение в тригоне присутствует у 85% женщин репродуктивного возраста и у 75% женщин в менопаузе (у мужчин тоже встречается), где это считается нормальным (неметапластическим) обнаружением. Возникновение за пределами этой области считается метапластическим.
- Ороговевающая (кератинизирующая) плоскоклеточная метаплазия. Также известна под термином лейкоплакия. Это редкое явление, чаще всего встречающееся у мужчин. Сообщается, что заболеваемость составляет 1:10000, однако анализ литературы показывает, что патология может быть более распространена.
Морфологическая картина лейкоплакии мочевого пузыря. Фото 1
Морфологическая картина лейкоплакии мочевого пузыря. Фото 2
Ороговевающая плоскоклеточная метаплазия преимущественно развивается в мочевом пузыре. Уч. Benson в своем исследовании анализировал 108 человек с лейкоплакией: у 78 было поражение мочевого пузыря, 24 имели изменение верхних мочевыводящих путей, 10 – уретры (1 с поражением почек и мочевого пузыря, 3 с поражением мочевого пузыря и уретры и 1 с поражением уретры и почек). Лейкоплакия в два раза чаще встречается в мочевом пузыре по сравнению с почечной лоханкой и мочеточником.
Риск инвазивной карциномы или обструктивной уропатии появляется, когда поражение сохраняется в течение долгого времени.
Несмотря на то, что предложено несколько этиологических факторов, вызывающих патологию, – хроническое воспаление, раздражители и инфекция, патогенез лейкоплакии до конца не изучен. Естественная история плоскоклеточной метаплазии и клиническое лечение спорны.
Многие ученые рассматривают плоскоклеточную метаплазию как неопластическое предраковое поражение, поэтому очень важно найти эффективное лечение, снижающее риск развития плоскоклеточного рака мочевого пузыря.
Возможные причины лейкоплакии и предрасполагающие факторы
Точная причина ороговевающей плоскоклеточной метаплазии не установлена. Ниже перечислены основные из предполагаемых этиологических факторов, которые приводят к хроническому раздражению слизистых оболочек мочевыводящих путей (преимущественно мочевого пузыря).
Инфекции:
- Шистосомоз (паразитарное заболевание). Наиболее частая причина плоскоклеточной метаплазии.
- Туберкулез мочевыводящих путей. Также ассоциируется с изменением слизистой этих органов и мочеиспускательного канала.
- Сифилис. Состояние лейкоплакии также наблюдалось при сифилисе до широкого применения пенициллина.
- Кишечная палочка, энтеробактерии из рода Proteus, энтерококки. Сейчас кишечная палочка, Proteus и Streptococcus faecalis – три наиболее идентифицируемых микроорганизма у людей с плоскоклеточным преобразованием уротелия. Традиционно в литературе приводится показатель от 49 до 100% доказанной инфекции у этих пациентов. Считается, что инфекции мочевыводящих путей вызывают ороговевшую плоскоклеточную метаплазию в ответ на воспалительную травму.
- Дефекты гликозаминогликанового слоя мочевого пузыря. Предрасполагают к изменению (в том числе неопластическому) слизистой оболочки.
- Некератинизирующая плоскоклеточная метаплазия или тригонит. Часто ассоциируется с инфекцией, причем хронической (в тригоне или треугольнике Льето создается своеобразный резервуар бактерий).
![]() Кишечная палочка Proteus
Кишечная палочка Proteus
Любой инфекционный процесс сопровождается воспалительным, который вызывает изменение тканей.
Постоянные, длительно воздействующие раздражители, которые могут привести плоскоклеточной метаплазии включают:
- постоянные катетеры;
- мочевые конкременты;
- непроходимость путей/мочевого пузыря;
- свищи;
- опухоли;
- экстрофия (порок мочевого пузыря);
- нейрогенный мочевой пузырь;
- хирургические вмешательства на мочевом пузыре в анамнезе;
- недостаток витамина А.
![]() Катетеры
Катетеры
Есть случаи, при которых наблюдали плоскоклеточную метаплазию, прогрессирующую до плоскоклеточной карциномы (squamous cell carcinoma SCC) у пациента, получающего лучевую терапию по поводу переходно-клеточной карциномы.
Также описан единственный случай, указывающий на генетическую предрасположенность к некератинизирующей плоскоклеточной метаплазии мочевыводящих путей. Он относится к описанию группы уч. Мюллера трех женщин в семье с уротелиальной лейкоплакией без основного этиологического фактора.
Симптомы лейкоплакии мочевого пузыря
У пациентов с лейкоплакией обычно имеются неспецифические симптомы со стороны мочевыделительной системы, включая:
- гематурию;
- дизурию;
- срочные позывы к мочеиспусканию;
- увеличенную частоту позывов.
Есть случай, когда у пациента были белые хлопья в моче.
Гистологические особенности
Гистопатологические особенности ороговевающего плоскоклеточного изменения уротелия впервые описал Рокитанский в 1862 году как чрезмерное образование плоского эпителия с десквамацией и нагромождением эпителия. Окончательный оно описано позже просто как ороговение неороговевшей оболочки.
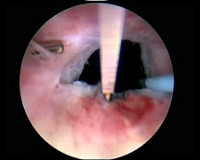
При цистоскопии ороговевающая плоскоклеточная метаплазия проявляется как область гиперемии с жемчужными бляшками, которые, кажется, плывут по окружающему воспаленному уротелию. Эти бляшки могут быть дискретными или диффузными, незаметно переходя в окружающий эпителий. Когда эти жемчужные бляшки нарушены, подлежащая поверхность выглядит сосочковой и легко кровоточит.
Кератинизация может затронуть любую часть мочевыводящих путей, включая простатический участок уретры.
Микроскопически определяется, что уротелий, который заменяется многослойным плоским эпителием, можно разделить на ороговевающие и некератинизирующие подтипы. В верхнем слое ороговевающего подтипа содержатся плоские роговые чешуйки (происходит процесс ороговения). К некератинизирующему типу относится изменение слизистой преимущественно у женщин на треугольнике Льето мочевого пузыря. Это считается нормальным анатомическим вариантом и вызвано гормональным воздействием.
Другие неинвазивные плоскоклеточные поражения мочевого пузыря следующие:
- веррукозная гиперплазия;
- плоская папиллома;
- остроконечные кондиломы;
- плоскоклеточная карцинома или SCC in situ.
Обычно ядерной атипии нет, но возможен спектр диспластических изменений. Можно увидеть картину от дисплазии низкой степени до высокой степени и даже плоскоклеточный рак in-situ. Следовательно, ороговевшая плоскоклеточная метаплазия, хотя и не является предраковым поражением как таковым, предположительно предопухолевое состояние. Однако из-за редкости в мочевом пузыре, а также ступенчатого развития от метаплазии через дисплазию и карциному in situ в инвазивную карциному, его труднее идентифицировать, чем, например, в шейке матки.
Чем опасна лейкоплакия
В настоящее время обсуждается естественный анамнез, прогноз и терапевтические последствия плоскоклеточной метаплазии мочевого пузыря. Плоскоклеточный рак наиболее часто ассоциируется с неоплазией, и, по оценкам, риск развития рака мочевого пузыря составляет от 21% до 42% при данной патологии. Поэтому большинство авторов признают ее пренеопластическим заболеванием, особенно когда поражение сохраняется с течением времени и поражает более 50% поверхности мочевого пузыря.
Кроме того, в тех случаях, когда такая метаплазия ассоциируется с клеточной дисплазией, градация поражения достигает доинвазивного статуса. Всякий раз, когда метаплазия обнаруживается в переходноклеточных карциномах и недифференцированных карциномах, это означает худший прогноз. Метаплазия также связана с развитием сморщенного мочевого пузыря, особенно при длительно персистирующих поражениях.
Увеличение активности рецептора эпителиального фактора роста (EGFR) было зарегистрировано в тех плоскоклеточных карциномах, которые были связаны с предшествующей плоскоклеточной метаплазией мочевого пузыря. Поэтому определение EGFR было предложено в качестве скринингового маркера для выявления плоскоклеточных поражений, а также возможной терапевтической мишени в будущем.
Диагностика ороговевающей метаплазии мочевыводящих путей/мочевого пузыря
Диагностика лейкоплакии уротелия комплексная и включает:
- Осмотр уролога (сбор анамнеза, в том числе семейного, физикальный осмотр, выяснение жалоб, направление на дальнейшее обследование);
- Анализ мочи общий (специфических изменений нет, но могут обнаруживаться лейкоциты, ороговевшие чешуйки, эритроциты);
- Культуральное исследование (посев) мочи выполняется для определения наличия/отсутствия бактериальной инфекции и чувствительности возбудителя к препаратам. Возбудителя можно быстро и точно установить с помощью ПЦР, но чувствительность к лекарствам можно узнать только при культуральном исследовании;
- Тестирование на ИППП (методами ПЦР);
- Сонографию – УЗИ органов мочевыводящей системы и малого таза, проводится обязательно, поскольку относится к информативным методам, позволяющим не только оценить строение органов, но и установить различные отклонения (камни, полипы, опухоли и т.д.);
- Цистоскопию, относится к золотому стандарту, позволяет осмотреть состояние органов и состояние слизистой “изнутри” и провести биопсию. Во время цистоскопии на стенке мочевого пузыря видны шелушащиеся белые образования в виде бляшек или пятна. Отмечается отсутствие заметных грубых изменений эпителиального слоя мочевого пузыря. Уротелий может казаться бледнее и толще, чем обычно, с неровными границами и окружающей зоной эритемы;
- Биопсию, которая необходима, чтобы провести подробный гистологический анализ для подтверждения диагноза ороговевающей плоскоклеточной метаплазии уротелия и одновременно исключения других патологий, в первую очередь злокачественных.
![]() Тестирование на ИППП – метод ПЦР
Тестирование на ИППП – метод ПЦР
Дифференциальный диагноз ороговевающей метаплазии уротелия
Дифференциальная диагностика лейкоплакии мочевыводящих путей проводится в отношении:
- малакоплакии мочевого пузыря;
- неопухолевые хронические гранулематозные поражения из-за хронической инфекции Escherichia coli у пациентов с ослабленным иммунитетом, обычно при наличии сахарного диабета или у реципиентов трансплантата;
- переходноклеточной карциномы;
- туберкулезного уретрита;
- мультифокальные или длинные стриктуры;
- обычно наблюдается обызвествление;
- кистозного уретрита;
- реактивные пролиферативные изменения уротелия, вызывающие множественные небольшие субэпителиальные кисты;
- веррукозной карциномы – хорошо дифференцированная опухоль с широким инвазивным ростом;
- плоскоклеточного рака (почечная лоханка, мочеточник и мочевой пузырь) – наблюдаются выраженная атипия, кровоизлияние, некроз;
- плоскоклеточной дисплазии – присутствует атипия клеток;
- карциномы уротелия in situ, наблюдается выраженная атипия при гистологии (но может быть неполной).
![]() Карцинома уротелия in situ
Карцинома уротелия in situ
Лечение лейкоплакии уротелия
Несмотря на то, что возможно спонтанное восстановление слизистой оболочки мочевого пузыря от плоскоклеточной метаплазии, обычным подходом является трансуретральная резекция мочевого пузыря.
Терапевтическое лечение ороговевшей плоскоклеточной метаплазии является спорным, и в настоящее время для ее лечения не существует эффективной медикаментозной терапии. Медицинские методы, такие как пероральный прием витамина А, введение нитрата серебра или уксусной кислоты в мочевой пузырь, были опробованы, но каких-либо многообещающих результатов не отмечено. Антибиотики применяются только при выраженном воспалении, назначаются с учетом чувствительности и курсом. Они могут вызывать симптоматическую ремиссию, но не вызывают объективных изменений при плоскоклеточной метаплазии.
Применяется терапевтическое лечение с помощью инстилляций гиалуроновой кислоты, в некоторых случаях наблюдается улучшение, но результаты спорны. В настоящее время необходимы дальнейшие исследования, чтобы сформулировать адекватную методику терапевтического лечения этого необычного поражения слизистой оболочки мочевого пузыря.
Поскольку терапевтическое лечение пока не увенчалось успехом и недостаточно эффективно, фактически, пациенты подвергаются трансуретральной резекции, и во избежание цистэктомии требуется мультидисциплинарный подход. В последующем для определения наличия дисплазии должна выполняться ежегодная цистоскопия с множественными биопсиями. Такой ежегодный мониторинг необходим для ранней диагностики плоскоклеточной карциномы, а также визуализации верхней мочевой системы для выявления возможных осложнений, связанных с кератинизацией мочевого пузыря.
![]() Цистоскопия
Цистоскопия
Радикальная цистэктомия предлагается в случаях втягивания мочевого пузыря, прогрессирования заболевания или у пациентов с ожидаемой продолжительностью жизни более 10 лет. Плоскоклеточный рак, который ассоциируется с ороговевающей плоскоклеточной метаплазией, часто диагностируется на поздних стадиях, обычно не поддается лечению трансуретральным доступом. В этих случаях, проводится радикальная цистэктомия, прогноз плоскоклеточного рака может быть сходен с прогнозом обычной уротелиальной карциномы с онкоспецифической выживаемостью 57% через 5 лет.
Рекомендации для профилактики поражений уротелия
Таким образом, лейкоплакия мочевыводящих путей и мочевого пузыря в первую очередь считается предшествующим неоплазии или пренеопластическим поражением. Оно нуждается в особом наблюдении как из-за его потенциальной злокачественности, так и из-за возможных осложнений, вызванных прогрессирующей кератинизацией.
Учитывая, что воспалительные и инфекционные процессы предрасполагают, считаются возможными причинами метапластических изменений уротелия, рекомендуется использовать барьерные методы контрацепции, практиковать моногамные отношения и незамедлительно обращаться к урологу при первых признаках ИППП.
При наличии раздражителей мочевого пузыря, например, катетеров, камней или перенесенных операций, рекомендуется регулярное профилактическое обследование у уролога с применением УЗИ и цистоскопии.
Источник