Эректильная функция после удаления мочевого пузыря
Содержание статьи
Радикальная цистэктомия
Основное лечение мышечно-инвазивного рака мочевого пузыря является хирургическое удаление мочевого пузыря.
Причины при которых может рекомендоваться удаление всего пузыря:
- Наличие мышечно-инвазивной опухоли
- Наличие опухоли, которая агрессивно растет, которая имеет множественные злокачественные очаги (мультифокальная) или поверхностная, но имеет рецидивы после химиотерапии или иммунотерапии
- Наличие постоянных болей и кровотечения у пациентов с неизлечимым заболеванием.
Оценить риск удаления мочевого пузыря, можно путем прохождения медицинской комиссии в составе (например, уролог, онколог, хирург, анестезиолог, терапевт).
Важны также такие факторы, как ваш биологический возраст (общесоматическое состояние, ваше самочувствие, измеряемое как состояние работоспособности или ожидаемая продолжительность жизни) и другие заболевания, которые у вас имеются (диабет, сердечные заболевания, гипертоническая болезнь и т.д.). Пациенты старше 80 лет труднее переносят такие операции и имеют более длительный восстановительный период.
Ранние операции на брюшной полости или лучевая терапия затрудняют хирургическое вмешательство, но редко являются причиной отказа от хирургического вмешательства. Избыточный вес не влияет на выживание после операции, но влияет на риск осложнений в послеоперационном периоде.
Удаление мочевого пузыря включает удаление мочевого пузыря, нижний отдел мочеточников и тазовых лимфатических узлов. В зависимости от таких факторов, как расположение опухоли и метод дальнейшего отведения мочи, часть прилежащих половых органов (простата и семенные пузырьки у мужчин, вся уретра, матка у женщин) удаляются.
Как проводится удаление мочевого пузыря?
Удаление мочевого пузыря осуществляется через разрез в брюшной полости (открытый) пациент под общей анестезией (сочетание внутривенных препаратов и ингаляционных газов). Мочевой пузырь, нижний отдел мочеточников, расположенные близко к мочевому пузырю, тазовые лимфатические узлы и (часть) прилежащих половые органы удаляются. Теперь должен быть сформирован другой метод хранения и отведения мочи.
Стандартная методика на данный момент — открытая хирургия. Тем не менее, это может быть сделано менее инвазивно (лапароскопическая или роботизированная хирургия). В настоящее время в специализированных центрах, имеющих специальное оборудование и опытных специалистов, малоинвазивные операции считаются методом выбора для удаления мочевого пузыря.
Как подготовиться к процедуре?
При поступлении в стационар врач информирует вас о том, как нужно готовиться до и что делать после операции.
Часть вашей кишки будет использоваться для создания мочевого резервуара. Врач подробно объяснит, как подготовиться к данной процедуре.
Перед операцией врач подробно проинформирует вас о том, как подготовиться к анестезии. Если вы принимаете какие-либо лекарственные препараты, сообщите об этом своему врачу. Возможно, потребуется отмена некоторых препаратов за несколько дней до операции.
В течение первых нескольких дней вы находитесь под динамическим наблюдением. Врач подробно проинформирует вас о послеоперационном периоде.
Во время госпитализации вы узнаете, как обращаться с уростомой. После того, как вы научитесь использовать и опорожнять уростому, будет установлена дата выписки.
Химиотерапия перед удалением мочевого пузыря
Химиотерапию проводят перед удалением мочевого пузыря, чтобы потенциально уменьшить опухоль и убить опухолевые клетки, которые уже проникли в кровь или лимфатические узлы.
Химиотерапию перед операцией можно рекомендовать пациентам с мышечно-инвазивной формой. Это также необходимо, при опухолях большого размера (> 3 см) или если есть признаки распространения рака на лимфатические узлы (метастазы). Решение о проведении химиотерапии принимается врачебной комиссией (включая онколога, уролога и радиолога). Необходима адекватная функция почек.
Положительная реакция на химиотерапию улучшает выживаемость, но не исключает необходимость хирургического вмешательства.
Химиотерапия после удаления мочевого пузыря
Если опухоль большая (> 3 см), не может быть полностью удалена или распространяется на лимфатические узлы (определяется патологоанатомом), показана химиотерапия после удаления мочевого пузыря. Рак, который распространился на лимфатические узлы, указывает на системное заболевание и может потребоваться системное лечение (с химиотерапией) в определенных случаях.
Отведение мочи: недержание или удержание.
Важно понять двухэтапный подход к удалению мочевого пузыря. Сначала удаляют мочевой пузырь и лимфатические узлы. Затем, мочу нужно отвести. Это может быть достигнуто несколькими способами. Вообще мы различаем варианты, которые являются недержанием (непрерывный поток мочи сразу выходит за пределы тела), и удержание (моча, хранится в организме и отводится при необходимости). Биологический возраст, функция почек и другие заболевания, качество жизни пациента имеют решающее значение при выборе тактики операции. Чтобы определиться, какой вариант лучше подходит в вашей конкретной ситуации, вы должны знать и понимать ограничения после каждого вида операции и побочные эффекты.
В дополнение к вашим личным предпочтениям важна способность физически и морально привыкнуть, и уметь обращаться с таким отведением мочи.
Перемещение мочеточников
Выведение мочеточников через кожу (уретерокутанеостомия).
Перемещая мочеточники или вместе или отдельно через кожу сбоку живота для отведения мочи от почек (стома) (рис.1), моча может просто вытекать через стому в мешок. Это отведение мочи является самым простым. Хотя он редко используется. Данный метод безопасен и доступен для пациентов, с отягощенным анамнезом (предшествующие операции, множественные проблемы со здоровьем, паллиативный уход) или у пациентов, которые не могут позаботиться о себе после операции. Основные осложнения встречаются редко, однако рецидивирующие инфекции и затягивание отверстия (стеноз) являются общими и могут потребовать лечения. Пациентам часто необходимо стентирование мочеточника, который необходимо регулярно менять.
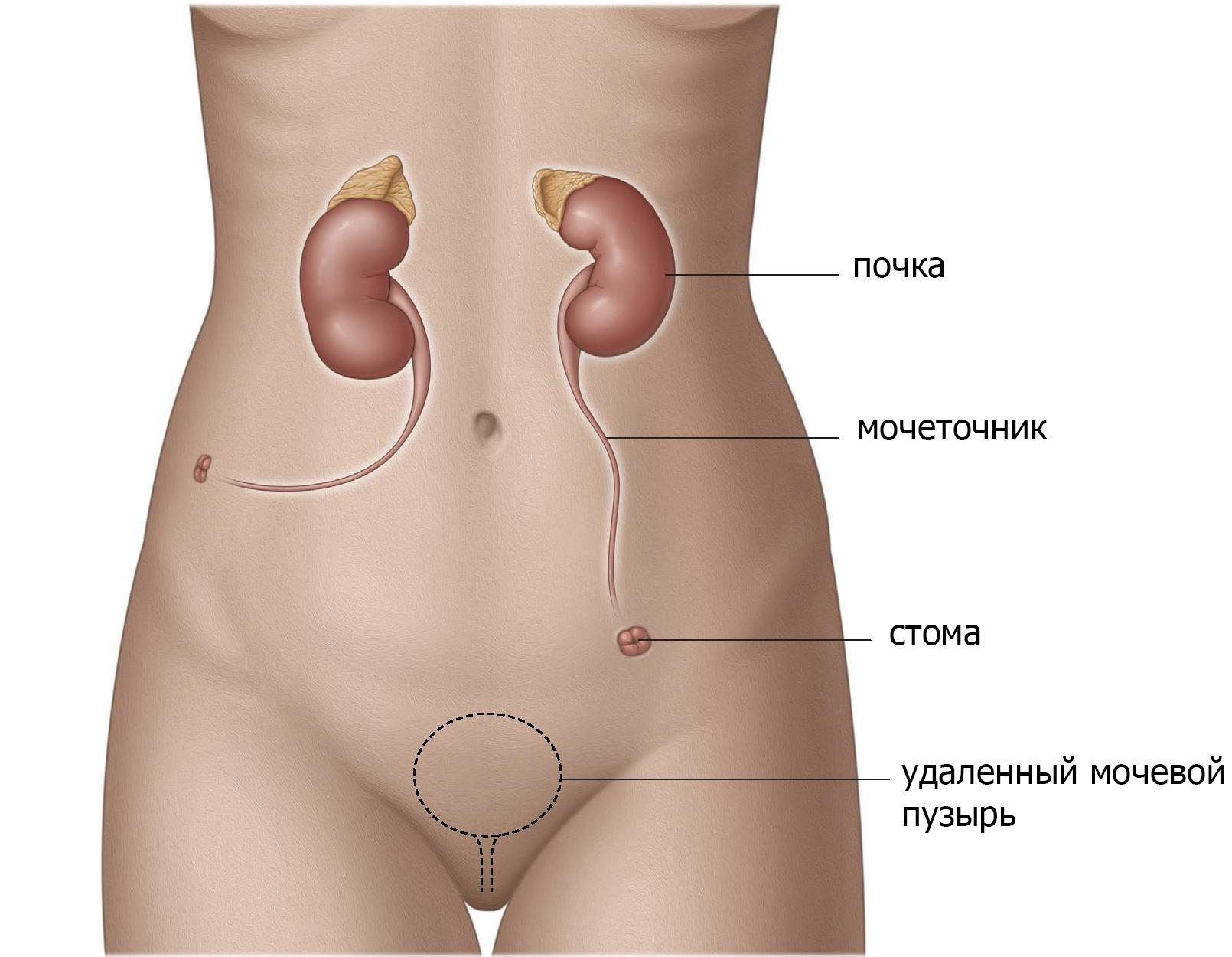
Рис. 1 уретерокутанеостома
Установить часть тонкой кишки между мочеточниками и кожей (подвздошный канал).
Подвздошный канал можно создать, поместив тонкую кишку между мочеточниками и кожей (рис.2). Эта «кишечная стома» создает большее расстояние между почками и кожей и снижает риск инфицирования. Другим преимуществом для пациентов является то, что эта стома легче обрабатывается и имеет меньше осложнений, таких как сужение выводного отверстия (стеноз). Данная операция технически относительно проста и надежна и поэтому является наиболее часто используемой.
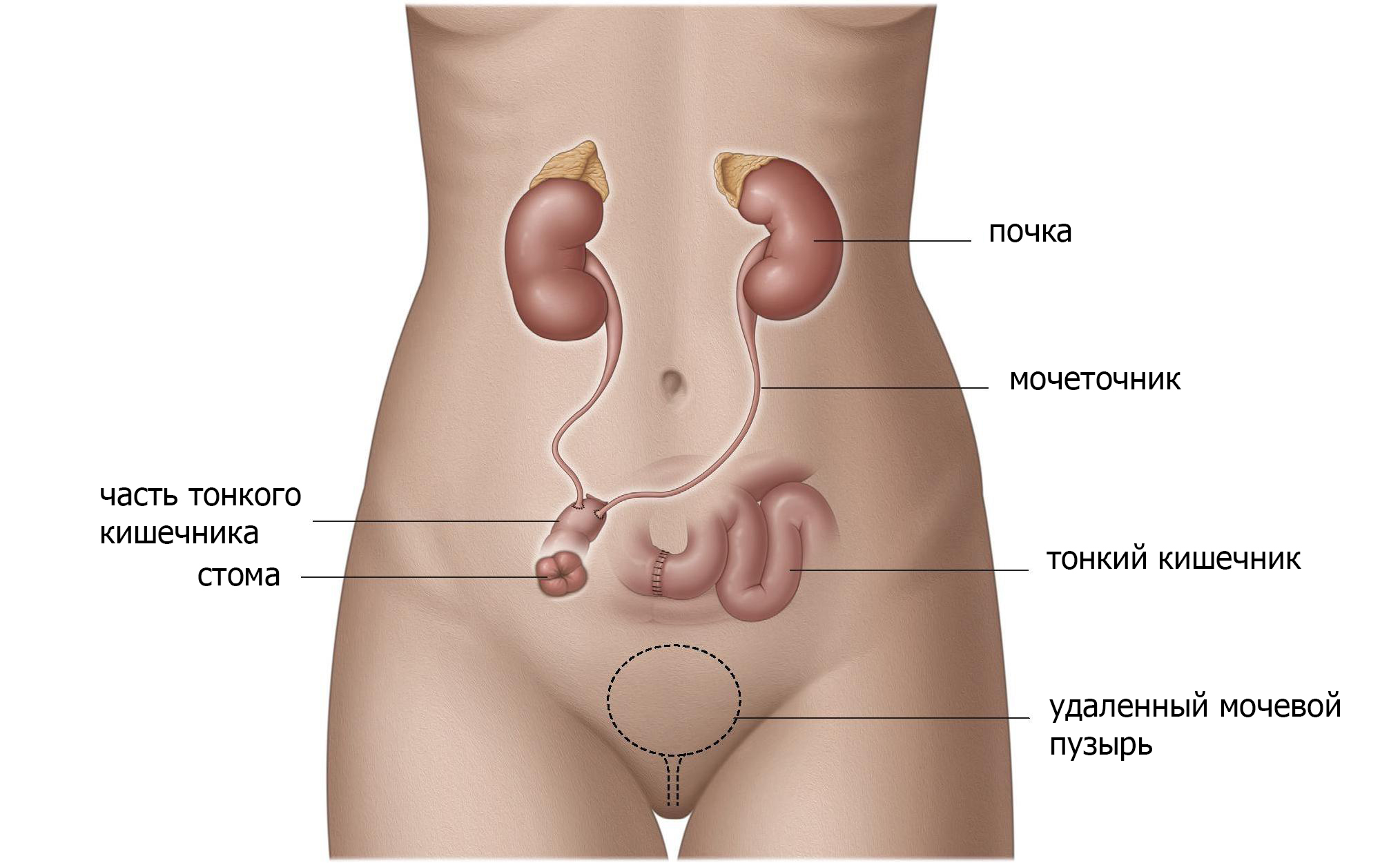
Рис. 2 Подвздошный канал
Выбирая данный вид отведения мочи, вы должны знать, что привыкнуть к жизни со стомой требует много времени и усилий.
Вновь сформированный мочевой пузырь. Создание резервуара внутри тела
Используя тонкую кишку или толстую кишку, а иногда и аппендикс, создается резервуар в брюшной полости, а затем соединяется с кожей с помощью клапанного механизма (рис. 3). С таким резервуаром низкого давления, моча может быть сохранена в теле. Цель этой процедуры — позволить контролировать опорожнение или обратный поток мочи в почки (рефлюкс). Резервуар опорожняется прерывистой катетеризацией небольшим пластиковым катетером каждые 2-6 часов. Отверстие может находиться где угодно на нижней части живота или в пупке.
Если выбран данный вид операции, вам потребуется регулярно катетеризировать и опорожнять данный резервуар. Функция печени и почек должна быть адекватной из-за реабсорбции мочевых компонентов (соли, мочевой кислоты, воды) в кишечной оболочке резервуара, что вызывает дополнительную нагрузку на эти органы.
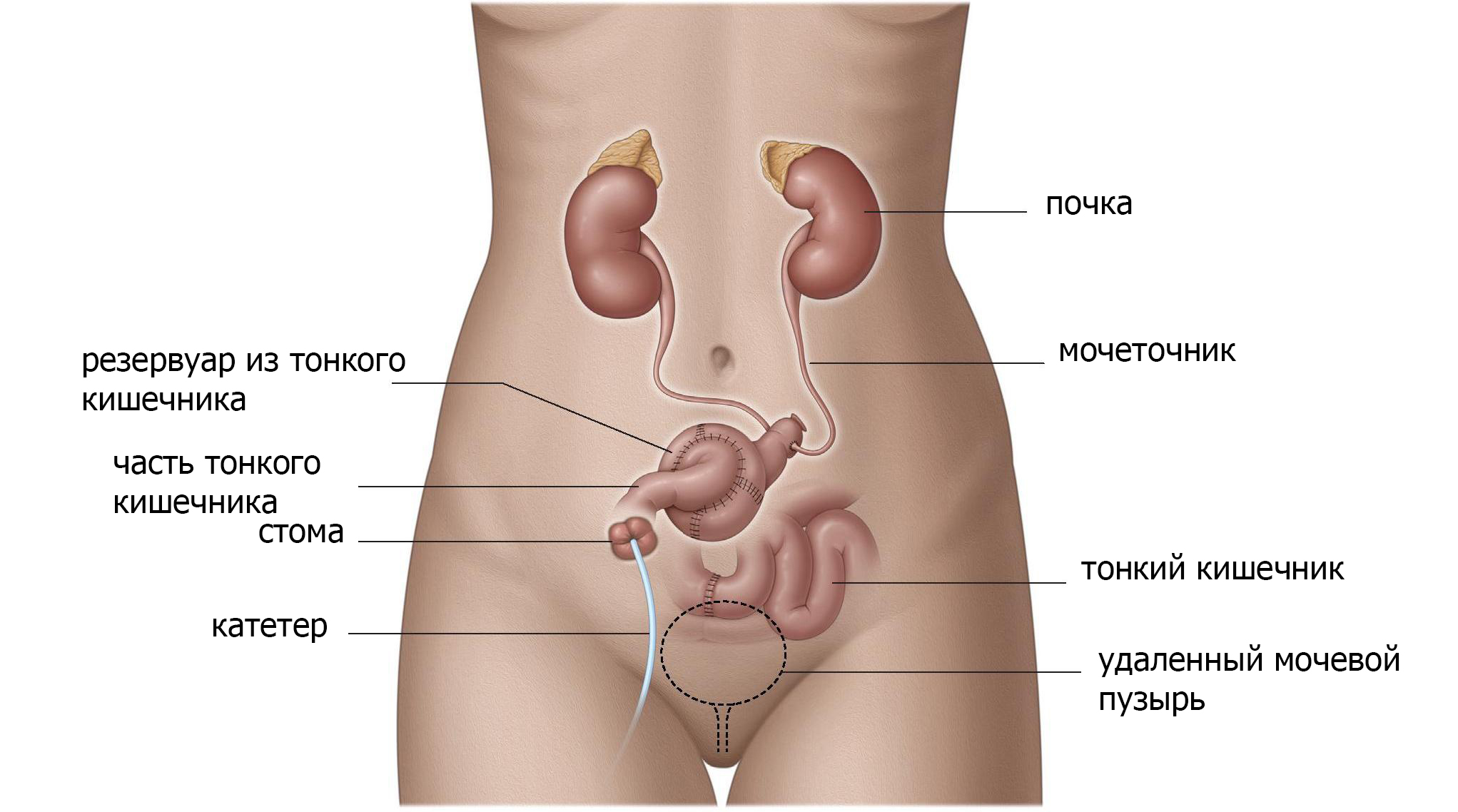
Рис. 3 Резервуар из кишечника
Осложнения включают инфекции, недержание мочи, грыжу, рефлюкс, затягивание отверстия (стеноз), а также синдром короткой кишки, метаболический и электролитный дисбаланс.
Поскольку эта операция имеет технические сложности, особенно при создание клапанного механизма, который не всегда бывает удачным, данный метод используется редко.
Имплантация мочеточников в прямую кишку (уретероректонеостомия)
Когда мочеточники имплантируют в прямую кишку, моча хранится в ампуле прямой кишки (рис.4). Анальное отверстие и тазовое дно становятся органом удерживающим мочу и должны функционировать должным образом. Данный вид отведения приводит к смешиванию фекалий с мочой, поэтому опорожнение и дефекация происходят одновременно. Этот метод имеет высокий уровень инфецирования, поэтому используется редко и только при определенных обстоятельствах. Краткосрочные осложнения включают повторяющиеся инфекции (включая воспаление брюшной стенки и почек), затягивание отверстия в прямой кишке (стеноз). Долгосрочные осложнения включают недержание мочи, раздражение кишечника и связанный с этим рак толстой кишки.
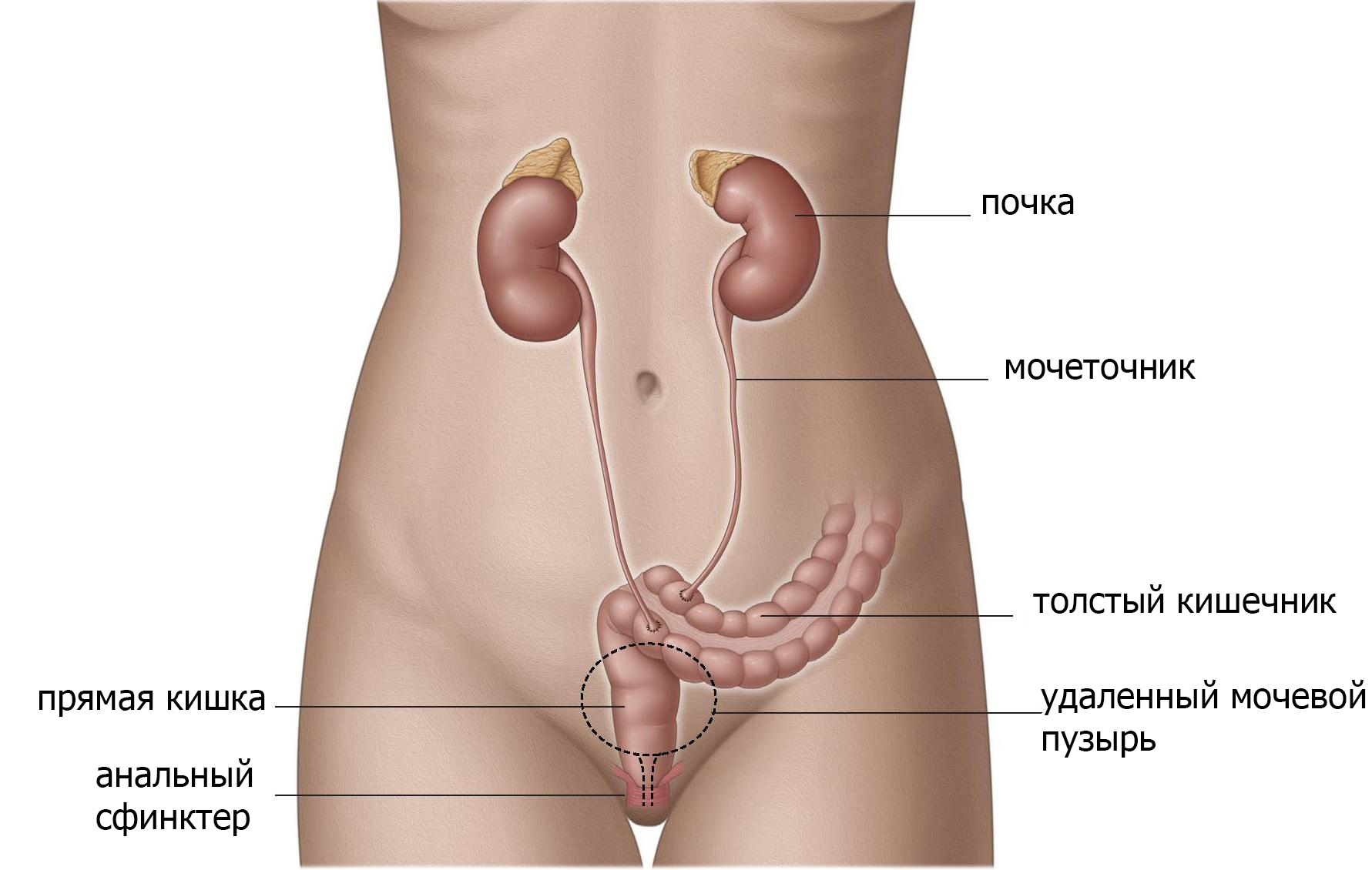
Рис. 4 Уретероректонеостома
Формирование мочевого пузыря из тонкой кишки
Новый мочевой пузырь может быть сформирован из тонкой кишки, которая изолируется от пищеварительного тракта (рис.5). Резервуар сформирован из тонкого кишечника и помещен в малый таз в качестве замены мочевого пузыря. В зависимости от используемой методики резервуар имеет сфероидальную форму, «W» или «V». Мочеточники прикреплены с обеих сторон, а нижний конец соединен с уретрой. Мочевой сфинктер сохраняется. При данный виде операции моча должна накапливаться а затем выводиться наружу как и при здоровом мочевом пузуре.
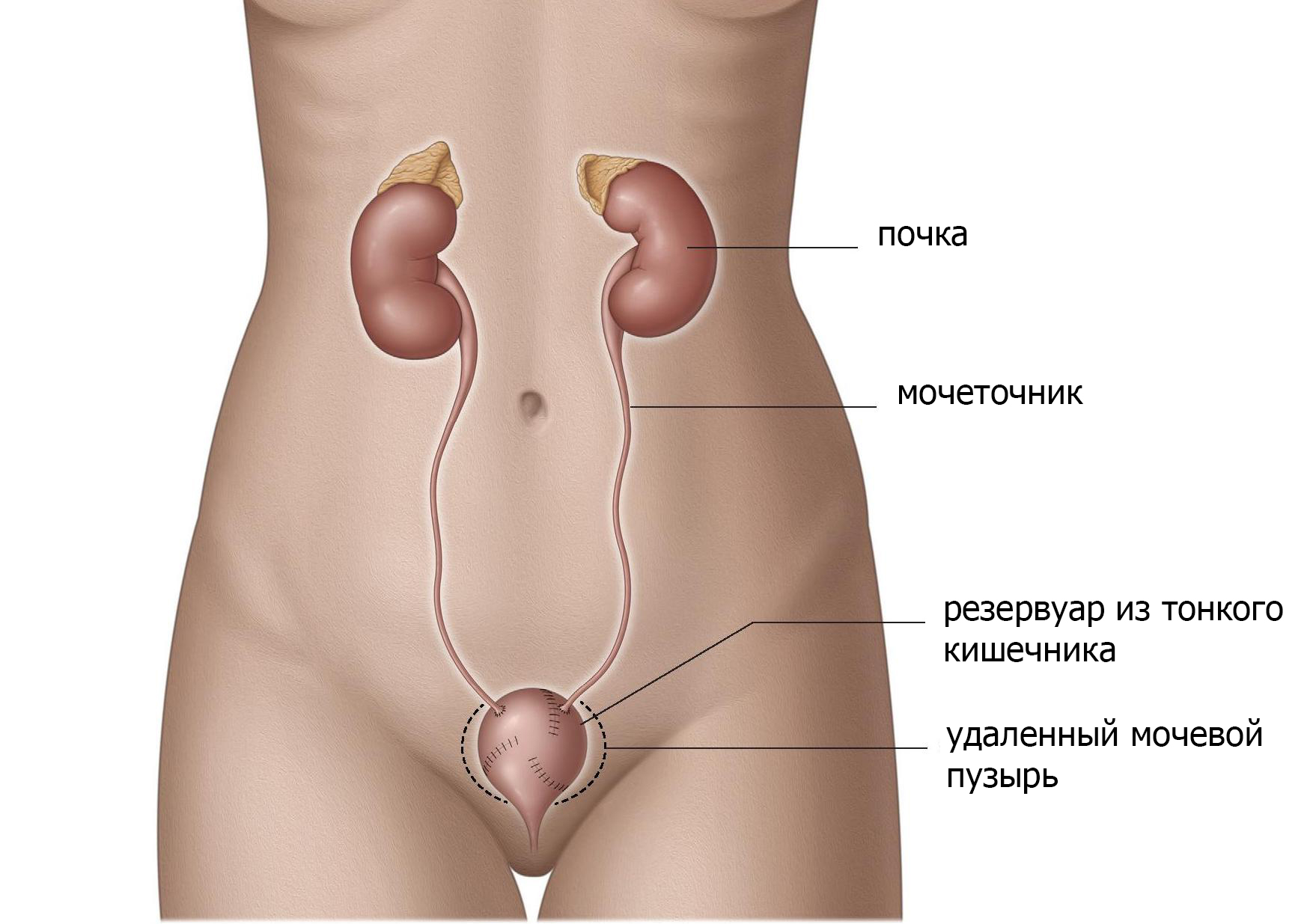
Рис. 5 мочевой пузырь из тонкой кишки
Вы не почувствуете наполнения мочевого пузыря или позыв к мочеиспусканию с пузырем из тонкого кишечника, поэтому опорожнение необходимо проводить каждые 2-4 часа. Пузырь освобождается, расслабляя мышцы тазового дна и сокращая брюшную полость (метод Вальсальвы). Нажатие на живот обеими руками может помочь для полного опорожнения. У 20% женщин необходимо выполнять периодическую самокатетеризацию для полного опорожнения, у мужчин этого не требуется.
При данном виде операции требуется удовлетворительная функция почек и печени, нормальное состояние мышц тазового дна. Осложнения после данного вмешательства включают в себя повторяющиеся инфекции (включая воспаление брюшной стенки и почек) и недержание мочи.
Долгосрочные осложнения включают затягивание отверстия в области анастамоза, изменения верхних мочевых путей, недержание мочи, синдром короткой кишки и грыжу, а также метаболический и электролитный дисбаланс.
Регулярный анализ крови поможет оценить количество мочевой кислоты которая реабсорбируется используемым участком кишечника, вызывая дисбаланс pH, который часто требует медикаментозного лечения пероральными препаратами (бикарбонат натрия — пищевая сода).
Для вновь образованного резервуара требуется время для его укрепления и начала работы. Для увеличить емкость сформированного пузыря, вам нужно будет его тренировать. Врач предоставит вам инструкции по тренировке мочевого пузыря. В начале недержание мочи может случиться из-за послеоперационного отека тазового дна.
Источник
Динамика качества жизни после хирургии стриктуры уретры у мужчин
Б.Г. Амирбеков, М.И. Коган, В.В. Митусов, З.А. Мирзаев, М.В. Костеров
ФГБОУ ВО «Ростовский государственный медицинский университет» МЗ РФ; Ростов-на-Дону, Россия
Введение
За последние годы были достигнуты серьезные успехи, как в лечении, так и в диагностике пациентов со стриктурами уретры (СУ). Широко внедрены в клиническую практику новые реконструктивно-пластические операции, позволяющие восстанавливать проходимость мочеиспускательного канала у мужчин при его сужениях и облитерациях в любых отделах и различной протяженности [1-6].
Однако, до настоящего времени, сохраняется целый ряд нерешенных вопросов, особенно затрагивающих реабилитацию пациентов со стриктурной болезнью, после выполнения у них успешных хирургических операций, в частности, такой вопрос, как восстановление эректильной функции [7-11].
При стриктурной болезни эректильные расстройства у мужчин в первую очередь связаны с поражением пенильных сосудов, ответственных за эректильную функцию, что резко ухудшает качество жизни больного, усугубляемое отсутствием самостоятельного мочеиспускания и наличием цистостомы [12-14].
Возможен и другой механизм развития эректильных расстройств у этой категории пациентов, когда нарушение гемодинамики полового члена обусловлено возникновением кавернозного фиброза и спонгиофиброза, что наиболее характерно для воспалительных стриктур уретры [15, 16].
Причинами возникновения эректильной дисфункции (ЭД) могут быть и эндокринные расстройства, где главная роль принадлежит тестостерону [17-20].
Следует подчеркнуть, что тестостерон играет важную роль в функционировании различных органов и систем организма мужчин, а его дефицит может оказывать серьезное влияние как на течение раневого процесса при хирургии различных урологических и неурологических заболеваний, тем самым определяя качество жизни пациентов в отдалённом послеоперационном периоде [21, 22].
По нашему мнению, помимо оценки мочеиспускания и эректильной функции после успешной операции по поводу СУ представляется важным определять и ментальное здоровье пациентов.
Исходя из вышеперечисленного, целью исследования явилось изучение распространённости тревоги и депрессии на фоне СНМП и эректильных расстройств у мужчин при стриктурной болезни до операции по поводу СУ и после ее успешного проведения в динамике.
Материалы и методы
Исследования основано на клинико-статистическом анализе 70 мужчин в возрасте 20-74 лет, которые проходили лечение по поводу стриктур уретры. Этиологическим фактором образования СУ явились травма — 51 (72,8%) воспаление — 16 (22,9%) и идопатический фактор — 3 (4,3%). При госпитализации у 51,4% больных было сохранено самостоятельное мочеиспускание, а в 48,6% деривация мочи осуществлялась через цистостому. 36 больных, которые мочились самостоятельно имели следующие СНМП: слабо выраженные — 3 случая (8,3%), умеренные — 17 (47,3%) и выраженные в 16 наблюдениях (44,4%).
При изучении нарушений сексуальной и эректильной функции у пациентов до операции было установлено, что у 46 мужчин (65,7%) из 70 имели место сексуальные расстройства и эректильная дисфункция, возникновение, которых больные связывали с наличием у них СУ.
Показатели тестестеронемии у больных до операции верифицировали в 20% как гипогонадный и в 80% как нормогонадный статус.
Все 70 человек оперированы, в 35 случаях выполнена первичная хирургия, а в 35 случаях — повторная.
Динамику качества жизни у ранее пролеченных больных определяли через 3 и 6 месяцев после операции по показателям урофлоуметрии, проявлениям СНМП, сексуальным расстройствам и эректильной дисфункции, изменению психоэмоционального статуса по шкалам тревоги и депрессии НADS 1, 2. Полученные данные сравнивали с аналогичными до хирургии СУ.
Статистическую обработку результатов исследований проводили по средним значениям и среднеквадратичным ошибкам и непараметрического критерия статистики (Хи-квадрат) для сравнения малых выборок. Для определения статистических различий количественных показателей использовали t-критерий Стьюдента и критерий Манна-Уитни с использованием общепринятых уровней значимости: p <0,05; p <0,01 и p <0,001.
Результаты и обсуждения
Известно, что любое хирургическое вмешательство сопровождается раневыми осложнениями. Исходя из этого, нами были оценены риски возникновения раневых осложнений у оперированных больных с учетом их возраста, этиологии болезни, кратности выполнения операции и типом самого вмешательства.
Оказалось, что риск развития раневых осложнений у гипогонадных мужчин старше 40 лет в 4 раза выше, чему эугонадных. Такойже риск имеет место у пациентов моложе 40 лет с дефицитом тестостерона и число возникающих осложнений у них в 4 раза выше, чем у эугонадных пациентов.
Риски раневых осложнений зависят также и от этиологии СУ. Установлено, что раневые осложнения у гипогонадных мужчин с травматическими СУ в 4,9 раза выше, чем у нормогонадных больных. Вероятность развития раневых осложнений при первичных операциях при гипогонадном статусе в 3,7 раза выше, чем у мужчин с нормогонадным статусом.
Таблица 1. Результаты хирургического лечения СУ через 3 месяца
| Показатели | Резекция уретры (n=52) | Аугментационная уретропластика буккальным трансплантатом | |
| одноэтапная (n=3) | двухэтапная(n=15) | ||
| Урофлоуметрия | 13,9 мл/сек | 11,5 мл/сек | 12,8 мл/сек |
| Опросник IPSS отсутствие симптомов лёгкая умеренная тяжёлая симптоматика | 6 (11,5%) 30 (57,7%) 16 (30,8%) — | 2 (66,7%) 1 (33,3%) — — | 3 (20%) 7 (46,7%) 5 (33,3%) — |
| Оценка качества жизни (шкала Qol) вследствие расстройств мочеиспускания хорошее удовлетворительное плохое | 17 (32,7%) 24 (46,1%) 11 (21,1%) | 1 (33,3%) 2 (66,7%) — | 8 (53,3%) 4 (26,7%) 3 (20%) |
| УЗИ мочевого пузыря (объём остаточной мочи >50 мл) | 5 (9,6%) | 1 (33,3%) | 3 (20%) |
| Восходящая уретроцистография с выявлением стенозирования уретры | 3 (5,8%) | 1 (33,3%) | 4(26,7%) |
| Необходимость выполнения повторных операций | — | — | — |
Раневые осложнения и их связь с типом операции установлены у пациентов, которым выполнялась резекция уретры. Причем эти риски в 4,7 раза выше при гипогонадизме, чем у нормогонадных пациентов.
Тем не менее, все оперированные больные были выписаны из клиники с восстановленным мочеиспусканием естественным путем.
Таким образом, гипотестостеронемия достоверно повышает риски послеоперационных раневых осложнений, на что по нашим данным, оказывают влияние возраст больных, этиология СУ, вид хирургического лечения и его кратность.
Оценка эффективности выполненной хирургии по поводу СУ согласно клиническим рекомендациям РОУ и EAU проводится в сроки 3 и 6 месяцев с момента ее проведения.
В таблицах 1, 2 представлены показатели стандартных шкал опросников, которые были использованы для оценки вышеперечисленных параметров.
Таблица 2. Результаты хирургического лечения СУ через 6 месяцев
| Показатели | Резекция уретры (n=52) | Аугментационная уретропластика буккальным трансплантатом | |
| одноэтапная (n=3) | двухэтапная(n=15) | ||
| Урофлоуметрия | 14,2 мл/сек | 12,8 мл/сек | 13,1 мл/сек |
| Опросник IPSS отсутствие симптомов лёгкая умеренная тяжёлая симптоматика | 17 (32,7%) 29 (55,8%) 6 (11,5%) | 1 (33,3%) 2 (66,7%) | 7 (46,7%) 5 (33,3%) 3 (20%) |
| Оценка качества жизни (шкала Qol) вследствие расстройств мочеиспускания хорошее удовлетворительное плохое | 37 (71,1%) 13 (25%) 2 (3,8%) | 1 (33,3%) 2 (66,7%) | 11 (73,3%) 2 (13,3%) 2 (13,3%) |
| УЗИ мочевого пузыря (объём остаточной мочи >50 мл) | 3 (5,8%) | 1 (33,3%) | 2 (13,3%) |
| Необходимость выполнения повторных операций рецидив СУ уретро-кожный свищ | 2 (13,3%) | ||
Установлено, что скорость мочеиспускания у оперированных больных не зависит от вида хирургии СУ и соответствует нормативным значениям. Оценка этого показателя в динамике к 6-м месяцам указывает на его увеличение, что связано с завершением процессов воспаления в уретре и отсутствием клинических проявлений рецидива заболевания.
С точки зрения доказательной медицины эффективность и положительный результат любой реконструктивной хирургии определяется целым рядом параметров. Хирургическое лечение СУ так же должно оцениваться с этих позиций. Наиболее важными критериями благоприятного исхода хирургического лечения СУ, по нашему мнению, следует считать: 1) ликвидация или минимизация СНМП;2) восстановление сексуальной функции у мужчины; 3) максимальное купирование состояний тревоги и депрессии у больного, обусловленных наличием болезни.
Такой комплексный клинико-статистический анализ соотношения этих показателей между собой нами был проведен на 30 больных, которые после хирургии СУ не имели никаких осложнений.
В таблицах 3-5, представлены показатели стандартных шкал опросников, которые были использованы для оценки вышеперечисленных параметров.
Таблица 3. Данные опроса больных по анкетам до операции
| Шкала оценки | Число больных | min значение | max значение | Средняя величина | Отклонения | Симптоматика в баллах |
| IPSS | 12* | 35 | 18,67 | ± 8,9 | 0-7 — лёгкая 8-19 — умеренная 20-35 — тяжёлая | |
| Qol | 30 | 1 | 6 | 5,37 | ± 1,2 | 0-6 — от прекрасно (0 баллов) до очень плохо (6 баллов) |
| АИОМС | 30 | 12 | 105 | 52,93 | ± 18,6 | < 68 — гипо 68-102 — норма > 102 — гипер |
| IIEF-5 | 30 | 5 | 20 | 12,47 | ± 4,1 | 5-10 — тяжёлая 11-15- умеренная 16-20 — лёгкая 21-25 — норма |
| HADS 1 | 30 | 18 | 8,30 | ± 4,9 | 0-7 — норма 8-10 — субклинич. ≥ 11 — клиническ. | |
| HADS 2 | 30 | 20 | 8,03 | 8,03 | 0-7 — норма 8-10 — субклинич. ≥ 11 — клиническ. |
Примечание. Здесь и в таблицах 4-5: IPSS — международная система суммарной оценки симптомов болезней предстательной железы; Qol — оценка качества жизни вследствие расстройств мочеиспускания; АИОМС — анкета интегральной оценки мужской сексуальности; IIEF-5 — международный индекс эректильной функции; HADS 1, 2 — госпитальная шкала тревоги и депрессии.
Таблица 4. Данные опроса мужчин по анкетам через 3 месяца после операции
| Шкала оценки | Число больных | min значение | max значение | Средняя величина | Отклонения | Симптоматика в баллах |
| IPSS | 30 | 2 | 11 | 5,73 | ± 2,7 | 0-7 — лёгкая 8-19 — умеренная 20-35 — тяжёлая |
| Qol | 30 | 1 | 4 | 1,87 | ± 0,8 | 0-6 — от прекрасно (0 баллов) до очень плохо (6 баллов) |
| IIEF-5 | 30 | 5 | 21 | 12,67 | ± 4,0 | 5-10 — тяжёлая 11-15 — умеренная 16-20 — лёгкая 21-25 — норма |
| HADS 1 | 30 | 3 | 15 | 7,20 | ± 3,2 | 0-7 — норма 8-10 — субклинич. ≥ 11 — клиническ. |
| HADS 2 | 30 | 2 | 15 | 7,57 | ± 3,3 | 0-7 — норма 8-10 — субклинич. ≥ 11 — клиническ |
Как видно из таблиц 3-5, на протяжении 6 месяцев отмечается стойкое снижение среднего значения показателей по шкалам IPSS и Qol. Так, средний балл IPSS снизился с 18,67 до 5,73 через 3 месяца (р0,1).
В отличие от положительной динамики по шкале IPSS, прирост баллов по шкале IIEF-5 был крайне слабо выражен. Среднее значение этого показателя незначительно растёт с 12,47 (до операции) до 12,67 через 3 месяца после выполнения операции и до 13,57 — через 6 месяцев. Различия являются статистически незначимыми (р>0,1).
Существенная положительная динамика эффективно проведенного хирургического лечения СУ была достигнута по оценке тревожных и депрессивных расстройств. Так, средний балл шкалы HADS 1 (тревоги), составлявший 8,3 до операции, через 3 месяца снизился до 7,2 (р>0,1) и 5,23 — по прошествии 6 месяцев после операции (р0,1) и до 5,47 — через 6 месяцев после операции (р<0,01).
Таким образом, эффективная хирургия СУ приводит к достоверной и выраженной редукции СНМП, но не сопровождается значимым снижением тяжести ЭД, даже через 6 месяцев при отсутствии ее лечения, что в реальной клинической практике требует углубленного обследования причин ее сохранения и выбора методики лечения, что может привести к купированию симптомов тревоги и депрессии у пациентов и стабилизации их социального статуса.
Таблица 5. Данные опроса мужчин по анкетам через 6 месяцев после операции
| Шкала оценки | Число больных | min значение | max значение | Средняя величина | Отклонения | Симптоматика в баллах |
| IPSS | 30 | 1 | 8 | 4,53 | ± 2,3 | 0-7 — лёгкая 8-19 — умеренная 20-35 — тяжёлая |
| Qol | 30 | 1 | 4 | 1,60 | ± 0,8 | 0-6 — от прекрасно (0 баллов) до очень плохо (6 баллов) |
| IIEF-5 | 30 | 5 | 22 | 13,57 | ± 4,1 | 5-10 — тяжёлая 11-15 — умеренная 16-20 — лёгкая 21-25 — норма |
| HADS 1 | 30 | 2 | 12 | 5,23 | ± 2,4 | 0-7 — норма 8-10 — субклинич. ≥ 11 — клиническ. |
| HADS 2 | 30 | 2 | 10 | 5,47 | ± 2,0 | 0-7 — норма 8-10 — субклинич. ≥ 11 — клиническ |
Заключение
Успешность хирургического лечения СУ ассоциируется с быстрой и достоверной редукцией СНМП на протяжении 6 месяцев послеоперационного мониторинга. Однако, существенная позитивная динамика СНМП не сопровождается значимым снижением тяжести ЭД. Послеоперационный регресс тревоги/депрессии доказательно связан исключительно с инволюцией СНМП, но не ЭД. Гипотестостеронемия тормозит снижение уровней тревоги и депрессии, в сравнении с нормогонадными мужчинами.
У 56,6% больных со СБУ до оперативного лечения имеют симптомы тревоги и депрессии, в 46,7% случаях — тревоги и в 43,3% — депрессии. Нарушения ментального статуса регрессируют в течение 6 месяцев после успешного хирургического лечения, однако сохраняются у 23,3% мужчин в виде симптомов тревоги и у 10% — в виде депрессии.
Совокупность оценки СНМП, ЭД и тревоги/ депрессии в среднесрочном и отдалённом периодах после оперативного лечения СУ целесообразно рассматривать как трифекту результатов хирургии СБУ.
Литература
- Zaid UB, Lavien G, Peterson AC. Management of the Recurrent Male Urethral Stricture. Curr Urol Rep. 2016;17(4):33. DOI: 10.1007/s11934-016-0588-0
- Kulkarni S, Kulkarni J, Surana S, Joshi PM. Management of Panurethral Stricture. Urol Clin North Am. 2017;44(1):67-75. DOI: 10.1016/j.ucl.2016.08.011
- Hillary CJ, Osman NI, Chapple CR. Current trends in urethral stricture management. Asian J Urol. 2014;1(1):46-54. DOI: 10.1016/j.ajur.2015.04.005
- Глухов В.П., Красулин В.В. Резекция уретры с концевым анастомозом при хирургическом лечении осложнённых стриктур уретры у мужчин. Кубанский научный медицинский вестник. 2009;4(109):78-82. eLIBRARY ID: 12955466
- Коган М.И., Глухов В.П., Митусов В.В., Красулин В.В., Ильяш А.В. Сравнительный анализ одно- и двухэтапной аугментационной дорсальной inlay-пластики буккальным графтом протяжённых стриктур спонгиозной уретры. Урология. 2018;1:84-91. DOI: 10.18565/ urol.2018.1.84-90
- Глухов В.П. Резекция уретры с концевым анастомозом при осложнённых стриктурах и облитерациях уретры у мужчин: Автореферат дис. … канд. мед. наук. СанктПетербург; 2010. Доступно по: https://medical-diss.com. Ссылка активна на 03.04.2019.
- Ибишев, X.С., Маркарьян Д.Р. Нарушение эректильной функции у пациентов с травмами уретры. Актуальные проблемы хирургии: II науч.-практ. конф. каф. хирург. бол. 4; 2005; Ростов н/Д. eLIBRARY ID: 15861900
- Коган М.И. Эректильная дисфункция (текущее мнение). М.: Боргес; 2016. eLIBRARY ID: 29982783
- Koraitim MM. Predictors of erectile dys post pelvic fracture urethral injuries: a multivariate analysis. Urology. 2017;81:1081-1085. DOI: 10.1016/j.urology.2012.12.040
- Xambre L. Sexual (Dys) aŌ er Urethroplasty. Sexual Urol. 2016;9671297. DOI:10.1155/2016/9671297
- Dogra PN, Singh P, Nayyar R, Yadav S. Sexual Dys AŌ er Urethroplasty. Urol Clin North Am. 2017;44(1):49-56. DOI:10.1016/j.ucl.2016.08.013
- Buckley JC, Heyns C, Gilling P, Carney J. SIU/ICUD Consultation on Urethral Strictures: Dilation, internal urethrotomy, and stenting of male anterior urethral strictures. Urology. 2014;83(3):18-22. DOI: 10.1016/j.urology.2013.08.075
- Коган М.И., Красулин В.В., Митусов В.В., Шангичев А.В., Глухов В.П., Наранов С.В. Оперативное лечение стриктур и облитераций уретры. Урология. 2015;2:17-23. eLIBRARY ID: 23608496
- Goksu C, Deveer M, Sivrioglu AK, Goksu P, Cucen B, Parlak S, Cetinkaya M, Altin L. Peripheral atherosclerosis in patients with arterial erectile dys. Int J Impot Res. 2014;26(2):55-60. DOI: 10.1038/ijir.2013.35
- Ибишев X.С. Морфологические изменения в кавернозной ткани полового члена у пациентов с травмой уретры. Известия высших учебных заведений. Северо-кавказский регион. Серия: естественные науки. 2006;8:77-82. eLIBRARY ID: 9209411
- Ravikumar BR, Tejus C, Madappa KM, Prashant D, Dhayanand GS. A comparative study of ascending urethrogram and sono-urethrogram in the evaluation of stricture urethra. Int Braz J Urol. 2015;41(2):388-392. DOI: 10.1590/S1677- 5538.IBJU.2015.02.30
- Гамидов С.И. Научные и практические аспекты диагностики и лечения эректильной дисфункции у пациентов с гипогонадизмом. Эффективная фармакотерапия. 2016;41:36-38. eLIBRARY ID: 28368704
- Ворник Б.М. Тестостерон и депрессия: парадоксы и закономерности. XVI съезд психиатров России. Всероссийская научно-практическая конференция с международным участием «Психиатрия на этапах реформ: проблемы и перспективы»; 2015; Санкт-Петербург. eLIBRARY ID: 27619659
- Коган М.И., Воробьев С.В., Хрипун И.А., Белоусов И.И., Ибишев Х.С. Тестостерон: от сексуальности к метаболическому контролю. М.: Феникс; 2017. eLIBRARY ID: 32822129
- Corona G, Maggi M. The role of testosterone in erectile dys. Nat Rev Urol. 2010;7(1):46-56. DOI: 10.1038/ nrurol.2009.235
- Пушкарь, Д.Ю., Живов А.В., Багаудинов М.Р., Исмаилов М.Р.М. Качество жизни мужчин после различных операций по поводу стриктуры уретры. Экспериментальная и клиническая урология. 2012;4:48-52. eLIBRARY ID: 18348721
- Lucas ET, Koff WJ, Rosito TE, Berger M, Bortolini T, Neto BS. Assessment of satisfaction and Quality of Life using self -reported questionnaires after urethroplasty: a prospective analysis. Int Braz J Urol. 2017;43(2):304-310. DOI: 10.1590/ S1677-5538.IBJU.2016.0207
Статья опубликована в журнале «Вестник урологии» №2 2019, стр. 5-13
Источник