Измерение белка в моче с сульфосалициловой кислотой
БЕЛОК В МОЧЕ АГАТ
по применению набора реактивов для определения белка в моче с сульфосалициловой кислотой
НАЗНАЧЕНИЕ
Диагностический набор предназначен для количественного определения содержания белка в моче по помутнению, образовавшемуся при добавлении сульфосалициловой кислоты. Для клинико-диагностических и биохимических лабораторий. Набор рассчитан на 660 определений при расходе 3,0 мл раствора сульфоофосалициловой кислоты на один анализ.
ПРИНЦИП МЕТОДА
Интенсивность помутнения при коагуляции белка сульфосалициловой кислотой, измеренная по оптической плотности при 620 нм, пропорциональна его концентрации. Калибровка осуществляется по раствору человеческого сывороточного альбумина.
СОСТАВ НАБОРА
1. 5-сульфосалициловая кислота, дигидрат, 30 г — 2 упаковки;
2. Калибровочный раствор альбумина 1000 мг/л, 10 мл — 1 флакон.
МЕРЫ ПРЕДОСТОРОЖНОСТИ
Сульфосалициловая кислота — едкое вещество. В случае попадания раствора на кожу и (или) слизистые необходимо сразу же промыть пораженное место большим количеством воды. Пипетирование per os категорически запрещается. Другие компоненты набора в используемых концентрациях являются нетоксичными. При работе с сывороткой или плазмой крови необходимо соблюдать правила техники безопасности принятые в лаборатории, т.к. образцы человеческой крови следует рассматривать как потенциально инфицированые.
ОБОРУДОВАНИЕ И РЕАГЕНТЫ
— Спектрофотометр, длина волны 620 нм или фотоэлектроколориметр, длина волны 590-650 нм (оранжевый или красный светофильтр), кювета с толщиной поглощающего свет слоя 10 мм;
— пипетки, позволяющие отбирать объемы жидкости от 0,25 до 5,0 мл; — пробирки вместимостью 5,0-10 мл;
— колба мерная вместимостью 1000 мл;
— секундомер;
— вода дистиллированная;
— раствор натрия хлористого, 9 г/л;
— перчатки резиновые или пластиковые.
АНАЛИЗИРУЕМЫЕ ОБРАЗЦЫ
Моча профильтрованная.
ПОДГОТОВКА РЕАГЕНТОВ ДЛЯ АНАЛИЗА
Раствор сульфосалициловой кислоты. Содержимое одной упаковки (30 г) с сульфосалициловой кислотой количественно переносят в мерную колбу вместимостью 1000 мл, растворяют в дистиллированной воде и доводят объем до метки. Раствор стабилен.
ПРОВЕДЕНИЕ АНАЛИЗА
В пробирки вносят реактивы по следующей схеме:
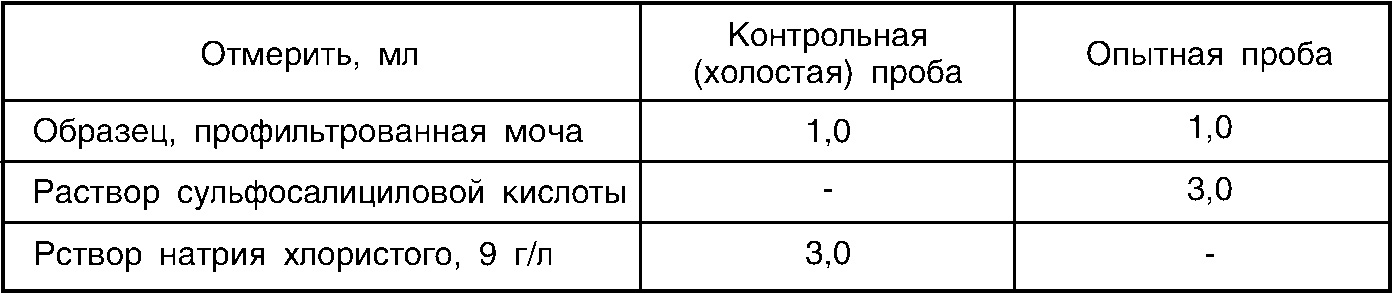
Содержимое пробирок тщательно перемешивают и выдерживают при температуре +18-22° С в течение 10 минут. Определяют оптическую плотность опытной пробы при длине волны 620 нм (590-650 нм, оранжевый или красный светофильтр) против холостой пробы в кювете с толщиной слоя 10 или 5 мм. При стоянии образцов более 20 минут возможно уменьшение значений оптической плотности за счет оседания части преципитата. Непосредственно перед измерением пробирку с опытной пробой тщательно встряхнуть. Расчет проводят по калибровочному графику.
Построение калибровочного графика
Для построения калибровочного графика из калибровочного раствора альбумина и 9 г/л раствора натрия хлористого готовят следующие разведения:
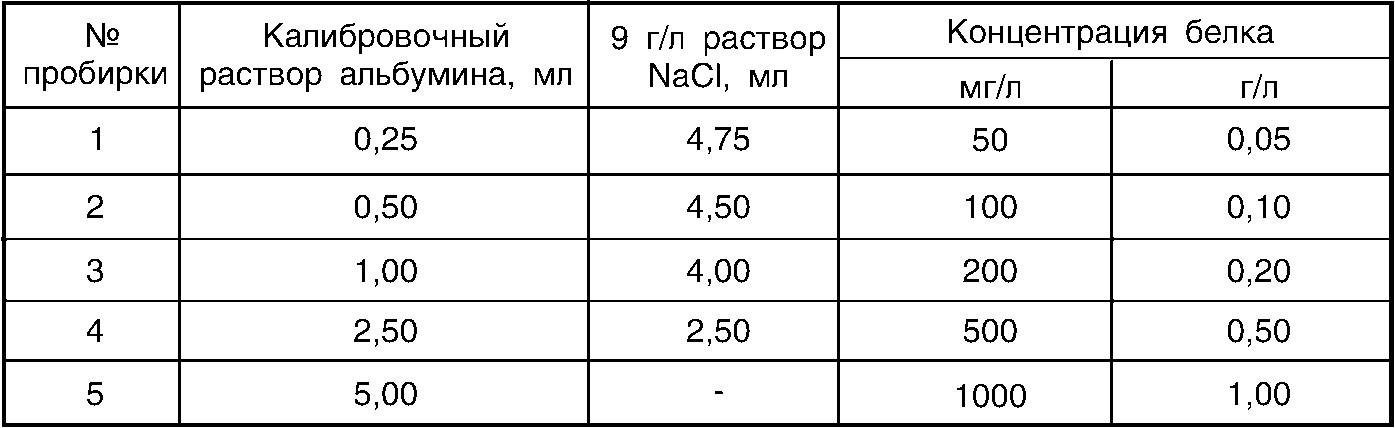
Полученные разведения обрабатывают так же, как и образец.
Примечания: Линейная зависимость сохраняется до концентрации белка 1 г/л. При более высоких концентрациях пробу следует развести в 2-3 раза, результат умножить на разведение. Результаты, получаемые данным методом чувствительны к изменениям температуры. Рекомендуется производить измерения при температуре +18-22° С. Ложноположительные результаты могут быть получены при наличии в моче контрастных веществ, содержащих органический йод. Поэтому тест нельзя использовать у лиц, принимающих препараты йода. Ложноположительный тест может быть также обусловлен приемом сульфаниламидных препаратов, больших доз пенициллина и при высоких концентрациях в моче мочевой кислоты.
УСЛОВИЯ ХРАНЕНИЯ И ЭКСПЛУАТАЦИИ
Набор следует хранить в упаковке предприятия-изготовителя при температуре +2-8° С в течение всего срока годности. Срок годности набора — 2 года.
Литература: Лабораторные методы исследования в клинике. Под редакцией проф. В.В. Меньшикова, М., 1987, с. 49.
По вопросам, касающимся приобретения наборов и их качества, просим обращаться по адресу: 105173, г. Москва, ул. Западная, д. 2, стр. 1, ООО «Агат-Мед». Телефон для справок: (495) 777-41-92.
Инструкция составлена: к.б.н. И.В. Смирновым — зав. лабораторией ГНЦ РАМН, В.В. Гладуном — главным технологом ООО «Агат-Мед».
Источник
Белок в моче – методы определения и границы нормы (современное состояние проблемы)
ЮНИТЕКА:
Анализ мочи:
26.02.2009
Куриляк О.А., к.б.н.
В норме белок выделяется с мочой в относительно небольшом количестве, обычно не более 100-150 мг/сут.
Суточный диурез у здорового человека составляет 1000-1500 мл/сут; таким образом, концентрация белка в физиологических условиях составляет 8-10 мг/дл (0,08-0,1 г/л).
Общий белок мочи представлен тремя основными фракциями — альбуминами, мукопротеинами и глобулинами.
Альбумин мочи — это та часть альбумина сыворотки крови, которая была профильтрована в клубочках и не была реабсорбирована в почечных канальцах; в норме экскреция альбумина в моче составляет менее 30 мг/сут. Иным главным источником белка в моче служат почечные канальцы, особенно дистальная часть канальцев. Эти канальцы секретируют две третьих общего количества мочевого белка; из этого количества примерно 50% представлено гликопротеидом Тамма‑Хорсфалла, который секретируется эпителием дистальных канальцев и играет важную роль в формировании мочевых камней. Иные белки присутствуют в моче в незначительном количестве и происходят из профильтровавшихся через почечный фильтр низкомолекулярных белков плазмы, которые не реабсорбируются в почечных канальцах, микроглобулинов из эпителия почечных канальцев (RTE), а также простатического и влагалищного отделяемого.
Протеинурия, то есть увеличение содержания белка в моче — один из наиболее значимых симптомов, отражающий поражение почек. Однако и целый ряд других состояний также может сопровождаться протеинурией. Поэтому различают две основные группы протеинурий: почечную (истинную) и внепочечную (ложную) протеинурию.
При почечной протеинурии белок проникает в мочу непосредственно из крови вследствие повышения проницаемости гломерулярного фильтра. Почечная протеинурия часто встречается при гломерулонефрите, нефрозе, пиелонефрите, нефросклерозе, амилоидозе почек, различных формах нефропатий, например нефропатии беременных, лихорадочных состояниях, гипертонической болезни и т.д. Протеинурия может обнаруживаться и у здоровых людей после тяжелых физических нагрузок, переохлаждения, психологического стресса. У новорожденных в первые недели жизни наблюдается физиологическая протеинурия, а при астении у детей и подростков в сочетании с быстрым ростом в возрасте 7-18 лет возможна ортостатическая протеинурия (в вертикальном положении тела).
При ложной (внепочечной) протеинурии источником белка в моче является примесь лейкоцитов, эритроцитов, клеток эпителия мочевых путей уротелия. Распад этих элементов, особенно резко выраженный при щелочной реакции мочи, приводит к попаданию белка в мочу, уже прошедшую почечный фильтр. Особенно высокую степень ложной протеинурии дает примесь крови в моче, при профузной гематурии она может достигать 30 г/л и более. Заболевания, которые могут сопровождаться внепочечной протеинурией — мочекаменная болезнь, туберкулез почки, опухоли почки или мочевых путей, циститы, пиелиты, простатиты, уретриты, вульвовагиниты.
Клиническая классификация включает легкую протеинурию (менее 0,5 г/сут.), умеренную (от 0,5 до 4 г/сут.), или тяжелую (более 4 г/сут.).
У большинства пациентов с заболеваниями почек, такими, как острый гломерулонефрит или пиелонефрит выявляют умеренную протеинурию, но больные с нефротическим синдромом обычно выделяют с мочой более 4 г белка ежедневно.
Для количественного определения белка применяется широкий спектр методов, в частности, унифицированный метод Брандберга-Робертса-Стольникова, биуретовый метод, метод с применением сульфосалициловой кислоты, методы с использованием красителя кумасси синий, красителя пирогаллоловый красный и др.
Использование различных методов определения белка в моче привело к тому, что в трактовке границ нормы содержания белка в моче возникла серьезная путаница. Поскольку наиболее часто в лабораториях используются 2 метода — с сульфосалициловой кислотой и красителем пирогаллоловый красный, рассмотрим проблему корректности границ норм именно для них. С позиции сульфосалицилового метода в нормальной моче содержание белка не должно превышать 0,03 г/л, с позиции же пирогаллолового — 0,1 г/л! Различия троекратные!!!
Низкие значения нормы концентрации белков в моче при использовании сульфосалицилового обусловлены следующими моментами:
- калибровочная кривая строится по водному раствору альбумина. Моча по своему составу очень сильно отличается от воды: рН, соли, низкомолекулярные соединения (креатинин, мочевина и др). Вследствие этого по данным Альтшулера, Ракова и Ткачева ошибка определения белка в моче может быть 3-х кратной и более! Т.е. корректные результаты определения могут быть получены только в тех случаях, когда моча имеет очень низкий удельный вес и по своему составу и рН приближается к воде;
- более высокая чувствительность сульфосалицилового метода к альбумину в сравнении с другими белками (в то время, как было упомянуто выше, альбумин в нормальных образцах мочи составляет не более 30% от общего белка мочи);
- если pH мочи сдвинута в щелочную сторону, происходит нейтрализация сульфосалициловой кислоты, что так же является причиной занижения результатов определения белка;
- скорость седиментации преципитатов подвержена значительной вариации — при невысоких концентрациях белка преципитация замедлена, и ранняя остановка реакции приводит к занижению результата;
- скорость реакции преципитации существенно зависит от перемешивания реакционной смеси. При высоких концентрациях белка активное встряхивание пробирки может приводить к образованию крупных хлопьев и их быстрому осаждению.
Все выше перечисленные особенности метода и приводят к значительному занижению определяемой в моче концентрации белка. При этом степень занижения сильно зависит от состава конкретной пробы мочи. Поскольку метод сульфосалициловой кислоты дает заниженные значения концентрации белка то и граница нормы для этого метода 0,03 г/л тоже занижена примерно в три раза в сравнении с данными, которые приводятся в зарубежных справочниках по клинической лабораторной диагностике.
Подавляющее большинство лабораторий западных стран отказались от применения сульфосалицилового метода для определения концентрации белка в моче и активно используют для этих целей пирогаллоловый метод. Пирогаллоловый метод определения концентрации белка в моче и других биологических жидкостях основан на фотометрическом принципе измерения оптической плотности окрашенного комплекса, образующегося при взаимодействии молекул белка с молекулами комплекса красителя пирогаллоловый красный и молибдата натрия (Pyrogallol Red-Molyb complex).
Почему пирогаллоловый метод позволяет получать более точные результаты измерения концентрации белка в моче? Во-первых, за счет большей кратности разведения пробы мочи в реакционной смеси. Если в сульфосалициловом методе отношение проба мочи/реагент составляет 1/3, то в пирогаллоловом методе оно может быть в пределах от 1/12,5 до 1/60 в зависимости от варианта методики, что значительно уменьшает влияние состава мочи на результат измерения. Во-вторых, реакция протекает в сукцинатном буфере, то есть при стабильном рН. И, наконец, сам принцип метода, можно сказать, более «прозрачный». Молибдат натрия и краситель пирогаллоловый красный образуют комплекс с молекулой белка. Это приводит к тому, что молекулы красителя в свободном состоянии не поглощающие свет на длине волны 600 нм в комплексе с белком свет поглощают. Таким образом, мы как бы метим каждую молекулу белка красителем и в результате получаем, что изменение оптической плотности реакционной смеси на длине волны 600 нм четко коррелирует с концентрацией белка в моче. Причем, поскольку сродство пирогаллолового красного к разным фракциям белка практически одинаковое, метод позволяет определять общий белок мочи. Поэтому граница нормальных значений концентрации белка в моче составляет 0,1 г/л (она и указана во всех современных западных руководствах по клинико-лабораторной диагностике, в том числе и в «Клиническом руководстве по лабораторным тестам», под ред. Н. Тица). Сравнительные характеристики пирогаллолового и сульфосалицилового методов определения белка в моче представлены в Таблице 1.
В заключение, хотелось бы еще раз акцентировать внимание на том факте, что при переходе лаборатории с сульфосалицилового метода определения белка в моче на пирогаллоловый метод граница нормальных значений существенно повышается (с 0,03 г/л до 0,1г/л!). Об этом сотрудники лаборатории должны непременно поставить в известность врачей-клиницистов, т.к. при сложившейся ситуации диагноз протеинурия может быть поставлен только в том случае, когда содержание белка в моче превышает 0,1 г/л.
Список литературы.
- Альтшулер Б.Ю., Раков С.С., Ткачев Г.А. // Вопр. мед. химии. — 2001. — № 4. — C.426-438.
- Ким Ю.В., Потехин О.Е., Токар М.И., Шибанов А.Н. // Лаб. мед. — 2003. — № 6. — C.94-98.
- Клиническое руководство по лабораторным тестам, под ред. Н. Тица.- М.- Юнимед-пресс.-2003.- 942 с.
- Козлов А.В., Слепышева В.В. Методы определения белка в моче: возможности и перспективы // Сборник трудов VII ежегод. СПб нефрол. семинара. — СПб: ТНА. — 1999. — C.17-28.
- Пупкова В.И., Пикалов И.В., Хрыкина Е.Н., Харьковский А.В. // Новости «Вектор-Бест». — 2003. — № 4 (30).
- Chambers R.E., Bullock D.G., Whicher J.T. // Ann. Clin. Biochem. — 1991. — Vol. 28 (Pt 5). — P.467-473.
- Clinical Laboratury Medicine. Ed. by Kenneth D. McClatchey. — 2nd ed.-2001.- 1993p.
- Eppel G.A., Nagy S., Jenkins M.A., Tudball R.N., Daskalakis M., Balazs N.D.H., Comper W.D. // Clin. Biochem. — 2000. — Vol. 33. — P.487-494.
- Franke G., Salvati M., Sommer R.G. Composition and device for urinary protein assay and method of using the same // ПатентСША № 5326707. — 1994.
- Kaplan I.V., Levinson S.S. // Clin. Chem. — 1999. — Vol. 45. — P.417-419.
- Kashif W., Siddiqi N., Dincer H.E., Dincer A.P., Hirsch S. // Cleveland Clin. J. of Med. — 2003. — Vol. 70 (6). — P.535-547.
- Koerbin G, Taylor L, Dutton J, Marshall K, Low P, Potter JM. // Clin. Chem. — 2001. — Vol. 47. — P.2183-2184.
- Le Bricon T., Erlich D., Dussaucy M., Garnier J.P., Bousquet B. // Article in French. — Ann. Biol. Clin. (Paris). — 1998. — Vol. 56 (6). — P.719-723.
- Marshall T., Williams K.M. // Clin. Chem. — 2003. — Vol. 49 (12). — P.2111-2112.
- Pugia M., Newman D.J., Lott J.A., D’Mello L., Clark L., Profitt J.A., Cast T. // Clin. Chim. Acta. — 2002. — Vol. 326 (1-2). — P.177-183.
- Ringsrud K.M., Linne J.J. Urinalysis and body fluids: A ColorText and Atlas // Mosby. — 1995. — P.52-54.
- Shepard M.D., Penberthy L.A. // Clin. Chem. — 1987. — Vol. 33. — P.792-795.
- Williams K.M., Marshall T. // J. Biochem. Biophys. Methods. — 2001. — Vol. 47. — P.197-207.
- Williams K.M., Arthur S.J., Burrell G., Kelly F., Phillips D.W., Marshall T. // J. Biochem. Biophys. Methods. — 2003. — Vol. 57 (1). — P.45-55.
Теги:
Источник
Методическая разработка практического занятия «Определение белка в моче» (1 курс)
Занятие №3.
Тема: Определение белка в моче.
Цель: Изучить исследование химических свойств мочи.
Задачи:
Изучить количественные и качественные методы определения белка в моче;
Изучить основные принципы работы с тест-полосками на автоматических анализаторах.
Тип занятия: практическое (6ч)
Планируемые результаты:
Студент должен знать:
Качественные пробы для определения белка.
Метод Робертса — Стольникова.
Определение белка 3 % ССК.
Биуретовый метод определения белка (ТХУ).
Диагностическое значение исследования показателей.
Виды протеинурий.
Студент должен уметь:
Подготовить рабочее место к исследованию мочи.
Приготовить реактивы, посуду и оборудование к исследованию.
Определять химические свойства мочи (белок в моче качественными и количественными методами).
Работать с бланочной продукцией (оформление бланков анализа).
Правильно интерпретировать полученные результаты исследования.
Средства достижения поставленной цели:
1. Работа с конспектами, учебной и специальной литературой.
2. Подготовка к практическим занятиям с использованием методических рекомендаций преподавателя, выполнение и оформление практических работ.
3. Работа с информационными средствами обучения на электронных и бумажных носителях.
Оборудование учебного кабинета и рабочих мест кабинета:
посадочные места по количеству обучающихся;
рабочее место преподавателя;
специализированная мебель и оборудование.
Технические средства обучения:
компьютеры для оснащения рабочего места преподавателя и обучающихся;
технические устройства для аудиовизуального отображения информации;
аудиовизуальные средства обучения (презентация, учебный видеосюжет).
Результатом освоения урока является:
Формирование практических профессиональных умений и первоначального практического опыта, в том числе профессиональными (ПК) и общими (ОК) компетенциями:
ПК 1.1. Готовить рабочее место для проведения лабораторных общеклинических исследований.
ПК 1.2. Проводить лабораторные общеклинические исследования биологических материалов.
ПК 1.3. Регистрировать результаты проведенных исследований.
ПК 1.4. Проводить утилизацию отработанного материала, дезинфекцию и стерилизацию использованной лабораторной посуды, инструментария, средств защиты.
ОК 1. Понимать сущность и социальную значимость своей будущей профессии, проявлять к ней устойчивый интерес.
ОК 2. Организовывать собственную деятельность, выбирать типовые методы и способы выполнения профессиональных задач, оценивать их эффективность и качество.
ОК 6. Работать в коллективе и команде, эффективно общаться с коллегами, руководством, пациентами.
ОК 9. Ориентироваться в условиях смены технологий в профессиональной деятельности.
ОК 13. Организовывать рабочее место с соблюдением требований охраны труда, производственной санитарии, инфекционной и противопожарной безопасности.
I модуль. Теоретическая часть с элементами самостоятельной работы
Задание №1. Изучите и законспектируйте учебный материал в рабочие тетради.
Моча здорового человека обычно содержит менее 0,002 г/л и редко до 0,012 г/л белка и как правило такое содержание белка в моче называют «в виде следов» и общепринятыми (унифицированными) химическими методами в моче здорового человека не определяется.
Содержание белка в порциях мочи, собранной в разное время суток, может колебаться в значительных пределах.
Появление белка в моче называется протеинурия.
В зависимости от суточной потери белка различают следующие степени протеинурии: умеренная — до 1 г; средняя — от 1 до 3 г; выраженная — более 3 г.
Существует два основных вида протеинурии:
Протеинурии, обусловленные заболеваниями мочевыводящих путей;
протеинурии, при поражениях (заболеваниях) почек.
Протеинурии, связанные с воспалительными процессами мочевыводящих путей, сопровождаются появлением в моче значительного количества лейкоцитов или эритроцитов, что, однако, не позволяет исключить одновременного попадания белка в мочу из почечной паренхимы; содержание белка редко превышает 1 г/л.
Почечная протеинурия в большинстве случаев связана с повышенной проницаемостью гломерул и делится на 2 группы:
физиологическая протеинурия;
патологическая протеинурия.
К физиологической протеинурии относят случаи временного появления белка в моче, не связанные с заболеваниями:
после приема большого количества пищи, богатой не денатурированными белками (сырое мясо, сырые яйца);
при интенсивной мышечной работе (продолжительные походы, спортивные соревнования);
при приеме холодной ванны или душа;
при сильных эмоциональных переживаниях;
при эпилептических приступах.
Различают ортостатическую, или юношескую, протеинурию, встречающуюся у детей и подростков и проходящую с возрастом. В дифференциально-диагностическом отношении имеет практическое значение то, что ортостатическая альбуминурия обнаруживается нередко в период выздоровления после острого гломерулонефрита.
Патологическая почечная протеинурия может быть следствием органических заболеваний почек и других органов и систем: острые гломерулонефриты; хронические гломерулонефриты; острые пиелонефриты; хронические пиелонефриты; нефропатии беременных; различные заболевания, сопровождающиеся лихорадкой; выраженная хроническая сердечная недостаточность; амилоидоз почек; липоидный нефроз; туберкулез почки; геморрагические лихорадки; геморрагический васкулит; выраженная анемия; гипертоническая болезнь и др.
Задание №2. Перепишите и зарисуйте схемы лабораторных методов определения белка в моче.
Лабораторные методы определения белка в моче
Существуют качественные и количественные методы определения белка в моче, они основаны на коагуляции белка в объеме мочи или на границе сред (моча и кислота); при этом измерение степени коагуляции делает пробу количественной.
Качественные методы
проба с 20% сульфосалициловой кислотой (унифицированная);
кольцевая проба Геллера (в настоящее время не используется);
обнаружение белка с помощью индикаторной бумаги (полосок) и тест-полосок.
Количественные методы
унифицированный метод Брандберга-Робертса-Стольникова;
с 3% сульфосалициловой кислотой.
Качественные методы определения белка в моче
Задание №3. Определение белка в моче с помощью унифицированной пробы с 20% сульфосалициловой кислотой
Принцип метода: основан на коагуляции белка в объеме мочи или на границе сред (моча и кислота)
Посуда, оборудование и реактивы:
20% сульфосалициловой кислоты (2-гидрокси-5-сульфобензойная кислота C7H506S).
фильтровальная бумага
3мл профильтрованной мочи
2 шт. химические пробирки
Ход исследования:
В две пробирки вносят по 3 мл профильтрованной мочи, в одну из них (опытную) прибавляют 6-8 капель сульфосалициловой кислоты. На темном фоне сравнивают обе пробирки.
Интерпретация полученных результатов:
Помутнение в опытной пробирке свидетельствует о наличии в моче белка — проба положительна.
Примечание. Мочу со щелочной реакцией перед исследованием подкисляют добавлением нескольких капель 10% раствора уксусной кислоты
Задание №4. Определение белка с помощью кольцевой пробы Геллера
Принцип метода: В основу положена кольцевая проба, заключающаяся в том, что при добавлении к моче азотной кислоты на границе сред (кислота — моча) при наличии белка происходит его коагуляция и появляется белое кольцо.
Посуда, оборудование и реактивы:
— химическая пробирка;
— реактивы: 30% раствор азотной кислоты (HNO3) (d = 1,2) или реактив Ларионовой: 20- 30 г хлорида натрия (NaCl) растворяют при нагревании в 100 мл дистиллированной воды, остужают, фильтруют; к 99 мл фильтрата приливают 1 мл концентрированной HNO3.
Ход исследования:
В пробирку наливают 1 — 2 мл 30% раствора HNO3 или реактива Ларионовой и осторожно по стенке наслаивают столько же профильтрованной мочи.
Интерпретация полученных результатов:
Появление на границе двух жидкостей между 2-й и 3-й мин тонкого белого кольца указывает на наличие белка в моче.
Зарисуйте схему определения белка
Количественное определение белка
Принцип метода: В основу положена кольцевая проба Геллера, заключающаяся в том, что при добавлении к моче азотной кислоты на границе сред (кислота — моча) при наличии белка происходит его коагуляция и появляется белое кольцо.
Посуда, оборудование и реактивы:
Химическая пробирка;
Реактив Ларионовой;
Фильтровальная бумага;
Биологическая жидкость (моча);
Дистиллированная вода.
Ход исследования:
В пробирку наливают 1 — 2 мл 30% раствора HNO3 или реактива Ларионовой и осторожно по стенке наслаивают столько же профильтрованной мочи.
Интерпретация полученных результатов:
Появление на границе двух жидкостей между 2-й и 3-й мин
тонкого белого кольца указывает на наличие белка в концентрации примерно 0,033 г/л. При появлении кольца раньше 2-х мин после наслаивания мочу следует развести дистиллированной водой и провести повторное исследование с разведенной мочой. Степень разведения мочи подбирают в зависимости от вида кольца, его ширины, компактности и времени появления.
При нитевидном кольце, появившемся ранее 2 мин, мочу разводят в 2 раза, при широком — в 4 раза, при компактном — в 8 раз и т.д. Концентрацию белка вычисляют, умножив степень разведения на 0,033 г/л.
Примечание:
Белое кольцо может образовываться при наличии большого количества уратов; в отличие от белкового оно появляется немного выше границы двух жидкостей и растворяется при легком нагревании.
Задание №6. Определение количества белка в моче с 3 % сульфосалициловой кислотой
Принцип метода: Концентрация белка в моче пропорциональна помутнению, появляющемуся при его коагуляции сульфосалициловой кислотой
Посуда, оборудование и реактивы:
3% раствор сульфосалициловой кислоты (C7H5O6S); j
0,9% раствор хлорида натрия;
1% стандартный раствор альбумина — 1 г лиофилизированного альбумина (из человеческой или бычьей сыворотки) растворяют в небольшом количестве 0,9% раствора NaCl в колбе емкостью 100 мл, а затем доводят до метки тем же растворителем. Реактив стабилизируют прибавлением 1 мл 5% раствора азида натрия (NaN3). При хранении в холодильнике реактив стабилен в течение 2 месяцев.
Ход исследования:
В пробирку вносят 1,25 мл профильтрованной мочи, добавляют 3,75 мл 3% раствора сульфосалициловой кислоты, перемешивают. Через 5 мин пробу фотометрируют на ФЭКе при длине волны 590-650 нм (оранжевый или красный светофильтр) против контроля в кювете с длиной оптического пути 5 мм. Контролем служит проба, в которой к 1,25 мл мочи добавлено 3,75 мл 0,9% раствора хлориде натрия. Концентрацию белка рассчитывают по калибровочному графику, для построение которого готовят разведения стандартного раствора альбумина (см. таблицу). Из каждого полученного разведенного раствора берут по 1,25 мл и обрабатывают, как опытные пробы.
Приготовление разведений для построения калибровочного графика
пробирки
Стандартный раствор, мл
0,9% раствор хлорида натрия, мл
Концентрация белка, г/л
1
0,05
9,95
0,05
2
0,1
9,9
0,1
3
0,2
9,8
0,2
4
0,5
9,5
0,5
5
1,0
9,0
1,0
Примечание:
Прямолинейная зависимость величины экстинкции и концентрации белка сохраняется до 1 г/л. При более высоких концентрациях белка пробу следует разводить и учитывать разведение при расчете.
При наличии в моче веществ, содержащих йод, могут быть получены ложноположительные результаты. Поэтому тест нельзя использовать у больных, принимающих препараты йода или прошедших исследование с применением йодсодержащих рентгеноконтрастных соединений. Ложноположительные J реакции при проведении исследования могут быть вызваны приемом сульфаниламидных лекарственных средств, больших доз пенициллина и при высоких концентрациях в моче мочевой кислоты.
Зарисуйте схему определения белка
Задание №7. Обнаружение в моче белка Бенс-Джонса
Принцип метода: основан на реакции термопреципитации
Посуда, оборудование и реактивы:
Реактив: 2М ацетатный буфер рН 4,9.
Профильтрованная моча;
Водянная баня.
Ход исследования:
4 мл профильтрованной мочи смешивают с 1 мл буферного раствора и нагревают 15 мин на водяной бане при температуре 56°С.
Интерпретация полученных результатов:
При наличии в моче белка Бенс-Джонса уже в первые 2 мин появляется выраженный осадок.
Примечание:
При концентрации белка менее 3 г/л проба может быть отрицательна, что встречается довольно редко, так как обычно концентрация белка Бенс-Джонса в моче весьма значительна.
Наиболее достоверно выявление белка Бенс-Джонса осаждением при температуре 40-60°С. Однако в слишком кислой (рН менее 3,0) или слишком щелочной (рН более 6,5) моче, при низкой относительной плотности мочи и низкой концентрации бежа Бенс-Джонса (менее 3 г/л) осаждение может не происходить.
Зарисуйте схему определения белка
II модуль. Самостоятельная работа с исследовательским этапом
Методические установки:
Задание №1. Изучите и законспектируйте приложение №1 «Обнаружение белка с помощью диагностических тест-полосок»
Задание №2.
— Получите образцы биологической жидкости (мочи) у преподавателя, пронумеруйте образцы;
— Проведите исследование мочи с помощью диагностических тест-полосок;
— Оцените полученный результат (норма, патология). Предположите причину возникновения белка в моче.
— Результат запишите в бланки анализа, сдайте их преподавателю.
Приложение №1
«Обнаружение белка с помощью диагностических тест-полосок»
Принцип. Белок изменяет цвет индикатора, нанесенного на полоску. Индикаторы упакованы в комплекте по 100 полосок, которые хранятся в плотно закрытом пенале, прохладном и сухом месте.
Правила работы с диагностическими тест-полосками
При работе с диагностическими тест-полосками необходимо соблюдать следущие правила:
— держать диагностические тест-полоски в плотно закрытых упаковках-пеналах;
— хранить пеналы в темном, сухом, прохладном месте при температуре, не превышающей 30ºС, но не в холодильнике;
— не подвергать полоски действию влаги и прямого солнечного света, высокой температуры и летучих химических веществ;
— доставать только строго необходимое количество полосок, после чего немедленно закрывать пенал;
— не дотрагиваться пальцами до диагностических зон.
Правила проведения теста
1. Для исследования используйте утреннюю мочу, собранную в одноразовый пластиковый контейнер для мочи (или чистую сухую посуду). Перемешайте доставленную мочу, но не центрифугируйте.
Внимание!
При использовании нестандартной приспособленной тары остатки моющих средств в посуде для сбора мочи являются причиной ложных результатов.
2. Из пенала возьмите тест-полоску.
3. Сразу же закройте пенал фабричной крышкой, полоску охраняйте от влаги.
4. Индикаторные бумажные зоны полоски опустите на 2-3 секунды в исследуемую мочу и сразу же выньте.
5. Для удаления избытка влаги с диагностических зон полоски проведите ее длинным краем по краю контейнера (или иной емкости, в которой доставлена моча) или приложите этот край полоски к фильтровальной бумаге.
Смывать с диагностических зон полоски лишнюю мочу нельзя!!!
6. По истечении времени, указанного на этикетке пенала или в инструкции к каждому тесту, сравните цвет соответствующей диагностической зоны с цветной шкалой на этикетке пенала с полосками (эталоном). Порядок проведения теста представлен рисунками 1-7.
7. Реакцию оценивают как положительную или отрицательную. Или выражают в цифровом обозначении в г/л. (см. рисунок №8).
Рис. №8 Оценка результатов исследования
III Модуль. Контрольные вопросы и задания
Ответьте на поставленные вопросы, используя рабочую тетрадь
Расскажите метод определения белка в моче 50% азотной кислотой.
Расскажите метод определения белка в моче 20 % ССК.
Расскажите методику определения белка в моче методом Робетса — Стольникова — Бранберга.
Расскажите методику определения белка в моче диагностическими тест- полосками.
Какие существуют правила работы с диагностическими тест-полосками.
Назовите основные критерии правильно проведенного теста.
Расскажите методику обнаружения в моче белка Бенс-Джонса.
Диагностическое значение определения химических свойств мочи.
Клиническая оценка химических свойств мочи.
Запишите в рабочей тетради термины и дайте им обозначение, используя изученный материал
Домашнее задание:
Знать теоретический и практический материал.
Отвечать на контрольные вопросы.
Знать термины.
Литература для самостоятельной подготовки: И.И.Миронова, Л.А.Романова, В.В.Долгов. Общеклинические исследования: моча, кал, ликвор, эякулят.- М.-Тверь: ООО «Издательство «Триада», 2005
Источник