Чем лечить аденому в мочевом пузыре
Содержание статьи
Доброкачественная опухоль мочевого пузыря
Опухолью мочевого пузыря называют доброкачественное новообразование, возникающее на его стенках. Наиболее часто патологические процессы происходят на задней и боковых стенках пузыря, шейке, в мочепузырном треугольнике (треугольник Льето), изменяя количественный и качественный состав клеток эпителия слизистых оболочек.
Доброкачественная опухоль мочевого пузыря, как правило, локализуясь на определённом участке поверхностей, изменяет его клетки, в результате чего образуются полипы, аденомы, эндометриоз, феохромоцитомы (фиброепителиомы), лейомиомы, рабдомиомы, невриномы и папилломы в мочевом пузыре, где преимущественно располагаются все опухоли мочевыделительной системы. Мужское население от 50 до 70 лет заболевает опухолевыми болезнями мочевого пузыря в 4 раза чаще, чем женское.
Эпителиального происхождения доброкачественные опухоли встречаются у 95-98% больных в виде папиллом и полипов, которые при озлокачествлениипроцесса могут перейти в разные виды рака мочевого пузыря и аденокарциному (90-96% от всех опухолей мочевого пузыря). Папиллома мочевого пузыря, невзирая на её морфологически доброкачественнуюструктуру, определяется как предраковая опухоль, потому как имеет склонность к частым рецидивами перерождению в злокачественную.
Доброкачественные опухоли мочевого пузыря отличаются отсутствием метастазирования, поражения здоровых тканей вокруг и продолжением роста после оперативного удаления. Самую большую распространенность среди мужчин после 45 лет получила аденома, хотя за последние десятки лет она значительно «помолодела».
Неэпителиального происхождения (из соединительной ткани) опухоли мочевого пузыря в виде фибром, миом, гемангиом, фибросарком — очень редко встречающиеся новообразования, хотя саркомы, дающие лимфогенные и гематогенные метастазы на ранних стадиях, определяются гораздо чаще.

Классификация опухолей мочевого пузыря
Доброкачественныеопухоли делятся на группы эпителиальногои неэпителиальногопроисхождения. К эпителиальным условно доброкачественным опухолям относятся:
- Папилломы, представляющие собой многочисленные длинные разветвленные ворсинки со множеством кровеносных сосудов, которые определяются как потенциально злокачественные, т.к. склонны к малигнизированию.
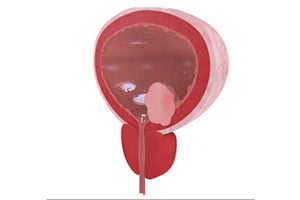
- Аденома (гиперплазия) предстательной железы, образующаяся из клеток слизистой мочевого пузыря или стромальной составляющей предстательной железы. Она имеет узелки, которые при увеличении размеров сдавливают мочевыводящий канал, мешая процессу мочеотделения.
- Эндометриозмочевого пузыря — это опухоль, являющаяся итогом гормональных нарушений, когда имеется избыток эстрогенов и дефицит прогестерона, с губчатой структурой из разнокалиберных кист на стенке, выпирающих в пузырь, на фоне повышенной отечности и гиперемии околослизистого пространства. Эндометриоз зависим от менструального цикла, имеет склонность к озлокачествлению клеток.
- Полипы — это выступающие над слизистым слоем мочевого пузыря патологические разрастания тканей.
- Феохромоцитома — нейроэндокринная опухоль в мышечном слое шейки, образовавшаяся из клеток хромаффинной ткани, выделяющей переизбыток катехоламинов.
- Типичная фиброэпителиома — нежное ворсистое новообразование на ножке, которое может размножиться.
- Атипичная фиброэпителиома — ворсинчатое образование с более грубыми ворсинками на более толстой ножке, с умеренно отечной и гиперемированной слизистой оболочкой вокруг. При объединении с папилломатозом она опасна перерождением в злокачественную опухоль.
К неэпителиальным доброкачественным опухолям мочевого пузыря относятся фибромы, миомы, фибромиксомы, гемангиомы, липомы, лимфангиомы, опухоль Абрикосова (зернистоклеточная опухоль), невриномы, встречающиеся в урологической практике относительно нечасто.
Прогноз и профилактика доброкачественных опухолей мочевого пузыря
В основной практике полипы и папилломы продолжительное время могут никак себя не проявлять, поэтому их обнаружение и лечение на запущенных стадиях озлокачествления редко даёт положительные результаты. Чтобы избежать усложнений заболевания, люди из группы риска должны периодически обследоваться, избавляться от провоцирующих опухолеобразование болезней, вести здоровый образ жизни и находиться под наблюдением врача. Послеоперационный период при неосложненных новообразованиях длится недолго, и возврат к нормальной полноценной жизни равен практически 100%.
Причины развития доброкачественных опухолей мочевого пузыря
Этиология развития опухолей мочевого пузыря окончательно не определена, однако, исходя из известных факторов, определяются следующие:
- анилиновые красители, особенно их производные — ароматические амины с их конечными метаболитами (бензидином, нафтиламином и др.), обладающие канцерогенным действием на работников лакокрасочных, бумажных, химических и резиновых производств;
- различные канцерогены окружающей среды, попадая в организм и выводясь с мочой, приобретают патологическое влияние на уротелий при застое мочи;
- курение и стаз мочи являются толчковым механизмом к образованию опухолей мочевого пузыря, когда ортоаминофенолы (продукты конечного обмена аминокислоты триптофана) вызывают разрастание клеток эпителия мочевыводящего тракта;
- возраст и пол больного, анатомические особенности строения мужской мочевыводящей системы, морфологические отличия слизистой пожилых людей, часто приводящие к застою мочи;
- наличие и частота воспалительных заболеваний уретры и мочевого пузыря, таких как шеечный цистит, простатит, мочекаменная болезнь, лейкоплакия, изъязвления мочевого пузыря;
- нарушения гормонального фона, снижение активности Т-системы иммунитета;
- паразитарные инвазии типа бильгарциоза, шистомоза и другие.
Кроме этого, существует обсуждаемая тема в мировой медицине о вирусном происхождении новообразований в мочевом пузыре.
Симптомы доброкачественных опухолей мочевого пузыря
Доброкачественная опухоль мочевого пузыря, симптомы которой обычно никак не проявляются, обнаруживается, как правило, случайно. Основные и наиболее выраженные симптомы доброкачественных опухолей:
- гематурия различных типов выраженности (микро-, макрогематурия, тотальная, терминальная): главный симптом при любой доброкачественной опухоли — это наличие крови и её сгустков в мочевой жидкости на различных этапах мочеиспускания у большинства пациентов, что отличает виды и стадии опухоли;
- дизурия — затрудненное мочеиспускание, наблюдаемое у трети пациентов с частотой, увеличивающейся в результате ухудшения состояния больного;
- вторичный цистит и восходящий пиелонефрит как результат распада новообразования;
- различной выраженности дискомфорт, жжение или болезненность при мочеиспускании;
- докучающие позывы к мочеиспусканию;
- недержание мочи у мужчин и женщин;
- ложные позывы к дефекации, боль, распространяющаяся в промежность, прямую кишку, крестец при опухоли шейки мочевого пузыря;
- нарушение опорожнения мочевого пузыря при сжимании устьев мочеточников опухолями приводит к проявлению признаков хронической почечной недостаточности, пиелонефроза и уретерогидронефроза;
- болевые ощущения, рези внизу живота, локализующиеся в лобковой, а затем и в паховой области.
Иногда, вследствие перекручивания полипа или папилломы пузыря, происходит острое нарушение кровообращения, ведущее к инфаркту новообразования, что сопровождается усилением гематурии. Доброкачественные опухоли мочевого пузыря являются катализаторами рецидивов воспалительных заболеваний мочевыводящих путей — циститов, восходящих уретеропиелонефритов.
Опасность перерождения доброкачественных тканей папиллом мочевого пузыря в злокачественные наиболее велика у заядлых курильщиков. Папилломы мочевого пузыря имеют склонность к повторному прорастанию с непредсказуемой периодикой, с каждым рецидивом становясь более злокачественными, чем прежде удаленные опухоли.
Обнаружили симптомы данного заболевания?
Звоните
Наши специалисты проконсультируют Вас!
Диагностика доброкачественных опухолей мочевого пузыря
Чтобы выявить и достоверно определить наличие, тип и стадию опухоли мочевого пузыря, необходимо провести комплексную диагностику пациента всеми доступными в настоящее время методами. Особенно следует отметить следующие.
Бимануальная пальпация (ручное исследование) — обязательное исследование, однако маленькие опухоли, выросшие вовнутрь, как правило, не пальпируются, а новообразование, которое удалось пальпировать, указывает на распространившееся проникающее поражение мочевого пузыря.
Ряд клинических и биохимических анализов крови и мочи через определённые этапы времени, позволяющие провести точную оценку развития заболевания.
Рентгенологическое исследование пузыря с введением контрастного вещества (экскреторная урография) в полость пузыря для определения дефекта наполнения его мочевой жидкостью и определения состояния его слизистой оболочки. Иногда это исследование проводят в условиях двойного контрастирования, вводя кислород в мочевой пузырь и окружающую его клетчатку, чтобы уточнить степень инфильтрации стенки пузыря и распространения её на окружающие участки.
Эндоскопическое исследование полости пузыря (цистоскопия) предоставляет его внутреннюю картину, помогает с достаточной точностью определить вид опухоли, её характеристики и площадь поражения с обязательным получением тканей и мочи для бактериологического анализа.
Цитологический анализ мочевой жидкости с целью выявления атипичных клеток проводится в случаях, когда нет возможности произвести биопсию на гистологию.
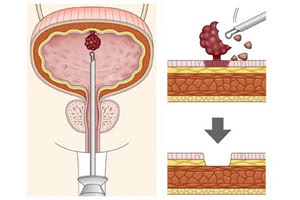
Трансуретральная пункционная биопсия тканей опухоли для определения их гистологии выполняется как отдельная процедура или при трансуретральной резекции мочевого пузыря.
УЗИ (ультразвуковое исследование) пузыря и органов малого таза выявит новообразование, его вид, размеры, экспозицию и широту распространенности.
Использование магнитно-резонансной и компьютерной томография почек с введением контрастного вещества позволит обнаружить опухоль пузыря, степень её прорастания в стенки и соседние органы, развитие метастазов в регионарных лимфатических узлах.
Экскреторная томография с введением контрастных веществ в вену позволит осуществить контроль над их выходом из почек и последующим выводом из организма.
Лечение доброкачественных опухолей мочевого пузыря
Хирургическое удаление является обязательным при диагностике доброкачественных новообразований методом трансуретральной резекции, эндоскопии, электро- или лазерной коагуляции опухоли. Также предписывается полное удаления мочевого пузыря в случае значительного вовлечения его и уретры в опухолевый процесс.
Лекарственное лечение обычно бывает направлено на укрепления местного и общего иммунитета.
Противовоспалительная, противопаразитарная и противовирусная терапия назначается при необходимости.
Данная статья размещена исключительно с целью ознакомления в познавательных целях и не является научным материалом или профессиональным медицинским советом. За диагностикой и лечением обратитесь к врачу.
Источник
Лечение симптомов патологии нижних мочевых путей при аденоме предстательной железы. Часть 3
Алгоритм лечения аденомы простаты основан на сочетании степени симптомов, количества беспокойства и размера органа (при этом ПСА используется в качестве маркера размера у пациентов без клинических признаков рака).
Варианты лечения аденомы предстательной железы, протекающей с симптомами мочевых путей
Варианты лечения включают:
- изменение образа жизни;
- ожидание, сопровождающееся динамическим наблюдением;
- фармакологические препараты;
- нехирургические процедуры;
- хирургические операции.
Лечение, будь то консервативное или более агрессивное, направлено на улучшение оттока мочи, облегчение симптомов, которые может испытывать человек, и задержку или предотвращение прогрессирования гиперплазии. Выбор тактики с точки зрения пациента может отличаться от выбора врача. Выбор правильного лечения лучше проводить не только исходя из личных предпочтений пациента, а совместно с рекомендациями уролога (у которого есть опыт и необходимые знания).
Каждый вариант лечения облегчит и улучшит симптомы, но каждый из них имеет различные риски, осложнения и шансы на успех. Крайне важно, чтобы предпочтения пациента в отношении конкретного лечения были сопоставлены с тяжестью симптомов и конкретными физиологическими переменными, используемыми при постановке диагноза урологом.
Пациенты, которые обращаются за лечением, как правило, имеют умеренные или тяжелые симптомы (например, баллы по шкале IPSS 8 или выше) и увеличение предстательной железы.
Динамическое наблюдение и изменение образа жизни
Динамическое наблюдение — это стратегия управления, во время которой пациент находится под наблюдением врача, но не получает медицинской помощи в виде серьезных лекарств и хирургических методов терапии. Такое бдительное ожидание вместе с изменением образа жизни и периодической переоценкой наиболее подходит пациентам с легкой формой доброкачественной гиперплазии простаты (то есть 7 или менее баллов по результатам анкеты) и/или без каких-либо беспокоящих симптомов, независимо от размера предстательной железы.
Уровень симптоматического дистресса, который пациент может терпеть, значительно варьируется. Поэтому динамическое наблюдение может быть выбором пациента, несмотря на высокий индекс симптомов Американской урологической ассоциации (AUA-SI) или оценку IPSS (напомним, INTERNATIONAL PROE SYMPTOM SCORE или международная оценка симптомов простаты, анкета, которую пациент заполняет во время консультации уролога).
Предлагаются различные изменения образа жизни, включающие:
- ограничение жидкости;
- отказ от раздражающих продуктов или напитков (например, кофеина, алкоголя);
- отказ и/или контроль приема некоторых лекарств (например, мочегонных, противоотечных, антигистаминных, антидепрессантов);
- своевременное мочеиспускание;
- упражнения для тазового дна;
- устранение запоров.
![]() Отказ от спиртного
Отказ от спиртного
Фармакотерапия аденомы предстательной железы
Для использования лечения аденомы простаты одобрены альфа-адренергические антагонисты (альфа-адреноблокаторы) и 5-ARIs (они же ингибиторы 5α-редуктаз). Правда фармакологическая терапия не всегда является столь эффективной, как хирургическое вмешательство, она способна обеспечить хорошее облегчение симптомов.
Таблица 5. Общие препараты, применяемые для лечения доброкачественной гиперплазии простаты
| Альфа-адреноблокаторы | Дозировка | Побочные эффекты |
| Теразозин | 1 мг один раз в день для начала; доза может увеличиваться до 20 мг/сут. | Астения, гипотония, головокружение, сонливость. |
| Доксазозин | 1 мг один раз в день в начале; дозировка может увеличиваться до 8 мг один раз ежедневно | Ортостатическая гипотензия, утомляемость, одышка |
| Тамсулозин | 0,4 мг один раз ежедневно | Головокружение, ринит, нарушение эякуляции |
| Альфузозин | 10 мг одинежедневно | Усталость, отек, ринит, головная боль, инфекции верхних дыхательных путей |
| Ингибиторы ферментов 5α-редуктаз | ||
| Финастерид | 5 мг, таблетки однократно в день | Импотенция, нарушение либидо (снижение), уменьшение количества спермы при эякуляции, снижение ПСА в сперме, гинекомастия (редко) |
| Дутастерид | 0,5 мг однократно в сутки | Импотенция, нарушение либидо, уменьшение количества спермы при эякуляции, снижение ПСА в сперме, гинекомастия (редко) |
Препараты альфа-адреноблокаторов
К альфа-адреноблокаторам второго поколения относятся доксазозин и теразозин, к подгруппе третьего поколения относятся альфузозин и тамсулозин. Они рекомендованы урологическими ассоциациями (например, американской AUA, канадской CUA) в качестве вариантов лечения лиц с СНМП, вторичными по отношению к доброкачественной гиперплазии простаты. Альфа-блокаторы первого поколения и празозин не рекомендуются.
Механизм действия альфа-адреноблокаторов приводит к расслаблению гладкой мускулатуры как простаты, так и шейки мочевого пузыря, поскольку ингибируют симпатическую стимуляцию, опосредованную α-адренорецепторами.
α-адреноблокаторы второго и третьего поколения хорошо зарекомендовали себя при лечении симптомов нижних мочевых путей, возникающих из-за дисплазии. Несмотря на то, что есть небольшие различия в их побочных эффектах, они считаются одинаково клинически эффективными и обеспечивают наиболее быстрое облегчение симптомов.
- Плюсы их применения: альфа-адреноблокаторы действительно улучшают симптомы.
- Минусы применения: они не обеспечивают длительного снижения возможности острой задержки мочеиспускания и не отодвигают хирургическое вмешательство, связанное с заболеванием.
![]() Препараты альфа-адреноблокаторов
Препараты альфа-адреноблокаторов
Препараты третьего поколения тамсулозин и альфузозин, в отличие от альфа-адреноблокаторов второго поколения, не нуждаются в корректировке дозировки с течением времени. Считается, что они более эффективны. Они избирательно расслабляют гладкие мышцы простаты, следовательно, они не оказывают влияние на артериальное давление.
Основные нежелательные явления, о которых сообщалось при приеме альфа-адреноблокаторов, — ортостатическая гипотензия, головокружение, усталость (астения), проблемы с эякуляцией и заложенность носа. Риск головокружения ниже при приеме тамсулозина и альфузозина, чем при приеме препаратов второго поколения. Обнаружено, что тамсулозин имеет более низкую вероятность ортостатической гипотензии, но более высокую частоту эякуляторной дисфункции (10%). Он не вызывает эректильной дисфункции или снижения полового влечения.
Урологу обсуждает с пациентом подходящий альфа-блокатор для лечения с учетом индивидуального состояния.
Препараты 5-ARIs или ингибиторов 5α-редуктаз
Дутастерид и финастерид, которые относятся к ингибиторам ферментов 5α-редуктаз, действуют, блокируя переход тестостерона в DHT или дигидротестостерон. DHT — андроген, который отвечает за увеличение предстательной железы.
Класс ингибиторов ферментов 5α-редуктаз представляет собой единственную в настоящее время фармакотерапию, которая демонстрирует как эффективность, так и приемлемую безопасность для медикаментозного лечения ДГПЖ. Продемонстрировано, что снижение DHT вызывает апоптоз и атрофию эпителиального эпителия простаты. Следовательно, обоснование использования 5-ARIs для терапии аденомы простаты заключается в снижении сывороточных и особенно клеточных уровней дигидротестостерона, приводя к уменьшению размера простаты.
Финастерид, который ингибирует изоферменты 5-AR (альфа-редуктазы) типа 2, подавляет сывороточный DHT на 70,8% ± 18,3% через 24 недели, но не до критических уровней.
Дутастерид обеспечивает более высокий уровень подавления сывороточного дигидротестостерона (95% ± 3%) и способен подавлять как 1-й, так и 2-й тип изоферментов 5-альфа-редуктаз. Согласно рекомендациям Американской и Канадской Урологических Ассоциаций, оба препарата подходят для применения при наличии симптомов нижних мочевыводящих путей, связанных с очевидным увеличением предстательной железы. Однако их не следует использовать, когда отсутствует увеличение простаты.
Проведено четырехлетний анализ долгосрочной эффективности, также безопасности применения препарата Проскар (Proscar, МНН финастерид). Установлено, что прием препаратов привел:
- к уменьшению размера/объема простаты на 18%. При использовании плацебо орган увеличился на 14% (p <0,0001);
- к улучшению оценки симптомов, оценка проводилась с использованием подсчета по баллам AUA-SI (2,6 балла против 1,0 для плацебо; p <0,001);
- и снизило по сравнению с плацебо риск ОЗМ на 51% и хирургического вмешательства на 55% (p <0,001 для обоих).
Применение финастерида в недавно опубликованной работе «Медицинская терапия простатических симптомов» (MTOPS) уменьшило величину простаты на 19%, но, что более важно, снизил риск клинического прогрессирования на 34% (до 2,9 на 100 человеко-лет) по сравнению с плацебо.
![]() Препараты 5-ARIs или ингибиторов 5α-редуктаз
Препараты 5-ARIs или ингибиторов 5α-редуктаз
Применение дутастерида (исследование проводилось в течение двух лет) продемонстрировало снижение размеров предстательной железы примерно на 26%, которое сохранялось в течение дополнительных 2 лет. Лечение дутастеридом также сопровождалось улучшением симптоматики на 4,5 балла (против 2,3 балла для плацебо; p <0,001), снижением рисков ОЗМ на 57%, уменьшением хирургического вмешательства на 48%. Недавно опубликована исследовательская работа CombAT (лечение комбинацией аводарта и тамсулозина). Специалисты изучили и сравнили данные применения дутастерида, тамсулозина и их комбинированного приема в первые два года.
Впервые выяснилось, что в популяции пациентов с величиной простаты более 30 см3 и показателем ПСА> 1,5 нг/мл (оптимальная популяция для терапии 5-ARI) лечение ингибиторами 5α-редуктаз (а именно дутастеридом) привело к значительно большему уменьшению симптомов, чем альфа-блокатор тамсулозин.
Установлено, что оба препарата (финастерид, дутастерид) снижают содержание ПСА примерно на 50% через полгода. Это подавление ПСА с течением времени сохраняется. Если уровень ПСА повышается при приеме этой группы препаратов, следует проверить режим их приема пациентом и удостовериться, что препарат надлежащего качества.
Комбинированная терапия
Пациентам при наличии увеличенной предстательной железы с симптомами обструкции выходного отверстия мочевого пузыря рекомендовано лечение как ингибиторами 5α-редуктаз, так и альфа-адреноблокаторами. Обоснование этой рекомендации — быстрое облегчение симптомов альфа-адреноблокатором с одной стороны и более длительное облегчение симптомов с помощью 5-ARI с другой стороны. Что еще более важно, 5-ARI снизит риск серьезных осложнений, таких как острая задержка мочи и/или необходимость хирургического вмешательства по поводу аденомы простаты.
В исследовании «медицинской терапии симптомов простаты» MTOPS риск прогрессирования при комбинированной терапии (финастерид и доксазозин) снизился на 66%. В дополнение к этому открытию, ученые установили, что потребность в хирургическом вмешательстве и риск ОЗМ были снижены при комбинированной терапии и при применении финастерида отдельно, но не при монотерапии доксазозином. Аналогичным образом исследование CombAT показало через 2 года, что уменьшение симптомов и беспокойства, а также вопрос 8 IPSS (качество жизни) были значительно выше при комбинированной терапии (дутастерид и тамсулозин), чем при любом режиме монотерапии.
Результаты исследования «Управление симптомами после сокращающей терапии» (SMART) и PROACT (комбинация Проскара и альфа-блокатора с последующим испытанием прекращения терапии) показывают, что для большинства пациентов альфа-блокатор можно безопасно отменить через 6-9 месяцев комбинированной терапии без снижения эффективности. Потенциальные преимущества отмены альфа-адреноблокатора включают более низкую стоимость, меньшее количество побочных эффектов и лучшее соблюдение режима лечения. Следовательно, если пациент хорошо себя чувствует на комбинированной терапии, целесообразно отменить альфа-блокаторы через полгода.
Фитохимические вещества для облегчения симптомов аденомы простаты
Фитохимические вещества — растительные соединения, которые обладают защитными или профилактическими свойствами. В последнее время интерес к их использованию для лечения ДГПЖ возобновился и растет. Исследования их эффективности проводятся, однако полученные результаты были неоднозначными, большинство исследований, связанных с фитохимическими веществами, не подвергалось таким же строгим доклиническим фармакологическим испытаниям и крупномасштабным клиническим испытаниям, которые проводятся с альфа-блокаторами и 5-ARI.
Наиболее полно описано и изучено фитотерапевтическое средство Serenoa repens (Сереноа ползучая). Применение этого препарата продемонстрировало эффективность от слабой до умеренной:
- в уменьшении никтурии;
- в увеличении максимального потока мочи;
- улучшении Международной шкалы симптомов простаты (IPSS) у мужчин с ДГПЖ, с результатами, сопоставимыми с эффективностью/результатами тамсулозина.
Однако другие испытания не показали значительного положительного эффекта S. repens по сравнению с плацебо. Проведенный недавно Кокрановский обзор пришел к выводу, что S. repens не более эффективен, чем плацебо для лечения симптомов мочеиспускания при доброкачественной гиперплазии простаты.
Еще одно популярное альтернативное средство лечения аденомы простаты — Pygeum africanum, экстракт африканского чернослива. В Кокрановском обзоре, показано, что его прием обеспечивает умеренное уменьшение проблем с мочеиспусканием, вызванных ДГПЖ. Однако исследования были небольшими, длились недолго, не проверялись различные дозы и препараты, и в большинстве случаев не использовались стандартизованные, проверенные меры оценки эффективности.
Хирургия, связанная с аденомой простаты
Хирургическое лечение аденомы простаты необходимо:
- если медикаментозное лечение не дает результатов;
- если доброкачественная обструкция предстательной железы вызывает почечную недостаточность, задержку мочи, рецидивирующие инфекции мочевыводящих путей, камни в мочевом пузыре или гидронефроз.
Варианты хирургического вмешательства включают:
- трансуретральную резекцию простаты. (ТУР);
- трансуретральную инцизию простаты (ТУИП). ТУИП рекомендуется для предстательной железы массой менее 30 г;
- открытая простатэктомия (рекомендуется для предстательной железы более 100 г);
- трансуретральная электровапоризация простаты (ТУВП);
- лазерная простатэктомия.
Трансуретральная резекция простаты
Возможны послеоперационные риски, такие как эректильная дисфункция, ретроградная эякуляция и недержание мочи (редко). Частота рецидивов ДГПЖ в течение 5 лет после операции составляет от 2% до 10%.
Менее инвазивные хирургические методы лечения (называемые минимально инвазивной терапией или MIST) включают трансуретральную микроволновую терапию (ТУМТ), трансуретальная игольчатая абляция (ТУНА или TUNA) и интрапростатические стенты.
Продолжение статьи
- Доброкачественная гиперплазия предстательной железы — характеристика патологии. Часть 1.
- Диагностика симптомов нижних мочевых путей, связанных с гиперплазией предстательной железы. Часть 2.
- Алгоритм лечения симптомов патологии нижних мочевых путей при аденоме предстательной железы. Часть 3.
Источник